下列有关性质的比较错误的是
| A.热稳定性:H2S<HCl | B.电负性:Cl>Br |
| C.第一电离能:S<P | D.离子半径:K+>Cl- |
更新时间:2024-01-02 10:45:19
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列关于元素金属性和非金属性强弱比较的说法不正确的是
A.根据气态氢化物的热稳定性: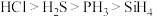 ,可得非金属性: ,可得非金属性: |
B.Si与 化合所需的温度远高于S与 化合所需的温度远高于S与 化合所需的温度,说明S的非金属性强于Si 化合所需的温度,说明S的非金属性强于Si |
| C.Na与冷水反应剧烈,而Mg与冷水反应缓慢,说明Na的金属性强于Mg |
D.铁投入 溶液中能置换出铜,钠投入 溶液中能置换出铜,钠投入 溶液中不能置换出铜,不能由此判断钠与铁的金属性强弱 溶液中不能置换出铜,不能由此判断钠与铁的金属性强弱 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】短周期元素X、Y、Z、W在元素周期表中的相对位置如下所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是
| Y | Z | ||
| X | W |
| A.原子半径:X<Y<Z |
| B.气态氢化物的稳定性:X>Z |
| C.Z、W均可与Mg形成离子化合物 |
| D.只含Z元素的物质一定是纯净物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列离子半径大小比较错误的是( )
| A.Na+>F- | B.K+>Li+ | C.I->Br- | D.Na+<O2- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关微粒性质的排列顺序中,错误的是
| A.元素的电负性:P<O<F |
| B.元素的第一电离能:C<N<O |
| C.离子半径:O2->Na+>Mg2+ |
| D.原子的未成对电子数:Mn>Si>Cl |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】 、
、 是同周期的两种非金属元素,不能说明
是同周期的两种非金属元素,不能说明 元素的非金属性比
元素的非金属性比 元素的非金属性强的事实是
元素的非金属性强的事实是
①将 的单质通入
的单质通入 溶液中产生
溶液中产生 单质
单质
②加热至 ,
, 发生分解而
发生分解而 不分解
不分解
③第一电离能:
④电负性:
⑤单质的熔点:
⑥气态氢化物的水溶液的酸性:
⑦ 与
与 形成的化合物
形成的化合物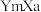 中
中 元素显负价
元素显负价
 、
、 是同周期的两种非金属元素,不能说明
是同周期的两种非金属元素,不能说明 元素的非金属性比
元素的非金属性比 元素的非金属性强的事实是
元素的非金属性强的事实是①将
 的单质通入
的单质通入 溶液中产生
溶液中产生 单质
单质②加热至
 ,
, 发生分解而
发生分解而 不分解
不分解③第一电离能:

④电负性:

⑤单质的熔点:

⑥气态氢化物的水溶液的酸性:

⑦
 与
与 形成的化合物
形成的化合物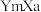 中
中 元素显负价
元素显负价| A.2项 | B.3项 | C.4项 | D.5项 |
您最近一年使用:0次
单选题
|
较易
(0.85)
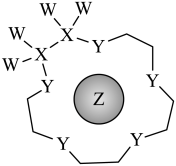
【推荐2】一种由短周期主族元素X、Y、Z、M组成的化合物A(如图所示),其是选择性强和稳定性好的极性溶剂,高精密电子、电路板、锂电池的优良清洗剂。四种元素原子序数之和为22,Y、Z、M均为同周期元素。下列说法正确的是

| A.化合物A中所有原子均达到8电子稳定结构 |
| B.化合物A中Y、Z两种原子的杂化方式相同 |
| C.Y、Z、M三种元素最高价氧化物的水化物均为强酸 |
D.Y、Z、M三种元素的第一电离能由大到小: |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】某化合物(结构如图所示)可用作酿造酵母的培养剂、强化剂、膨松剂、发酵助剂。已知X、Y、Z、W为元素周期表中前20号元素且位于不同周期,原子序数依次增大,Y为地壳中含量最高的元素。下列有关说法正确的是
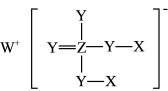
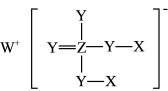
| A.X分别和Y、W形成的化合物中,所含化学键类型相同 |
| B.同周期中第一电离能比Z小的元素只有4种 |
| C.电负性:Y>Z>W |
| D.X与Z形成的最简单化合物比X与Y形成的最简单化合物稳定 |
您最近一年使用:0次
【推荐2】下列微粒对应的元素电负性最大的是
A. |
B.基态原子核外电子排布式: |
C.基态原子价电子排布图: |
| D.第二周期元素基态原子p能级电子数比s能级电子数多1 |
您最近一年使用:0次


 键的数目为61
键的数目为61

