下列判断不正确的是
| A.电负性:P<S<Cl | B.沸点:Cl2<Br2<I2 |
| C.微粒半径:Li+<O2-<Na+ | D.键角:BF3>CH4>H2O |
更新时间:2023-12-25 14:57:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】五种短周期元素X、Y、Z、M、W的原子序数与其常见化合价的关系如图所示,则下列有关的叙述中,不正确的是


| A.元素X可能为锂 |
B.原子半径大小: |
| C.元素气态氢化物的稳定性:Y>M |
D.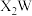 中各原子均达到8电子稳定结构 中各原子均达到8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】W、X、Y、Z、Q均为短周期主族元素,且原子序数依次增加,由它们组成的单质或化合物存在以下转化关系。已知B、C、D为非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒;化合物G的焰色试验呈黄色;化合物H常温常压下为液体。下列说法不正确的是


| A.原子半径:Z>X>Y>W |
| B.最高价氧化物的水化物的酸性:Q>X |
| C.化合物WQY中各原子均满足8电子稳定结构 |
| D.化合物ZYW中含有离子键和极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y、Z可形成结构如图所示的“糖葫芦”分子。X、Y、Z位于同周期,其中X是该周期中原子半径最大的元素。下列有关说法正确的是
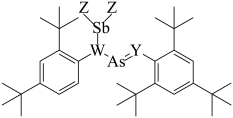

| A.电负性:Z>Y | B.原子半径:W>Y |
| C.简单气态氢化物的沸点:Z>W | D.工业上常用电解饱和XZ溶液的方法来制取X单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R五种短周期元素的最高正化合价和原子半径见下表。
下列有关说法正确的是
| 元素 | X | Y | Z | W | R |
| 最高正化合价或最低负化合价 |  |  |   |   |   |
| 原子半径/nm | 0.074 | 0.143 | 0.075 | 0.102 | 0.077 |
| A.简单气态氢化物的热稳定性:W>X |
B.Y、R形成的化合物可表示为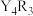 |
C.简单离子半径: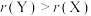 |
| D.电负性:Z>X |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】Li2O的Born-Haber循环如图所示,下列说法正确的是


| A.金属锂的原子化热为318 kJ/mol | B.Li的第一电离能为1040kJ/mol |
| C.O=O键的键能为249kJ/mol | D. 的晶格能为2908kJ/mol 的晶格能为2908kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】Fe3+的配位化合物较稳定几用途广泛。Fe3+可与H2O、SCN-、F-等配体形成溶液呈浅紫色的[(Fe(H2O)6]3+、红色的[Fe(SCN)6]3+、无色的[FeF6]3+配离子。某同学按如下步骤完成实验:

已知:向Co2+的溶液中加入KSCN溶液生成蓝色的[Co(SCN)4]2+的配离子;Co2+不能与F-形成配位离子。下列说法正确的是
| A.可用NaF和KSCN溶液检验FeCl3溶液中是否含有Co2+ |
| B.Fe第四电离能(I4)小于第三电离能(I3) |
| C.向溶液I中滴加少量NaOH溶液,溶液逐渐变为浅紫色 |
| D.配离子[(Fe(H2O)6]3+中H-O-H的键角与H2O分子中H-O-H的键角相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列化学用语表示不正确 的是
A. 分子的空间填充模型: 分子的空间填充模型: | B. 的结构式: 的结构式: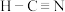 |
C. 的电子式: 的电子式: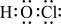 | D. 中B的杂化轨道模型: 中B的杂化轨道模型: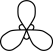 |
您最近一年使用:0次
【推荐2】下列说法不正确的是
| A.激光、焰色试验、原子光谱等与电子跃迁有关 |
| B.硫化氢晶体中,一个硫化氢分子周围有12个紧邻分子 |
| C.某元素基态原子的最外层电子排布式为4s1,则该元素为IA族元素 |
D.CO 与SO 与SO 中,O-C-O键角大于O-S-O键角 中,O-C-O键角大于O-S-O键角 |
您最近一年使用:0次

 ,将
,将 转化为
转化为 ,反应过程如图所示。下列说法错误的是
,反应过程如图所示。下列说法错误的是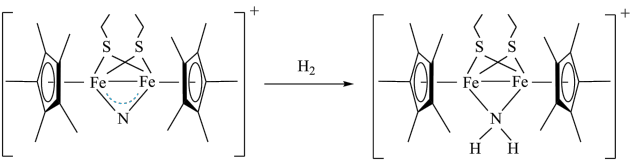

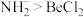
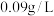 ,Y的同位素可用于测定文物年代,Z元素的某种单质可用作自来水消毒剂,下列说法正确的是
,Y的同位素可用于测定文物年代,Z元素的某种单质可用作自来水消毒剂,下列说法正确的是


