已知由一种阳离子与两种酸根阴离子组成的盐称为混盐。向混盐CaOCl2中加入足量浓硫酸,发生反应:CaOCl2+H2SO4(浓)=CaSO4+Cl2+H2O。下列说法不正确的是
| A.CaOCl2中的两种酸根阴离子分别为Cl-和ClO- |
| B.CaOCl2和Cl2中均含有非极性共价键 |
| C.在上述反应中,浓硫酸不体现氧化性 |
| D.每产生标准状况下2.24LCl2,转移电子的数目约为6.02×1023 |
更新时间:2024-01-04 10:27:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】硫及其化合物的转化具有重要应用。下列说法不正确的是 )
A.实验室制取少量 的原理: 的原理: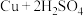 (浓) (浓)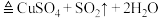 |
B.实验室检验 既具有氧化性也具有还原性: 既具有氧化性也具有还原性: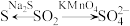 |
C.工业上接触法制硫酸过程中物质转化: |
D.工业上用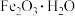 脱除天然气中的 脱除天然气中的 : : |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,在溶液中能发生如下反应:①2A2++B2=2A3++2B-;②2B-+Z2=B2+2Z-;③16H++10Z-+2XO =2X2++5Z2+8H2O,由此判断下列说法错误的是
=2X2++5Z2+8H2O,由此判断下列说法错误的是
 =2X2++5Z2+8H2O,由此判断下列说法错误的是
=2X2++5Z2+8H2O,由此判断下列说法错误的是A.氧化性强到弱顺序是XO 、Z2、B2、A3+ 、Z2、B2、A3+ |
| B.向AB2溶液加入少量Z2的离子方程式为② |
| C.Z元素在②反应中被还原,在③反应中被氧化 |
| D.还原性强到弱顺序是A2+、B-、Z-、X2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】实验室制Cl2反应4HCl(浓)+MnO2  MnCl2+ Cl2↑+2H2O,下列说法不正确的是
MnCl2+ Cl2↑+2H2O,下列说法不正确的是
 MnCl2+ Cl2↑+2H2O,下列说法不正确的是
MnCl2+ Cl2↑+2H2O,下列说法不正确的是| A.还原剂是HCl,氧化剂是MnO2 |
| B.每有2molHCl被氧化,转移电子的物质的量为2mol |
| C.每消耗1mol MnO2,起还原剂作用的HCl消耗4mol |
| D.转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L |
您最近一年使用:0次
【推荐2】将0.03molFe加到过量的HNO3中,铁完全溶解,若生成NO、NO2混合气体共0.896L (标准状况)。将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体全部溶于水生成HNO3,则通入O2的体积是
| A.504mL | B.336mL | C.224mL | D.168mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某化合物结构如图所示,Z、X、M、Y为原子序数依次增大的短周期元素,X元素原子核外最外层电子数是Y元素原子核外电子数的一半。下列叙述不正确 的是


| A.X比Z更易与Y结合成相应的化合物 |
| B.元素非金属性的顺序为X>Z>Y |
| C.该化合物中各粒子均满足8电子稳定结构 |
D.Y的最高价氧化物能与 化合生成弱酸 化合生成弱酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期主族元素X、Y、Z、W 原子序数依次增大,且 X、Z 同主族,Y 为金属元素,且Y 的原子序数小于X 和 Z 的最外层电子数之和,Z 原子的最外层电子数与核外电子总数之比为 3∶8。下列说法正确的是( )
| A.原子半径:r(W)>r(Y)>r(X) |
| B.X与Y 组成的化合物中均不含共价键 |
| C.Z 的简单气态氢化物的热稳定性比W的强 |
| D.元素Y、W 形成的化合物的水溶液呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用NA表示阿伏加德罗常数,下列说法中正确的是
| A.常温常压下,1mol水中含有NA个H+和NA个OH- |
| B.在1LpH=1的硫酸溶液中,H+的个数约为0.1NA |
| C.标准状况下,17g氨中含有的共价键数目为NA |
| D.78gNa2O2与足量CO2反应,电子转移个数为2NA |
您最近一年使用:0次

 N2 + 4NH3↑+ 3SO2↑+6H2O中,当有12NA个电子转移时,以下说法正确的是
N2 + 4NH3↑+ 3SO2↑+6H2O中,当有12NA个电子转移时,以下说法正确的是

