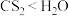“肼合成酶”以其中的Fe2+配合物为催化中心,可将NH2OH与NH3 转化为肼(NH2NH2),其反应历程如下所示。

下列说法正确的是

下列说法正确的是
| A.NH2NH2、NH3和H2O均为只含极性键的极性分子 |
B.反应涉及 、 、 键断裂和 键断裂和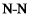 键生成 键生成 |
| C.反应过程没有元素化合价变化 |
| D.将NH2OH替换为ND2OD,反应可得ND2ND2 |
更新时间:2024-01-09 12:02:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F、G、H均为18电子分子。A和E为双原子分子,E为性质极其活泼的浅黄绿色气体;C和F为四原子分子,F的水溶液常用于医用消毒;B有臭鸡蛋气味;D与甲烷分子构型相同;G为火箭推进器常用燃料;H为烷烃。下列判断错误的是
| A.B分子中的化学键为sp3-sσ键,有轴对称性,可以旋转 |
| B.F和H中均含有极性键和非极性键,但是前者为极性分子,后者为非极性分子(不考虑空间异构) |
| C.C分子中原子序数较大的元素可形成正四面体结构的单质分子,键角为109°28ˊ |
| D.G和D中心原子杂化方式相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中,错误的是
| A.金属元素与非金属元素也可能形成共价键 |
| B.键长愈长,共价键愈牢固 |
| C.键角是两个相邻共价键之间的夹角,说明共价键有方向性 |
| D.共价键是通过原子轨道重叠并共用电子对而形成的,所以共价键有饱和性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向含HCN的废水中加入铁粉和K2CO3可制备K4[Fe(CN)6],发生反应: 6HCN+ Fe+2K2CO3=K4[Fe(CN)6]+ H2↑+2CO2↑+2H2O,下列说法正确的是
| A.HCN的VSEPR模型为四面体形 |
| B.基态碳原子和基态氮原子的未成对电子数之比为3:2 |
| C.CO2和H2O均为含有极性键的非极性分子 |
| D.HCN和CO2的中心原子C采用的杂化方式相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】第VA族元素的原子可与Cl结合形成NCl3、AsCl3、AsCl5等分子。化合价为+3的铬的卤化物有CrF3、CrCl3等,制备三氯化铬的主要反应式为Cr2O3+3CCl4 2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是
2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是
 2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是
2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是| A.[Cr(H2O)4Cl2]Cl的中心离子配位数为7 |
| B.CCl4是极性键形成的非极性分子 |
| C.CrCl3和CrF3晶体类型相同 |
| D.1mol[Cr(H2O)4Cl2]Cl和足量硝酸银溶液反应生成3molAgCl |
您最近一年使用:0次

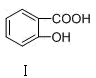 >
>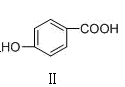

 比
比 稳定
稳定