化学电池的发明,是贮能和供能技术的巨大进步。______ (填“正极”或“负极”)。
(2)装置中锌片上发生_____ (“氧化”或“还原”)反应,写出负极发生的电极反应式______ 。
(3)电子流动的方向是________ (“Zn→Cu”或“Cu→Zn”)。
(4)上图所示装置可将_______ (写离子方程式)反应释放的能量 直接转变为电能;能证明产生电能的实验现象是________ 。
(5)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。___________ (填序号)。
①A为电池的正极 ②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
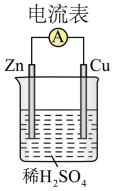
(2)装置中锌片上发生
(3)电子流动的方向是
(4)上图所示装置可将
(5)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
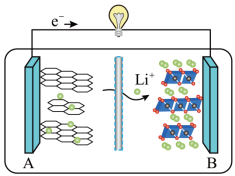
①A为电池的正极 ②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
更新时间:2024-01-06 21:24:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】分别按图甲乙所示装置进行实验,两个烧杯里的溶液为同浓度的稀硫酸,甲中A为电流表。
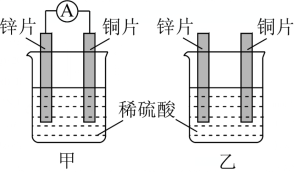
(1)下列叙述正确的是___________
A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片作正极,乙中铜片作负极
C. 两烧杯溶液中 浓度均减小
浓度均减小
D. 甲产生气泡的速率比乙慢
(2)在甲装置中,若把稀硫酸换成CuSO4溶液,一段时间后测得某一电极增重12.8g,则该电池反应共转移电子数目___________
(3)甲装置中的能量转化形式为___________ 能转化为___________ 能,乙装置中的能量转化形式为___________ 能转化为___________ 能
(4)如果将反应2FeCl3+Fe=3FeCl2设计成原电池,则正极电极反应为___________ ,正极材料是___________ ,负极材料是___________ ,电解质溶液是___________ 。

(1)下列叙述正确的是
A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片作正极,乙中铜片作负极
C. 两烧杯溶液中
 浓度均减小
浓度均减小D. 甲产生气泡的速率比乙慢
(2)在甲装置中,若把稀硫酸换成CuSO4溶液,一段时间后测得某一电极增重12.8g,则该电池反应共转移电子数目
(3)甲装置中的能量转化形式为
(4)如果将反应2FeCl3+Fe=3FeCl2设计成原电池,则正极电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电池与工农业生产、日常生活有着密切的关联。请回答下列问题:
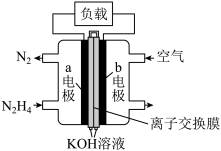
(1)燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。
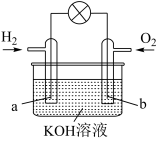
①负极是_______ (填“a”或“b”),该电极上发生_______ (填“氧化”或“还原”)反应。
②b极发生的电极反应式是_______ 。
③标准状况下,消耗11.2LH2时,转移的电子数为_______ 。
(2)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法正确的是_______(填字母)。

(3)铁及其化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:_______ 。
(1)燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①负极是
②b极发生的电极反应式是
③标准状况下,消耗11.2LH2时,转移的电子数为
(2)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法正确的是_______(填字母)。

| A.电子由铝制易拉罐经导线流向碳棒 |
| B.在碳棒上有气体生成,该气体可能为氢气 |
| C.铝质易拉罐逐渐被腐蚀,说明铝失去电子 |
| D.扬声器发声,说明该装置将电能转化为化学能 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学电池的发明,是贮能和供能技术的巨大进步。
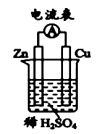
(1)如图所示装置中,Cu片是_______ (填“正极”或“负极”)。
(2)如图所示装置可将_______ (写化学方程式)反应释放的能量直接转变为电能;能证明产生电能的实验现象是_______ 、_______ 。
(3)锌在如图所示装置中的作用是传导电子、_______ 。
(4)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
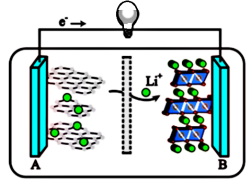
下列说法正确的是_______ (填序号)。
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动

(1)如图所示装置中,Cu片是
(2)如图所示装置可将
(3)锌在如图所示装置中的作用是传导电子、
(4)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。

下列说法正确的是
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
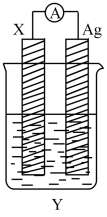
(1)电极X的材料是____ ;电解质溶液Y是____ 。
(2)X电极发生的电极反应式为____ ;Ag电极上发生的反应类型为____ 。
(3)外电路中的电子是从____ 电极流向____ 电极。Cu2+向___ (填“正极”或“负极”)移动。
(4)当Ag电极增重21.6g时,则X电极的质量减少____ 。
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O;B极:O2+4e-=2O2-。则A极是电池的____ 极;当B极参加反应的气体为112mL(标准状况),电路中转移电子的个数约为____ ,该电池的总反应为____ 。

(1)电极X的材料是
(2)X电极发生的电极反应式为
(3)外电路中的电子是从
(4)当Ag电极增重21.6g时,则X电极的质量减少
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O;B极:O2+4e-=2O2-。则A极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于___ (“离子化合物”或“共价化合物”)。
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为___________ 。
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从___________ (填“a”或“b”)通入,该电池的正极是___________ (填“M”或“N”)电极,其中在N极发生的电极反应式是___________ 。
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为___________ L。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据原电池原理,人们研制出了性能各异的化学电池。
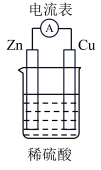
(1)如图装置中,Cu片作_______ (填“正极”或“负极”),Zn片上发生反应的电极反应式为_______ ,能证明化学能转化为电能的实验现象是_______ 。
(2)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示。其总反应为:2Mg+O2+2H2O=2Mg(OH)2。下列说法正确的是_______ (填字母)。
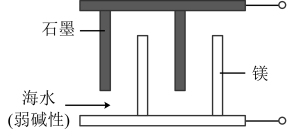
a.石墨是电池的负极 b.Mg发生氧化反应
(1)如图装置中,Cu片作

(2)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示。其总反应为:2Mg+O2+2H2O=2Mg(OH)2。下列说法正确的是

a.石墨是电池的负极 b.Mg发生氧化反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)利用反应 设计成如图甲所示原电池,回答下列问题:
设计成如图甲所示原电池,回答下列问题:
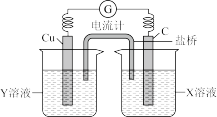
①写出电极反应式:正极________________ 。
②图中X溶液是_____ ,Y溶液是______ 。
③原电池工作时,盐桥中的___________ (填“阳”或“阴”)离子向X溶液方向移动。
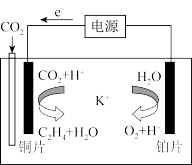
(2)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图所示,在___ (填“阳”或“阴”)极上产生乙烯的电极反应方程式为________ 。
 设计成如图甲所示原电池,回答下列问题:
设计成如图甲所示原电池,回答下列问题:
①写出电极反应式:正极
②图中X溶液是
③原电池工作时,盐桥中的
(2)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图所示,在

您最近一年使用:0次

 的性质选择合适的溶液配制方法:
的性质选择合适的溶液配制方法:

