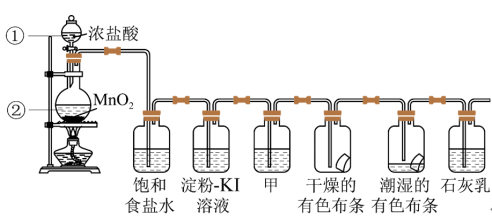
采用如下图装置制取一定量的饱和氯水,并进行氯水的性质实验。
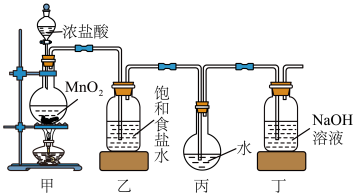
(1)写出甲装置中反应的离子方程式:________________________________________ ;该反应中氧化剂与还原剂的物质的量之比为__________ 。
(2)乙装置的作用是:________________________________________ 。
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)
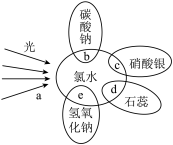
①d过程中的现象是______________________________ ;
②e过程的离子方程式______________________________ 。
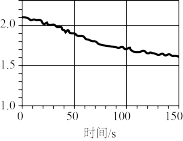
(4)数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。如图是将传感器插入盛有氯气的广口瓶中测定光照氯水过程所得到的图象,该图象表示的意义是__________(填序号)。
(5)某同学将新制的饱和氯水滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去,该同学分析红色突然褪去的原因可能有两种:
①氯水中的酸或氯气分子与 发生反应,将
发生反应,将 消耗所致;
消耗所致;
②氯水中次氯酸的强氧化性,使红色褪去所致。
设计实验证明红色褪去的原因:取褪色后的溶液于试管中,向其中滴加少量 溶液,若
溶液,若______________________________ ,则是原因①;否则是原因②。

(1)写出甲装置中反应的离子方程式:
(2)乙装置的作用是:
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)

①d过程中的现象是
②e过程的离子方程式
(4)数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。如图是将传感器插入盛有氯气的广口瓶中测定光照氯水过程所得到的图象,该图象表示的意义是__________(填序号)。

| A.氯离子浓度随时间的变化 | B.氧气体积分数随时间的变化 |
C.氯水的 随时间的变化 随时间的变化 | D.氯水导电能力随时间的变化 |
(5)某同学将新制的饱和氯水滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去,该同学分析红色突然褪去的原因可能有两种:
①氯水中的酸或氯气分子与
 发生反应,将
发生反应,将 消耗所致;
消耗所致;②氯水中次氯酸的强氧化性,使红色褪去所致。
设计实验证明红色褪去的原因:取褪色后的溶液于试管中,向其中滴加少量
 溶液,若
溶液,若
更新时间:2024-01-12 08:32:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】 为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的
为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的 与
与 反应制取,反应装置如图所示(夹持装置已略)。
反应制取,反应装置如图所示(夹持装置已略)。

已知: 熔点为
熔点为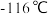 ,沸点为
,沸点为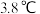 ,浓度过高或加热时易发生分解并爆炸。
,浓度过高或加热时易发生分解并爆炸。 沸点为
沸点为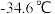 ,液氨沸点为
,液氨沸点为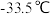 。
。
(1)写出装置A中发生反应的离子方程式:___________ 。
(2)检查虚框中装置气密性的方法为:___________ 。
(3)下列有关该实验的说法中,不正确的是___________
A.实验室也可用 与浓盐酸反应制备氯气
与浓盐酸反应制备氯气
B.B中试剂是浓硫酸,目的是干燥氯气
C.氮气的作用之一是稀释生成的 ,减少实验爆炸危险
,减少实验爆炸危险
D.从装置D中逸出气体的主要成分是
(4)①装置C中潮湿的 与
与 以等物质的量反应,生成
以等物质的量反应,生成 、气体
、气体 和另一种盐X,试写出该反应化学方程式:
和另一种盐X,试写出该反应化学方程式:___________ 。
②设计实验方案验证C中生成的产物中另一种盐X中的阴离子___________ 。
(5)该实验装置存在一处明显的不足,其改进措施为___________ 。
 为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的
为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的 与
与 反应制取,反应装置如图所示(夹持装置已略)。
反应制取,反应装置如图所示(夹持装置已略)。
已知:
 熔点为
熔点为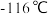 ,沸点为
,沸点为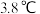 ,浓度过高或加热时易发生分解并爆炸。
,浓度过高或加热时易发生分解并爆炸。 沸点为
沸点为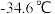 ,液氨沸点为
,液氨沸点为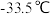 。
。(1)写出装置A中发生反应的离子方程式:
(2)检查虚框中装置气密性的方法为:
(3)下列有关该实验的说法中,不正确的是
A.实验室也可用
 与浓盐酸反应制备氯气
与浓盐酸反应制备氯气B.B中试剂是浓硫酸,目的是干燥氯气
C.氮气的作用之一是稀释生成的
 ,减少实验爆炸危险
,减少实验爆炸危险D.从装置D中逸出气体的主要成分是

(4)①装置C中潮湿的
 与
与 以等物质的量反应,生成
以等物质的量反应,生成 、气体
、气体 和另一种盐X,试写出该反应化学方程式:
和另一种盐X,试写出该反应化学方程式:②设计实验方案验证C中生成的产物中另一种盐X中的阴离子
(5)该实验装置存在一处明显的不足,其改进措施为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】磺酰氯(SO2Cl2)可用于制造锂电池正极活性物质。实验室可利用SO2和Cl2在活性炭催化下反应制取少量SO2Cl2,装置如图(部分夹持装置已省略)。
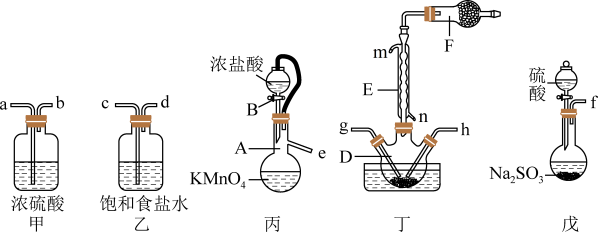
已知:①SO2(g)+Cl2(g)=SO2Cl2(l);伴随反应进行,过程中会放出热量;
②SO2Cl2熔点为-54.1℃,沸点69.1℃,常温较稳定。遇水剧烈反应,100℃以上易分解;
③装置丙中利用KMnO4与浓盐酸的反应产生出Cl2;
装置戊中反应方程式为: 。
。
④
回答下列问题:
(1)仪器E的名称是___________ ,水从___________ 口进入(选填“m”或“n”):仪器F中盛放的固体的成分可以是___________ 。
(2)装置乙的作用是___________ 。去除装置甲可能会降低SO2Cl2的产量,原因可能是___________ 。
(3)配平下列氧化还原反应方程式,并用单线桥法标出电子转移的方向和数目___________ 。

(4)装置丁中三颈烧瓶置于冷水浴中,其原因是___________ 。
(5)某实验小组利用该装置消耗了标准状况下氯气1120 mL(SO2足量),最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为___________ 。

已知:①SO2(g)+Cl2(g)=SO2Cl2(l);伴随反应进行,过程中会放出热量;
②SO2Cl2熔点为-54.1℃,沸点69.1℃,常温较稳定。遇水剧烈反应,100℃以上易分解;
③装置丙中利用KMnO4与浓盐酸的反应产生出Cl2;
装置戊中反应方程式为:
 。
。④

回答下列问题:
(1)仪器E的名称是
(2)装置乙的作用是
(3)配平下列氧化还原反应方程式,并用单线桥法标出电子转移的方向和数目

(4)装置丁中三颈烧瓶置于冷水浴中,其原因是
(5)某实验小组利用该装置消耗了标准状况下氯气1120 mL(SO2足量),最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】下图是氯气的实验室制法装置图。
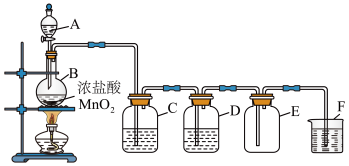
(1)写出实验室制氯气的化学方程式_______ 。
(2)C中的液体是_______ ,作用是_______ 。
(3)D中的液体是_______ ,作用是_______ 。
(4)F中液体为_______ ,写出其中发生反应的离子方程式_______ 。
(5)将生成的氯气溶于水得到的氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
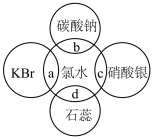
①能证明氯水具有漂白性的是_______ (填“a”“b”“c”或“d”)。
②c过程的现象是_______ ,反应的离子方程式是_______ 。

(1)写出实验室制氯气的化学方程式
(2)C中的液体是
(3)D中的液体是
(4)F中液体为
(5)将生成的氯气溶于水得到的氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

①能证明氯水具有漂白性的是
②c过程的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】1810年,英国化学家戴维以大量事实为依据,确认一种新元素组成的单质氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。

(1)仪器b的名称为_________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为_________ 。
(2)仪器a中发生反应的化学方程式为_________ 。根据氯气的性质D中的收集装置可以选择_________ (填序号)。

(3)下列有关该实验的说法中不正确的是_________ (填字母)。
A.将b中液体换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
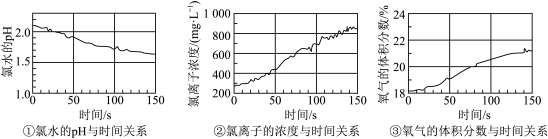
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:_________ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中不正确的是
A.将b中液体换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.X、Y、Z是中学化学常见的三种物质,它们之间的相互转化关系如下(X、Y、Z为英文字母,部分反应条件及产物略去)
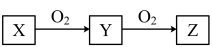
(1)若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
①则Y和新制氯水主要成分反应生成两种强酸的化学方程式___________ 。
②Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为___________ 。
(2)若Z是红棕色气体。试写出Z与水反应制备另一种强酸的化学方程式___________ 。
Ⅱ.根据所学有机化合物知识填空。
(3)下列各组物质:(填序号)
① 和
和 ②
② 和
和 ③金刚石和石墨
③金刚石和石墨
④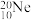 和
和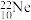 ⑤
⑤ 和丁烷 ⑥
和丁烷 ⑥ 和
和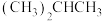
互为同分异构体的是___________ ,互为同系物的是___________ ,互为同位素的是___________ ,
互为同素异形体的是___________ ,是同一物质的是___________ 。
(4)某1mol烷烃完全燃烧需要消耗5mol氧气,写出该烷烃一氯代物的结构简式___________ 。

(1)若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
①则Y和新制氯水主要成分反应生成两种强酸的化学方程式
②Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为
(2)若Z是红棕色气体。试写出Z与水反应制备另一种强酸的化学方程式
Ⅱ.根据所学有机化合物知识填空。
(3)下列各组物质:(填序号)
①
 和
和 ②
② 和
和 ③金刚石和石墨
③金刚石和石墨④
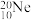 和
和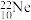 ⑤
⑤ 和丁烷 ⑥
和丁烷 ⑥ 和
和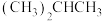
互为同分异构体的是
互为同素异形体的是
(4)某1mol烷烃完全燃烧需要消耗5mol氧气,写出该烷烃一氯代物的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组为了探究HClO的漂白性,设计了如下的实验:

(1)通入Cl2后,从集气瓶A、B的现象可得出的结论是__ ;其中发生反应的化学方程式为____ 。
(2)为了确认是HClO使湿润的红色布条褪色,你认为还应增加的实验是____ 。
(3)烧杯中NaOH溶液所起的作用是____ ,烧杯中所发生反应的化学方程式为_____ 。
(4)为保证实验安全,氯气以每分钟1.12 L(已换算为标准状况下)的流速匀速通入,若实验需耗时4 min,小烧杯中盛放2 mol·L-1的NaOH溶液的体积至少应为___ mL。

(1)通入Cl2后,从集气瓶A、B的现象可得出的结论是
(2)为了确认是HClO使湿润的红色布条褪色,你认为还应增加的实验是
(3)烧杯中NaOH溶液所起的作用是
(4)为保证实验安全,氯气以每分钟1.12 L(已换算为标准状况下)的流速匀速通入,若实验需耗时4 min,小烧杯中盛放2 mol·L-1的NaOH溶液的体积至少应为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组的同学用下图所示实验装置进行实验研究(图中a、b、c表示止水夹).请对其方案进行完善或评价;
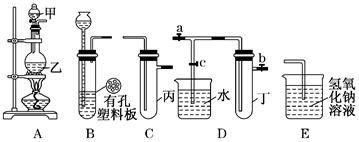
(1)实验室将B、C、E相连后,以_______ 、_________ (填写名称)为原料可制取Cl2,为接下来研究氯气的化学性质做准备。
(2) 利用实验室常用方法制取氯气,将A、C、E相连,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
请你评价:实验Ⅰ后,推出相应结论是否合理?________________ 。若不合理,请说明理由(若合理,则无需填写下行):___________________________________________ .
实验Ⅱ推出相应的结论是否合理?________________ 若不合理,请说明理由(若合理,无需填写下行):____________________________________________________ .
(3)A、C、E相连,可设计一个简单的实验,以验证Cl-和Br-的还原性强弱。有关反应的离子方程式为:____________________ ,_______________
(4)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①B中发生反应的化学方程式为___________________________
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹________ ,再打开止水夹________ ,使烧杯中的水进入试管丁的可能的操作是_______________________________ 。

(1)实验室将B、C、E相连后,以
(2) 利用实验室常用方法制取氯气,将A、C、E相连,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
请你评价:实验Ⅰ后,推出相应结论是否合理?
实验Ⅱ推出相应的结论是否合理?
(3)A、C、E相连,可设计一个简单的实验,以验证Cl-和Br-的还原性强弱。有关反应的离子方程式为:
(4)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①B中发生反应的化学方程式为
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。

(1)固体二氧化锰和浓盐酸制备氯气的化学反应方程式为:__________________ 。装置B中饱和食盐水的作用是__________________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________________ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入______ 。(填序号)
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2氧化性_________________ Br2(填>、<或=)。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是__________________________ 。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式____________________ 。

(1)固体二氧化锰和浓盐酸制备氯气的化学反应方程式为:
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式
您最近一年使用:0次