下列事实中,不能说明 属于弱碱的是
属于弱碱的是
 属于弱碱的是
属于弱碱的是A.室温下, 溶液的 溶液的 |
B. 溶液与等体积 溶液与等体积 盐酸恰好完全反应 盐酸恰好完全反应 |
C.室温下, 溶液的导电能力比相同浓度的 溶液的导电能力比相同浓度的 溶液弱 溶液弱 |
D.室温下,相同pH的 溶液与 溶液与 溶液, 溶液, 溶液的物质的量浓度更大 溶液的物质的量浓度更大 |
更新时间:2024-01-12 14:44:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列判断正确的是
①Ca(OH)2微溶于水,所以Ca(OH)2是弱电解质;②强电解质溶液的导电能力可能比弱电解质溶液导电能力弱;③液态氯化氢不导电,但它是电解质;④碳酸氢钠是弱酸的酸式盐,所以是弱电解质;⑤SO3溶于水后导电,所以SO3是电解质;⑥Cu能导电,但它不是化合物,所以Cu是非电解质
①Ca(OH)2微溶于水,所以Ca(OH)2是弱电解质;②强电解质溶液的导电能力可能比弱电解质溶液导电能力弱;③液态氯化氢不导电,但它是电解质;④碳酸氢钠是弱酸的酸式盐,所以是弱电解质;⑤SO3溶于水后导电,所以SO3是电解质;⑥Cu能导电,但它不是化合物,所以Cu是非电解质
| A.②③ | B.②③⑥ | C.①④⑤⑥ | D.②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.硫酸的导电能力比盐酸溶液强 |
| B.氨气溶于水能导电,所以氨气是电解质 |
| C.NaCl溶液在电流作用下电离成Na+与Cl- |
| D.氯化氢溶于水能导电,但液态氯化氢不导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,将1L0.3mol⋅ L−1HA溶液与0.1molNaOH固体混合,使之充分反应得到溶液(a)。然后向该溶液中通入HCl或加入NaOH固体(忽略体积和温度变化),溶液pH随通(加)入物质的量的变化如图。下列叙述错误的是
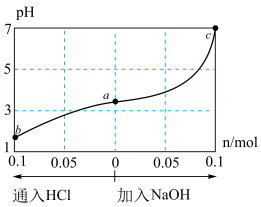

| A.HA是一种弱酸 |
| B.向a点对应溶液中通入HCl,充分反应后,c(H+)/c(HA)增大 |
| C.b点对应溶液中:c(Na+)=c(Cl-)>c(HA)>c(H+)>c(OH-) |
| D.c点对应溶液中:c(Na+)=c(A-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知25℃时,lgKa(CH3COOH)=lgKb(NH3·H2O)=-4.75。下列说法正确的是
| A.0.1 mol·L-1 CH3COONH4溶液中:c(CH3COO-)=c(NH4+)=c(H+)=c(OH-) |
| B.0.1 mol·L-1 氨水与0.1 mol·L-1 NH4Cl溶液等体积混合:c(NH4+)+c(NH3·H2O)=2c(Cl-) |
| C.0.1 mol·L-1 CH3COONa溶液与0.1 mol·L-1 CH3COOH溶液等体积混合:c(CH3COOH)>c(Na+)>c(CH3COO-) |
D.CH3COOH+NH3·H2O CH3COO-+NH4++H2O的平衡常数为K,则lgK=9.5 CH3COO-+NH4++H2O的平衡常数为K,则lgK=9.5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】相同温度下,根据三种酸的电离平衡常数,下列判断正确的是
| 酸 | HX | HY | HZ |
| 电离平衡常数 | 9×10-7 | 9×10-6 | 1×10-2 |
| A.从电离平衡常数可以判断,HX 和 HY 属于弱酸,HZ 属于强酸 |
| B.三种酸的强弱关系:HX> HY > HZ |
| C.反应 X- + HZ = Z-+ HX 能够发生 |
| D.相同温度下,0.1 mol/L HY 溶液的电离平衡常数大于 0.01 mol/L HY 溶液的电离平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,pH均为2的两种溶液:①醋酸溶液,②盐酸。下列说法错误的是
| A.两溶液中水电离出的c(H+):①=② |
| B.两溶液分别加水稀释10倍,稀释后溶液的pH:②>① |
| C.取大小和形状完全相同的两块锌粒分别投入两种酸中,当产生相同体积的气体时所需的时间:①>② |
| D.等体积的两溶液分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积:①>② |
您最近一年使用:0次

 表示水分子),下列说法错误的是
表示水分子),下列说法错误的是
 在水溶液中的导电情况
在水溶液中的导电情况 +
+
 的氨水和氢氧化钠溶液加水稀释时的
的氨水和氢氧化钠溶液加水稀释时的
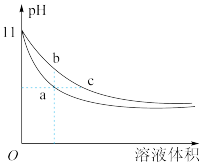
 点导电能力比
点导电能力比 点强
点强 值大于
值大于 点
点
 相等
相等

