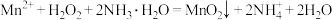工业生产中除去电石渣浆(含 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是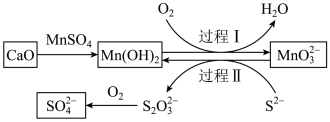
A.碱性条件下,氧化性: |
B.过程Ⅱ中,反应的离子方程式为 |
C.将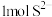 转化为 转化为 理论上需要 理论上需要 的体积为 的体积为 (标准状况) (标准状况) |
| D.该过程中涉及的化学反应均是氧化还原反应 |
更新时间:2024-01-14 23:17:23
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列化学反应的离子方程式正确的是
| A.0.01mol/L NH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合产生沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O |
| B.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ |
C.NH4HCO3溶液与过量NaOH溶液共热:NH4++OH- NH3↑+H2O NH3↑+H2O |
D.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+  Fe3++3NO2↑+3H2O Fe3++3NO2↑+3H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列离子方程式正确的是
A.氯气和水反应:Cl2+H2O Cl-+ClO-+2H+ Cl-+ClO-+2H+ |
B.硫酸铵溶液和氢氧化钡溶液反应:Ba2++ == BaSO4↓ == BaSO4↓ |
| C.酸性硫酸亚铁溶液在空气中被氧化:4Fe2++O2+4H+==4Fe3++2H2O |
D.碳酸氢钠溶液和过量的澄清石灰水混合:2 +Ca2++2OH- ==CaCO3↓+ +Ca2++2OH- ==CaCO3↓+ +2H2O +2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.01 mol的混合溶液中加入0.01 mol铁粉,经搅拌后发生的变化应是( )
| A.铁溶解,析出0.01 mol Ag和0.005 mol Cu |
| B.铁溶解,析出0.01 mol Ag并放出H2 |
| C.铁溶解,析出0.01 mol Ag,溶液中不再有Fe3+ |
| D.铁溶解,析出0.01 mol Ag,溶液中不再有Cu2+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为3:1,则Cl2与KOH反应时,被还原的氯元素和被氧化的氯元素的质量之比为()
| A.1 : 3 | B.4 : 3 | C.2 : 1 | D.3 : 1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水反应的化学方程式是:4K2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8KOH,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾。制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是
湿法制备:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是
| A.高铁酸钾处理水时,水发生氧化反应 |
| B.湿法中每生成1mol Na2FeO4共转移3mol电子 |
| C.干法中每生成1mol Na2FeO4共转移4mol电子 |
| D.K2FeO4处理水时,不仅能杀菌,并能使悬浮杂质沉降 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某电镀污泥含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量金等,某小组设计如下资源综合利用的方案:

已知:碲和硫位于同主族,煅烧时Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2,滤渣中TeO2溶于稀硫酸发生的反应为TeO2+H2SO4====TeOSO4+H2O。
2CuO+TeO2,滤渣中TeO2溶于稀硫酸发生的反应为TeO2+H2SO4====TeOSO4+H2O。
下列说法错误的是

已知:碲和硫位于同主族,煅烧时Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2,滤渣中TeO2溶于稀硫酸发生的反应为TeO2+H2SO4====TeOSO4+H2O。
2CuO+TeO2,滤渣中TeO2溶于稀硫酸发生的反应为TeO2+H2SO4====TeOSO4+H2O。下列说法错误的是
| A.“高温煅烧”电镀污泥时铜、碲和铬元素都被氧化 |
| B.“酸化”时可向溶液中加入硫酸 |
| C.“固体1”的主要成分为Cu |
| D.“滤液3”可以循环利用 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】雌黄 和雄黄
和雄黄 都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是
都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是

 和雄黄
和雄黄 都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是
都是自然界中常见的难溶砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也可用来入药。砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示(雌黄和雄黄中S元素的价态相同)。下列说法正确的是
| A.反应Ⅰ、Ⅱ、Ⅲ、Ⅳ均为氧化还原反应 |
B.反应Ⅱ中,若物质a为 ,当 ,当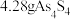 参与反应时转移 参与反应时转移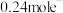 |
| C.反应过程中的尾气用硫酸铜溶液吸收 |
D.反应Ⅰ的离子方程式为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】以下工业流程制备无机功能材料MnO2,粗MnO2的提纯是工业生产的重要环节,某研究性学习小组设计了将粗MnO2(含有较多MnO和MnCO3)样品转化为纯MnO2实验。

针对上述工业流程,下列选项错误的是( )

针对上述工业流程,下列选项错误的是( )
A.第①步加稀 时,粗MnO2样品中的MnO、MnCO3转化为可溶性物质 时,粗MnO2样品中的MnO、MnCO3转化为可溶性物质 |
B.不考虑操作过程中的损失,本流程中的 固体能全部循环,不需额外补充 固体能全部循环,不需额外补充 |
C.第②步反应的离子方程式 |
| D.实验室模拟上述工业流程中得到MnO2固体的操作必须用到的玻璃仪器有玻璃棒、烧杯、漏斗 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】用久置于空气中的生石灰[主要成分为 ,还含有
,还含有 和
和 ]制取
]制取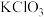 的流程如下图所示。已知,“转化”时发生的化学反应方程式为:
的流程如下图所示。已知,“转化”时发生的化学反应方程式为: ,下列说法不正确的是
,下列说法不正确的是

 ,还含有
,还含有 和
和 ]制取
]制取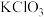 的流程如下图所示。已知,“转化”时发生的化学反应方程式为:
的流程如下图所示。已知,“转化”时发生的化学反应方程式为: ,下列说法不正确的是
,下列说法不正确的是
| A.“打浆”有利于后续“氯化”反应的加速进行 |
B.“过滤”后的滤渣中含有 |
C.由“转化”反应可知,相同条件下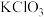 的溶解度小于 的溶解度小于 |
| D.该流程中所有反应均为非氧化还原反应 |
您最近一年使用:0次

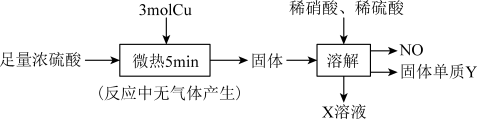
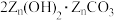 是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量
是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量 、
、 等离子)为原料制备
等离子)为原料制备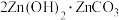 的工艺流程如图,下列说法不正确的是
的工艺流程如图,下列说法不正确的是
 ,
, 的混合溶液呈中性时,
的混合溶液呈中性时,
 的离子方程式为:
的离子方程式为: