含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为_______。
(2)我国从2000年起逐步用ClO2气体替代氯气进行消毒,实验室常用KClO3、草酸(H2C2O4)和稀硫酸制备ClO2,草酸被氧化成CO2,则该反应的离子方程式为_______ 。
(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质:NaClO2、ClO2、H2O2、NaOH、H2O、 ,写出反应的化学方程式:
,写出反应的化学方程式:_______ 。
(4)请完成该过程的化学方程式并配平_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
若反应生成71g Cl2,被氧化的HCl的物质的量为_______ 。
(5)实验室用下列方法均可制取氯气
①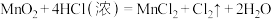
②
③
④
若各反应转移的电子数相同,①②③④生成的氯气的物质的量之比为_______ 。
(1)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为_______。
| A.NaCl、Cl2 | B.NaCl、NaClO |
| C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质:NaClO2、ClO2、H2O2、NaOH、H2O、
 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)请完成该过程的化学方程式并配平
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______若反应生成71g Cl2,被氧化的HCl的物质的量为
(5)实验室用下列方法均可制取氯气
①
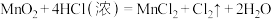
②

③

④

若各反应转移的电子数相同,①②③④生成的氯气的物质的量之比为
更新时间:2024-01-16 10:03:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应与离子反应在生产生活与科学实验中有重要作用,回答下列问题。
I、过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。根据下列反应回答问题:
A.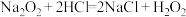
B.
C.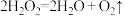
D.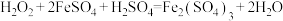
(1)上述反应中, 仅体现氧化性的反应是
仅体现氧化性的反应是___________ (填字母,下同), 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是___________ , 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是___________ 。
(2)在酸性条件下发生反应, 溶液可被
溶液可被 还原为
还原为 ,请写出这个离子反应方程式
,请写出这个离子反应方程式___________ 。
II、有一包固体粉末,其中可能含有NaCl、 、
、 、
、 中的一种或几种,现做以下实验:
中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③另取①中过滤后的滤液加入足量 溶液,产生白色沉淀。
溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(3)原固体粉末中一定不含有的物质是___________ (写化学式,下同),可能含有的物质是___________ 。
I、过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。根据下列反应回答问题:
A.
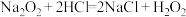
B.

C.
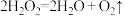
D.
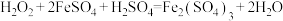
(1)上述反应中,
 仅体现氧化性的反应是
仅体现氧化性的反应是 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是(2)在酸性条件下发生反应,
 溶液可被
溶液可被 还原为
还原为 ,请写出这个离子反应方程式
,请写出这个离子反应方程式II、有一包固体粉末,其中可能含有NaCl、
 、
、 、
、 中的一种或几种,现做以下实验:
中的一种或几种,现做以下实验:①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③另取①中过滤后的滤液加入足量
 溶液,产生白色沉淀。
溶液,产生白色沉淀。根据上述实验事实,回答下列问题:
(3)原固体粉末中一定不含有的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】①HCl、②过氧化钠、③碳酸氢钠、④二氧化硅是常见的物质。请回答下列问题。
(1)上述4种物质中属于盐的是_________ (填序号,下同);上述四种物质加入紫色石蕊溶液中,溶液变红的是___________ 。
(2)写出HCl的电离方程式_____________________________ 。
(3)写出过氧化钠与水反应的化学方程式___________________________ 。
(4)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为______________ 。
(5)写出二氧化硅与氢氧化钠溶液反应的化学方程式_______________________ 。
(1)上述4种物质中属于盐的是
(2)写出HCl的电离方程式
(3)写出过氧化钠与水反应的化学方程式
(4)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
(5)写出二氧化硅与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.现有以下物质:①石墨;②乙醇;③氨水;④二氧化碳;⑤碳酸钠固体;⑥氢氧化钡溶液;⑦纯醋酸;⑧氯化氢气体。(填序号)
(1)其中能导电的是_______ ;属于非电解质的是_______ ;属于电解质的是_______ 。
II.某100mL溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知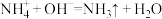 ,气体全部逸出)。
,气体全部逸出)。
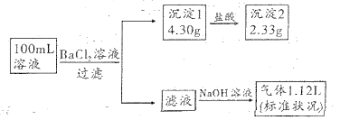
(2)原溶液中一定含有_______ 离子,可能含有_______ 离子。
(3)实验中生成硫酸钡的离子方程式为_______ 。
(4)原溶液中 的物质的量浓度范围是
的物质的量浓度范围是_______ 。
(5)对可能存在的离子用什么方法检验_______ 。
(1)其中能导电的是
II.某100mL溶液可能含有
 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知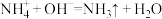 ,气体全部逸出)。
,气体全部逸出)。
(2)原溶液中一定含有
(3)实验中生成硫酸钡的离子方程式为
(4)原溶液中
 的物质的量浓度范围是
的物质的量浓度范围是(5)对可能存在的离子用什么方法检验
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中;
(1)_______________ 是氧化剂,___________ 是氧化产物。(均填写化学式)
(2)请用双线桥(或单线桥)法标出电子转移方向和数目_______
3Cu+8HNO3(稀)===3Cu(NO3)2 +2NO↑+4H2O
(3)若产生的气体在标准状况下的体积为44.8L,则反应中电子转移了_______ mol。
(1)
(2)请用双线桥(或单线桥)法标出电子转移方向和数目
3Cu+8HNO3(稀)===3Cu(NO3)2 +2NO↑+4H2O
(3)若产生的气体在标准状况下的体积为44.8L,则反应中电子转移了
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】实验室常用高锰酸钾固体与浓盐酸在常温下反应来快速制备少量 。反应方程式为:
。反应方程式为:
(1)用双线桥标出该反应中电子转移方向和数目________ 。
(2)氧化剂与还原剂的物质的量比是________ ;在标况下,若生成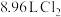 ,则转移的电子数为
,则转移的电子数为________  。
。
 。反应方程式为:
。反应方程式为:
(1)用双线桥标出该反应中电子转移方向和数目
(2)氧化剂与还原剂的物质的量比是
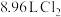 ,则转移的电子数为
,则转移的电子数为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.回答下列问题:
(1)实验室中化学药品保存方法是由药品本身性质决定的,下列试剂保存方法不正确的是_______ 。
a.浓硝酸见光受热易分解,用棕色试剂瓶保存
b.浓硫酸、氢氧化钠溶液、碳酸钠溶液都不可以用带有玻璃塞的试剂瓶保存
c.硫酸亚铁溶液易被空气氧化,保存时常加入铁粉
d.液溴有挥发性,保存时应水封
Ⅱ.氮、磷元素存在于人体所有细胞中,几乎参与所有生理上的化学反应。磷元素有多种含氧酸,除了常见的磷酸 为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。
为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。
(2)次磷酸 可由
可由 与碘水反应制备,其化学反应方程式为
与碘水反应制备,其化学反应方程式为____ ; 和
和 比较,热稳定性较强的是
比较,热稳定性较强的是_______ 。
(3) 与过量
与过量 溶液反应生成的盐为
溶液反应生成的盐为 ,该盐属于
,该盐属于_____ (选填“酸式”、“正”)盐。
(4)由同主族元素性质的相似性可知, 属于
属于_______ (选填“离子”、“共价”)化合物, 含有的化学键类型为
含有的化学键类型为_______ 。
(1)实验室中化学药品保存方法是由药品本身性质决定的,下列试剂保存方法不正确的是
a.浓硝酸见光受热易分解,用棕色试剂瓶保存
b.浓硫酸、氢氧化钠溶液、碳酸钠溶液都不可以用带有玻璃塞的试剂瓶保存
c.硫酸亚铁溶液易被空气氧化,保存时常加入铁粉
d.液溴有挥发性,保存时应水封
Ⅱ.氮、磷元素存在于人体所有细胞中,几乎参与所有生理上的化学反应。磷元素有多种含氧酸,除了常见的磷酸
 为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。
为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。(2)次磷酸
 可由
可由 与碘水反应制备,其化学反应方程式为
与碘水反应制备,其化学反应方程式为 和
和 比较,热稳定性较强的是
比较,热稳定性较强的是(3)
 与过量
与过量 溶液反应生成的盐为
溶液反应生成的盐为 ,该盐属于
,该盐属于(4)由同主族元素性质的相似性可知,
 属于
属于 含有的化学键类型为
含有的化学键类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据题目信息,完成有关方程式的书写。
(1)制备氢氧化铁胶体的离子方程式为_______ 。
(2) 与石灰乳反应的化学方程式:
与石灰乳反应的化学方程式:_______ 。
(3)用单线桥分析 与水反应中电子转移的方向和数目:
与水反应中电子转移的方向和数目:_______ 。
(4)将 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。写出该反应的离子方程式:
无色)。写出该反应的离子方程式:_______ 。
(1)制备氢氧化铁胶体的离子方程式为
(2)
 与石灰乳反应的化学方程式:
与石灰乳反应的化学方程式:(3)用单线桥分析
 与水反应中电子转移的方向和数目:
与水反应中电子转移的方向和数目:(4)将
 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。写出该反应的离子方程式:
无色)。写出该反应的离子方程式:
您最近一年使用:0次
【推荐3】回答下列问题:
(1)已知乙醇能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O。Cr2O 和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
①写出Cr2(SO4)3的电离方程式:___ 。
②该反应___ (填“是”或“不是”)氧化还原反应,判断的依据是___ 。
③这一反应可用来检测司机是否酒后驾,简述其原理:___ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是___ ;若反应中转移了0.3mol电子,则氧化产物的质量是___ g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱顺序为___ 。足量Cl2通入FeBr2溶液中发生反应的离子方程式为___ 。
(1)已知乙醇能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O。Cr2O
 和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+在溶液中分别显橙色和绿色,回答下列问题:①写出Cr2(SO4)3的电离方程式:
②该反应
③这一反应可用来检测司机是否酒后驾,简述其原理:
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱顺序为
您最近一年使用:0次

 在催化剂、加热条件下消除污染。反应为:
在催化剂、加热条件下消除污染。反应为: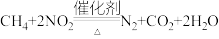
 ,则消耗
,则消耗

