I.回答下列问题:
(1)实验室中化学药品保存方法是由药品本身性质决定的,下列试剂保存方法不正确的是_______ 。
a.浓硝酸见光受热易分解,用棕色试剂瓶保存
b.浓硫酸、氢氧化钠溶液、碳酸钠溶液都不可以用带有玻璃塞的试剂瓶保存
c.硫酸亚铁溶液易被空气氧化,保存时常加入铁粉
d.液溴有挥发性,保存时应水封
Ⅱ.氮、磷元素存在于人体所有细胞中,几乎参与所有生理上的化学反应。磷元素有多种含氧酸,除了常见的磷酸 为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。
为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。
(2)次磷酸 可由
可由 与碘水反应制备,其化学反应方程式为
与碘水反应制备,其化学反应方程式为____ ; 和
和 比较,热稳定性较强的是
比较,热稳定性较强的是_______ 。
(3) 与过量
与过量 溶液反应生成的盐为
溶液反应生成的盐为 ,该盐属于
,该盐属于_____ (选填“酸式”、“正”)盐。
(4)由同主族元素性质的相似性可知, 属于
属于_______ (选填“离子”、“共价”)化合物, 含有的化学键类型为
含有的化学键类型为_______ 。
(1)实验室中化学药品保存方法是由药品本身性质决定的,下列试剂保存方法不正确的是
a.浓硝酸见光受热易分解,用棕色试剂瓶保存
b.浓硫酸、氢氧化钠溶液、碳酸钠溶液都不可以用带有玻璃塞的试剂瓶保存
c.硫酸亚铁溶液易被空气氧化,保存时常加入铁粉
d.液溴有挥发性,保存时应水封
Ⅱ.氮、磷元素存在于人体所有细胞中,几乎参与所有生理上的化学反应。磷元素有多种含氧酸,除了常见的磷酸
 为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。
为三元中强酸外,还有次磷酸等弱酸,结合已学知识回答下列问题。(2)次磷酸
 可由
可由 与碘水反应制备,其化学反应方程式为
与碘水反应制备,其化学反应方程式为 和
和 比较,热稳定性较强的是
比较,热稳定性较强的是(3)
 与过量
与过量 溶液反应生成的盐为
溶液反应生成的盐为 ,该盐属于
,该盐属于(4)由同主族元素性质的相似性可知,
 属于
属于 含有的化学键类型为
含有的化学键类型为
更新时间:2024-04-11 18:01:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)===KCl+MnCl2+Cl2↑+H2O(未配平)
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目_________ 。
(2)在该反应中,如有1molCl2生成,被氧化的HCl的物质的量是_______ ,转移电子的数目是________ 。
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是________ 。
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是________ (用离子方程式表示)。
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目
(2)在该反应中,如有1molCl2生成,被氧化的HCl的物质的量是
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与
 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:将SO2通入FeCl3溶液中,溶液颜色会变为浅绿色,其原理可表示为:
□Fe3++ □SO2+ □H2O —— □Fe2++ □SO42-+ □H+
(1)在上述方框内填上配平后的系数,并用单线桥法标出电子转移的方向和数目_____ 。
(2)若参加反应的SO2体积为1.12 L(标准状况下),则反应中转移电子的物质的量为______ mol;
(3)已知向Fe2+溶液中滴加少量硝酸时,溶液由浅绿色变为黄色。则Fe3+、SO42-、HNO3的氧化性由强到弱的顺序为________________________ 。
□Fe3++ □SO2+ □H2O —— □Fe2++ □SO42-+ □H+
(1)在上述方框内填上配平后的系数,并用单线桥法标出电子转移的方向和数目
(2)若参加反应的SO2体积为1.12 L(标准状况下),则反应中转移电子的物质的量为
(3)已知向Fe2+溶液中滴加少量硝酸时,溶液由浅绿色变为黄色。则Fe3+、SO42-、HNO3的氧化性由强到弱的顺序为
您最近半年使用:0次
【推荐3】H、C、N、O、Na、Cr是常见的六种元素。
(1)C位于元素周期表第____ 周期第___ 族;Cr的基态原子核外电子排布式为___________ ;C2H2分子中σ键与π键数目之比为____________ 。
(2)用“>”或“<”填空:
(3)25℃、101kPa下:①2Na(s)+1/2O2(g)=Na2O(s) ΔH=-414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ·mol-1
写出Na2O2与单质钠化合成Na2O固体的热化学方程式_________________________ 。
(4)我国已经立法规定酒驾入刑。“酒精检测仪”中有红色CrO3和少量H2SO4,检测酒驾时产物有三价铬和CO2等,该反应的化学方程式为______________________________________ 。
(1)C位于元素周期表第
(2)用“>”或“<”填空:
| 电负性 | 键长 | 键的极性 | 沸点(同压) |
| C | C=C | N-H | 甲醇 |
②2Na(s)+O2(g)=Na2O2(s) ΔH=-511kJ·mol-1
写出Na2O2与单质钠化合成Na2O固体的热化学方程式
(4)我国已经立法规定酒驾入刑。“酒精检测仪”中有红色CrO3和少量H2SO4,检测酒驾时产物有三价铬和CO2等,该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答:
(1)石英砂主要成分的化学式是_______ ;氯化钙中含有化学键的类型是_______ 。
(2)在 溶液中加入
溶液中加入 溶液时观察到的现象是
溶液时观察到的现象是_______ 。
(3)浓硝酸见光或者受热发生分解的化学方程式是_______ 。
(1)石英砂主要成分的化学式是
(2)在
 溶液中加入
溶液中加入 溶液时观察到的现象是
溶液时观察到的现象是(3)浓硝酸见光或者受热发生分解的化学方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫酸工业在国民经济中占有重要地位。
(1)在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾( )为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为
)为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为___________ (填化学式)。该方法中“煅烧”反应方程式为:___________ (补全反应化学方程式)。
 ___________
___________
(2)“铅室法”[使用了大容积铅室制备硫酸(76%以下)]与“塔士法”制硫酸的主要反应有:
___________ ___________
___________ ___________+___________
___________+___________
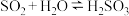
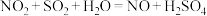


副反应: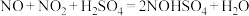
①补全反应化学方程式___________ 。
___________ ___________
___________ ___________+___________
___________+___________
② 在上述过程中作用为
在上述过程中作用为___________ 。
③上述方法生产硫酸的总反应为___________ 。
④为了适应化工生产的需求 “铅室法”、“塔式法”最终被接触法所代替,其主要原因是___________ (答出一点即可)。
(3)有关接触法制硫酸的叙述,其中错误的是___________。
(1)在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾(
 )为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为
)为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为 ___________
___________(2)“铅室法”[使用了大容积铅室制备硫酸(76%以下)]与“塔士法”制硫酸的主要反应有:
___________
 ___________
___________ ___________+___________
___________+___________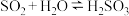
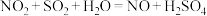


副反应:
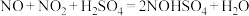
①补全反应化学方程式
___________
 ___________
___________ ___________+___________
___________+___________②
 在上述过程中作用为
在上述过程中作用为③上述方法生产硫酸的总反应为
④为了适应化工生产的需求 “铅室法”、“塔式法”最终被接触法所代替,其主要原因是
(3)有关接触法制硫酸的叙述,其中错误的是___________。
| A.用硫黄或含硫矿石均可作为原料 |
| B.尾气含有二氧化硫,在排入大气前需进行净化处理 |
| C.硫酸生产中涉及的化学反应全部是氧化还原反应 |
| D.硫酸生产中涉及的化学反应都需要使用催化剂 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】在盛有一定量浓硝酸的试管中加入6.4 g铜片发生反应。请回答:
(1)开始阶段,观察到的现象为铜片逐渐溶解,溶液由无色变为_______ 色,产生_______ 色的气体,反应的化学方程式是_______ 。
(2)反应结束后,铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式是_______ 。
(3)若6.4 g铜片消耗完时共产生气体2.8 L(标准状况)。则消耗硝酸的物质的量是_______ 。
(4)实验室中硝酸通常保存在棕色试剂瓶中,原因是_______ (用化学方程式表示)。
(5)工业上通常用氨催化氧化法制硝酸,写出氨催化氧化的化学方程式:_______ 。
(1)开始阶段,观察到的现象为铜片逐渐溶解,溶液由无色变为
(2)反应结束后,铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式是
(3)若6.4 g铜片消耗完时共产生气体2.8 L(标准状况)。则消耗硝酸的物质的量是
(4)实验室中硝酸通常保存在棕色试剂瓶中,原因是
(5)工业上通常用氨催化氧化法制硝酸,写出氨催化氧化的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是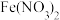 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______________ 。
(2)实验室配制 溶液时,如果没有隔绝空气,
溶液时,如果没有隔绝空气, 会被氧化为
会被氧化为________ (填写化学式)。在该溶液中加入________ 试剂,看到_________ 现象,证明溶液变质。写出检验 已经被氧化的离子方程式
已经被氧化的离子方程式_________ 。
(3)已知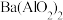 可溶于水,下图表示的是向
可溶于水,下图表示的是向 溶液中逐滴加入
溶液中逐滴加入 溶液时,生成沉淀的物质的量y与加入
溶液时,生成沉淀的物质的量y与加入 的物质的量x的关系。
的物质的量x的关系。

由图可知c点的沉淀是______ (填化学式),a-b过程中沉淀物质的量较大的是____ (填化学式),写出从开始滴加入 溶液至c点的总反应离子方程式
溶液至c点的总反应离子方程式_______ 。
(1)过量的铁和稀硝酸发生反应,产物是
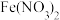 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)实验室配制
 溶液时,如果没有隔绝空气,
溶液时,如果没有隔绝空气, 会被氧化为
会被氧化为 已经被氧化的离子方程式
已经被氧化的离子方程式(3)已知
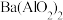 可溶于水,下图表示的是向
可溶于水,下图表示的是向 溶液中逐滴加入
溶液中逐滴加入 溶液时,生成沉淀的物质的量y与加入
溶液时,生成沉淀的物质的量y与加入 的物质的量x的关系。
的物质的量x的关系。
由图可知c点的沉淀是
 溶液至c点的总反应离子方程式
溶液至c点的总反应离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】混合物的除杂
| 混合物(括号内为杂质) | 除杂方法及试剂 |
| Fe2+(Fe3+) | ① |
| FeCl3溶液(FeCl2溶液) | ② |
| Fe2+(Cu2+) | ③ |
| Fe(Al) | ④ |
| Fe2O3(Al 2O3) | ⑤ |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求写出反应方程式:
(1)写出硫酸氢铵在水中的电离方程式:______ 。
(2)写出金属钠与硫酸铜溶液反应的离子方程式:______ 。
(3)过氧化钠可作为供氧剂吸收二氧化碳,请写出化学方程式,并用双线桥法 标出电子转移的方向和数目:______ 。
(4)漂白粉在空气中会逐渐吸收CO2变质生成碳酸钙,请写出化学方程式:______ 。
(5) FeSO4溶液能够使酸性KMnO4溶液褪色,请写出反应的离子方程式:______ 。
(1)写出硫酸氢铵在水中的电离方程式:
(2)写出金属钠与硫酸铜溶液反应的离子方程式:
(3)过氧化钠可作为供氧剂吸收二氧化碳,请写出化学方程式,并用
(4)漂白粉在空气中会逐渐吸收CO2变质生成碳酸钙,请写出化学方程式:
(5) FeSO4溶液能够使酸性KMnO4溶液褪色,请写出反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)写出下列物质的电子式:NH4Cl___________ ,N2___________ ,Mg(OH)2___________ 。
(2)用电子式表示出下列化合物形成过程:Na2O___________ ,CO2___________ 。
(3)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是___________ ;只含有共价键的是___________ ;既含有离子键又含有共价键的是___________ ;含有非极性共价键的化合物是___________ ;不含化学键的是___________ 。
(4)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是___________ (填序号,下同),属于电解质的是___________ ,上述条件下能导电的是___________ 。
(2)用电子式表示出下列化合物形成过程:Na2O
(3)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是
(4)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用序号按要求回答下列问题:
(1)下列各组微粒: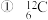 与
与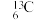
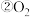 和
和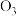
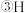 、D、
、D、 金刚石和石墨
金刚石和石墨 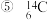 和
和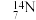 ,互为同位素的是
,互为同位素的是_________ ;互为同素异形体的是________ ;质量数相等,但不能互称为同位素的是 ______ 。
(2)下列各种物质:
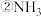
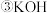 ④Na2O2 ⑤MgCl2
④Na2O2 ⑤MgCl2 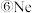 ,不存在化学键的是
,不存在化学键的是______ ;只存在离子键的是______ ;属于共价化合物的是________ ;含非极性键的离子化合物是 _________ 。
(3)下列变化过程: 碘的升华
碘的升华  NaCl固体溶于水
NaCl固体溶于水  O2溶于水
O2溶于水  HCl气体溶于水
HCl气体溶于水 烧碱熔化
烧碱熔化  氯化铵受热分解,化学键没有被破坏的是
氯化铵受热分解,化学键没有被破坏的是__________ ; 仅破坏离子键的是__________ ;仅破坏共价键的是__________ 。
(1)下列各组微粒:
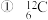 与
与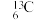
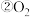 和
和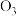
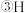 、D、
、D、 金刚石和石墨
金刚石和石墨 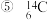 和
和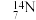 ,互为同位素的是
,互为同位素的是(2)下列各种物质:

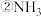
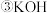 ④Na2O2 ⑤MgCl2
④Na2O2 ⑤MgCl2 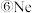 ,不存在化学键的是
,不存在化学键的是(3)下列变化过程:
 碘的升华
碘的升华  NaCl固体溶于水
NaCl固体溶于水  O2溶于水
O2溶于水  HCl气体溶于水
HCl气体溶于水 烧碱熔化
烧碱熔化  氯化铵受热分解,化学键没有被破坏的是
氯化铵受热分解,化学键没有被破坏的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.根据下列6种符号回答问题:
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)互为同位素的是____________ 。(填序号,下同)
(2)质量数相等的是______________ ,中子数相等的是_________ 。
Ⅱ.现有6种物质: ①MgCl2②HCl ③SO2 ④ K2CO3⑤ CaO ⑥ NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是_____________ 。
(2)只含离子键的化合物是_________ 。
(3)含共价键的离子化合物是______ 。
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)互为同位素的是
(2)质量数相等的是
Ⅱ.现有6种物质: ①MgCl2②HCl ③SO2 ④ K2CO3⑤ CaO ⑥ NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是
(2)只含离子键的化合物是
(3)含共价键的离子化合物是
您最近半年使用:0次



