实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)===KCl+MnCl2+Cl2↑+H2O(未配平)
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目_________ 。
(2)在该反应中,如有1molCl2生成,被氧化的HCl的物质的量是_______ ,转移电子的数目是________ 。
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是________ 。
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是________ (用离子方程式表示)。
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目
(2)在该反应中,如有1molCl2生成,被氧化的HCl的物质的量是
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与
 物质的量之比为1∶1的混合液,反应的化学方程式是
物质的量之比为1∶1的混合液,反应的化学方程式是(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是
更新时间:2020-09-26 11:38:01
|
相似题推荐
【推荐1】I.储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。请回答下列问题:
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目___________ 。
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。
(2)上述反应中氧化剂是___________ ,被氧化的元素是___________ (填元素符号) 。
(3)H2SO4在上述反应中表现出来的性质是___________(填标号)。
(4)请配平下列离子方程式___________ 。
___________Fe2++___________H++___________ =___________Fe3++___________N2O↑+___________H2O
=___________Fe3++___________N2O↑+___________H2O
II.已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO;②N2O3;③N2O4;④HNO3;⑤NH3;⑥N2O中:
(5)氮元素只能作还原剂的是___________ (填序号,下同)。
(6)可能是HNO2还原产物的是___________ 。
(7)不可能是N2的氧化产物是___________ 。
(8)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________ 。
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。
(2)上述反应中氧化剂是
(3)H2SO4在上述反应中表现出来的性质是___________(填标号)。
| A.酸性 | B.氧化性 | C.氧化性和酸性 | D.还原性和酸性 |
___________Fe2++___________H++___________
 =___________Fe3++___________N2O↑+___________H2O
=___________Fe3++___________N2O↑+___________H2OII.已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO;②N2O3;③N2O4;④HNO3;⑤NH3;⑥N2O中:
(5)氮元素只能作还原剂的是
(6)可能是HNO2还原产物的是
(7)不可能是N2的氧化产物是
(8)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)在 、
、 、
、 、
、 、S微粒中只有氧化性的是
、S微粒中只有氧化性的是_______ ;既有氧化性又有还原性的是_______ 。
(2)在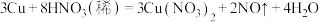 反应中:
反应中:
①_______ 是还原剂,_______ 是还原产物。(填写化学式)
②用单线桥法标出该反应电子转移的方向和数目:_______
③反应中稀硝酸表现出的性质是_______ 。(填写字母)
a.还原性 b.酸性 c.氧化性。
(3)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 ;已知该反应中
;已知该反应中 只发生如下过程:
只发生如下过程: 。
。
①该反应中,发生还原反应的过程是_______ →_______ 。
②写出该反应的化学方程式:_______ 。
(1)在
 、
、 、
、 、
、 、S微粒中只有氧化性的是
、S微粒中只有氧化性的是(2)在
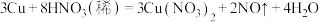 反应中:
反应中:①
②用单线桥法标出该反应电子转移的方向和数目:
③反应中稀硝酸表现出的性质是
a.还原性 b.酸性 c.氧化性。
(3)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 ;已知该反应中
;已知该反应中 只发生如下过程:
只发生如下过程: 。
。①该反应中,发生还原反应的过程是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)现有以下物质(用编号填写下列空白):①Al;②液态氧;③硝酸钾溶液;④KOH固体;⑤蔗糖;⑥SiO2;⑦NaCl;⑧空气;⑨硫酸铜晶体(CuSO4·5H2O);⑩NO2;属于酸性氧化物的是:_______ ;能导电的有:_______ ;属于电解质的是:_______ ;属于盐的有:_______ ;属于混合物的有:_______
(2)有以下物质,按要求用编号填空①NH3 ②CO2 ③NaOH ④Na2O2 ⑤Cl2 ⑥NH4Cl ⑦NaCl;含有极性共价键的物质有:_______ ;含有非极性共价键的物质有:_______ ;属于离子化合物的是:_______ ;只含离子键的有:_______
(3)用双线桥法标出Br2+SO2+2H2O=2HBr+H2SO4反应电子转移的方向和数目:_______ 。此反应中氧化剂是_______ ,还原剂是_______ ,还原产物是_______ ,当消耗32gSO2时,生成的氧化产物物质的量为_______
(1)现有以下物质(用编号填写下列空白):①Al;②液态氧;③硝酸钾溶液;④KOH固体;⑤蔗糖;⑥SiO2;⑦NaCl;⑧空气;⑨硫酸铜晶体(CuSO4·5H2O);⑩NO2;属于酸性氧化物的是:
(2)有以下物质,按要求用编号填空①NH3 ②CO2 ③NaOH ④Na2O2 ⑤Cl2 ⑥NH4Cl ⑦NaCl;含有极性共价键的物质有:
(3)用双线桥法标出Br2+SO2+2H2O=2HBr+H2SO4反应电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)①H2 + CuO  Cu + H2O
Cu + H2O
②CaCO3 + 2HCl==CaCl2 + CO2↑ + H2O
③3S + 6NaOH 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O
④NH4NO3 + Zn==ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl==2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是__________________________ (填序号)
(2)用双线桥法表示下述反应的电子转移MnO2 + 4HCl(浓) MnCl2 +Cl2↑+ 2H2O
MnCl2 +Cl2↑+ 2H2O________
(3)在反应 KIO3 + 6HI==3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为________ 。
(4)若反应 3Cu + 8HNO3(稀)==3Cu(NO3)2 + 2NO↑+ 4H2O中转移了3mol电子,则生成的NO气体在标况下的体积是_____________ L。
(5)配平下面两个反应① ____H2O + ____Cl2 +____ SO2 ==____H2SO4 + ____HCl,____________
② ____KMnO4 + ____HCl==____KCl + ____MnCl2 + ____Cl2↑ + ____H2O(系数是1的也请填上),_____
根据以上两个反应反应,写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平。______________________________________ 。
 Cu + H2O
Cu + H2O ②CaCO3 + 2HCl==CaCl2 + CO2↑ + H2O
③3S + 6NaOH
 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O ④NH4NO3 + Zn==ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl==2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是
(2)用双线桥法表示下述反应的电子转移MnO2 + 4HCl(浓)
 MnCl2 +Cl2↑+ 2H2O
MnCl2 +Cl2↑+ 2H2O(3)在反应 KIO3 + 6HI==3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为
(4)若反应 3Cu + 8HNO3(稀)==3Cu(NO3)2 + 2NO↑+ 4H2O中转移了3mol电子,则生成的NO气体在标况下的体积是
(5)配平下面两个反应① ____H2O + ____Cl2 +____ SO2 ==____H2SO4 + ____HCl,
② ____KMnO4 + ____HCl==____KCl + ____MnCl2 + ____Cl2↑ + ____H2O(系数是1的也请填上),
根据以上两个反应反应,写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)①H3PO2是一元中强酸,写出其电离方程式______________________ 。
②NaH2PO2为___________ (填“正盐”或“酸式盐”),其溶液显___________ (填“弱酸性”“中性”或“弱碱性”)。
③H3PO2中,P元素的化合价为___________ ;
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为________ 。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________ 。
(1)①H3PO2是一元中强酸,写出其电离方程式
②NaH2PO2为
③H3PO2中,P元素的化合价为
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应,写出白磷与Ba(OH)2溶液反应的化学方程式
您最近一年使用:0次
【推荐3】氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是____ (填字母)。

(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:____ ,其中水为____ 剂。
(3)过氧化氢俗称双氧水,医疗上利用它的杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),可经以下反应实现:KCN+H2O2+H2O=A+NH3↑,试写出生成物A的化学式:____ ,并阐明H2O2被称为绿色氧化剂的理由:____ 。
(4)氯化铵常用于焊接。如在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为CuO+NH4Cl Cu+CuCl2+N2↑+H2O(未配平)。
Cu+CuCl2+N2↑+H2O(未配平)。
①配平此氧化还原反应方程式__ CuO+__ NH4Cl
__ Cu+__ CuCl2+__ N2↑+__ H2O。
②该反应中,被氧化的元素是____ (填元素名称),氧化剂是______ (填化学式)。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是

(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(3)过氧化氢俗称双氧水,医疗上利用它的杀菌消毒作用来清洗伤口。H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),可经以下反应实现:KCN+H2O2+H2O=A+NH3↑,试写出生成物A的化学式:
(4)氯化铵常用于焊接。如在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为CuO+NH4Cl
 Cu+CuCl2+N2↑+H2O(未配平)。
Cu+CuCl2+N2↑+H2O(未配平)。①配平此氧化还原反应方程式

②该反应中,被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题。
Ⅰ.对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替现有以下物质:①Ba(OH)2 ②Cu ③CaCO3固体 ④Fe(OH)3胶体 ⑤酒精 ⑥氨气 ⑦稀硫酸 ⑧Na2O ⑨熔融的MgCl2
(1)属于电解质的是___________ 。
(2)写出①与⑦反应的离子方程式___________ 。
II.下列反应属于分类中的氧化还原反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O。
(3)在参加反应的HCl中,起还原剂作用的HCl与起酸性作用的HCl的物质的量之比为___________ 。
(4)用单线桥 法标明电子转移的方向和数目___________ 。
Ⅰ.对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替现有以下物质:①Ba(OH)2 ②Cu ③CaCO3固体 ④Fe(OH)3胶体 ⑤酒精 ⑥氨气 ⑦稀硫酸 ⑧Na2O ⑨熔融的MgCl2
(1)属于电解质的是
(2)写出①与⑦反应的离子方程式
II.下列反应属于分类中的氧化还原反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O。
(3)在参加反应的HCl中,起还原剂作用的HCl与起酸性作用的HCl的物质的量之比为
(4)用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)NH3是_____ 剂(填“氧化”或“还原”),在该反应中体现_____ 性(填“氧化”或“还原’);Cl2在该反应中_____ (填”得到“或”失去)电子,发生____ 反应(填“氧化”或“还原”)。
(2)氧化剂与还原剂的分子数之比为_____ 。
(3)当有4个NH3参加反应时,转移的电子个数为____ 。
(4)用双线桥的方法表示该反应的电子转移情况: 8NH3+3Cl2=6NH4Cl+N2____ 。
(5)用单线桥表示此反应中的电子转移情况: 8NH3+3Cl2=6NH4Cl+N2____ 。
(1)NH3是
(2)氧化剂与还原剂的分子数之比为
(3)当有4个NH3参加反应时,转移的电子个数为
(4)用双线桥的方法表示该反应的
(5)用单线桥表示此反应中的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室制取氯气有下列反应:2KMnO4+16HCl(浓) = 2MnCl2+2KCl+5Cl2↑+8H2O
(1)该反应中氧化剂是_______________ ;被还原的元素是 _______________ ;氧化产物是__________________ 。
(2)用单线桥法标出电子转移的方向和数目:
2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O____
(3)该反应有a个KMnO4参加反应,被氧化的HCl为______ 个,转移电子________ 个。(用含a的表达式表示)
(1)该反应中氧化剂是
(2)用单线桥法标出电子转移的方向和数目:
2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
(3)该反应有a个KMnO4参加反应,被氧化的HCl为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)实验室制取NO的反应如下:3Cu+8HNO3 (稀) =3Cu(NO3)2+2NO↑+4H2O,用双线桥法表示出电子转移的方向和数目___________ ,发生氧化反应的原子与发生还原反应的原子个数比为___________ ;该反应的离子方程式为___________ 。
(2)化工厂用浓氨水检验氯气管道是否漏气,利用的反应为:8NH3+3Cl2=N2+6NH4Cl
①氯元素的化合价___________ (填“升高”或“降低”)。
②反应中每消耗1个Cl2分子,转移___________ 个电子。
(1)实验室制取NO的反应如下:3Cu+8HNO3 (稀) =3Cu(NO3)2+2NO↑+4H2O,用双线桥法表示出电子转移的方向和数目
(2)化工厂用浓氨水检验氯气管道是否漏气,利用的反应为:8NH3+3Cl2=N2+6NH4Cl
①氯元素的化合价
②反应中每消耗1个Cl2分子,转移
您最近一年使用:0次
【推荐2】如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10mL盐酸于试管中,试回答下列问题:

(1)实验中观察到的现象是_______ 。
(2)产生上述现象的原因是_______ 。
(3)写出有关反应的离子方程式:_______ ;反应中转移了0.04mol电子时;标准状况下产生多少_______ mL的H2;生成的MgCl2物质的量浓度为_______ 。(溶液体积保持不变)
(4)由实验推知,镁片和盐酸的总能量_______ (填“大于”、“小于”或“等于”)MgCl2溶液和H2的总能量;此反应为_______ (填放热反应或者吸热反应)。

(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式:
(4)由实验推知,镁片和盐酸的总能量
您最近一年使用:0次

 按要求完成下列空格。
按要求完成下列空格。 被氧化,则产生
被氧化,则产生 的物质的量为
的物质的量为

