根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)NH3是_____ 剂(填“氧化”或“还原”),在该反应中体现_____ 性(填“氧化”或“还原’);Cl2在该反应中_____ (填”得到“或”失去)电子,发生____ 反应(填“氧化”或“还原”)。
(2)氧化剂与还原剂的分子数之比为_____ 。
(3)当有4个NH3参加反应时,转移的电子个数为____ 。
(4)用双线桥的方法表示该反应的电子转移情况: 8NH3+3Cl2=6NH4Cl+N2____ 。
(5)用单线桥表示此反应中的电子转移情况: 8NH3+3Cl2=6NH4Cl+N2____ 。
(1)NH3是
(2)氧化剂与还原剂的分子数之比为
(3)当有4个NH3参加反应时,转移的电子个数为
(4)用双线桥的方法表示该反应的
(5)用单线桥表示此反应中的
更新时间:2022-10-26 08:31:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
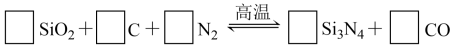
(1)配平上述反应的化学方程式(将化学计量数填在方框内);_____ SiO2+_____ C+_____ N2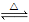
_____ Si3O4+_____ CO
(2)该反应的氧化剂是_________ ,其还原产物是_________ ;
(3)该反应产生标准状况下11.2升CO气体,则电子转移________ 摩尔。
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移______ (填大于、等于或小于)2摩尔,理由是__________________________ 。
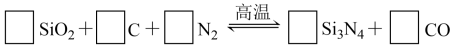
(1)配平上述反应的化学方程式(将化学计量数填在方框内);

(2)该反应的氧化剂是
(3)该反应产生标准状况下11.2升CO气体,则电子转移
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是___ 。
(2)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是___ ;过一会儿,溶液颜色逐渐褪去,起作用的成分是___ ;
(3)鉴别Na2CO3和NaHCO3溶液可选用___ 。(填序号)
①NaOH ②Ca(OH)2 ③BaCl2 ④K2SO4 ⑤Ca(NO3)2
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。
①其中被还原的元素是___ 。
②当反应有3.612×1024个电子转移时被硝酸钾氧化得到的氧化产物在标准状况下的体积___ 。
(5)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是___ ,R的相对原子质量是___ 。
(2)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是
(3)鉴别Na2CO3和NaHCO3溶液可选用
①NaOH ②Ca(OH)2 ③BaCl2 ④K2SO4 ⑤Ca(NO3)2
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。
①其中被还原的元素是
②当反应有3.612×1024个电子转移时被硝酸钾氧化得到的氧化产物在标准状况下的体积
(5)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯及其化合物有重要用途,氯气和 气体均常用于自来水消毒。以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
气体均常用于自来水消毒。以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
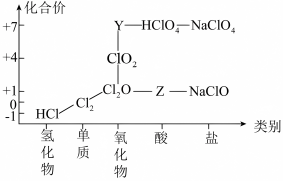
(1)根据图中信息写出Y、Z的化学式:______ 、______ 。
(2)已知高氯酸( )是强酸,写出高氯酸与氢氧化钠反应的离子方程式:
)是强酸,写出高氯酸与氢氧化钠反应的离子方程式:______ 。
(3)已知:消毒效率可用单位质量消毒剂得到的电子数的相对大小来表示。 是最早用于饮用水消毒的物质,
是最早用于饮用水消毒的物质, 是一种新的广谱消毒剂。等质量的
是一种新的广谱消毒剂。等质量的 和
和 消毒效率较高的是
消毒效率较高的是______ (填化学式);
(4)工业常用 和
和 溶液混合酸化后反应制得
溶液混合酸化后反应制得 气体,该反应的离子方程式为:
气体,该反应的离子方程式为:______ 。
(5)84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。其原理为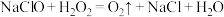 ,反应产生的
,反应产生的 促进藻类快速生长。
促进藻类快速生长。
①该反应说明氧化性:NaClO______  (填“>”或“<”)。
(填“>”或“<”)。
②当标准状况下有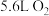 生成时,转移电子
生成时,转移电子______ mol。
高铁酸钠( )是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为
)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为 离子,制取高铁酸钠的化学方程式如下:
离子,制取高铁酸钠的化学方程式如下:
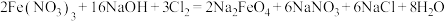
(6)在上述反应中______ (元素名称)元素被氧化,氧化剂是______ (化学式)。
(7)高铁酸钠( )是一种新型净水剂。在水处理过程中,
)是一种新型净水剂。在水处理过程中, 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮物聚沉。向
胶体,使水中悬浮物聚沉。向 胶体中逐滴加入HCl稀溶液至过量,会出现的现象是:
胶体中逐滴加入HCl稀溶液至过量,会出现的现象是:______ 。
(8)实验室制备 胶体的离子方程式:
胶体的离子方程式:______ 。
 气体均常用于自来水消毒。以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
气体均常用于自来水消毒。以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
(1)根据图中信息写出Y、Z的化学式:
(2)已知高氯酸(
 )是强酸,写出高氯酸与氢氧化钠反应的离子方程式:
)是强酸,写出高氯酸与氢氧化钠反应的离子方程式:(3)已知:消毒效率可用单位质量消毒剂得到的电子数的相对大小来表示。
 是最早用于饮用水消毒的物质,
是最早用于饮用水消毒的物质, 是一种新的广谱消毒剂。等质量的
是一种新的广谱消毒剂。等质量的 和
和 消毒效率较高的是
消毒效率较高的是(4)工业常用
 和
和 溶液混合酸化后反应制得
溶液混合酸化后反应制得 气体,该反应的离子方程式为:
气体,该反应的离子方程式为:(5)84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。其原理为
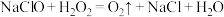 ,反应产生的
,反应产生的 促进藻类快速生长。
促进藻类快速生长。①该反应说明氧化性:NaClO
 (填“>”或“<”)。
(填“>”或“<”)。②当标准状况下有
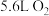 生成时,转移电子
生成时,转移电子高铁酸钠(
 )是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为
)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为 离子,制取高铁酸钠的化学方程式如下:
离子,制取高铁酸钠的化学方程式如下: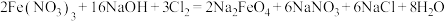
(6)在上述反应中
(7)高铁酸钠(
 )是一种新型净水剂。在水处理过程中,
)是一种新型净水剂。在水处理过程中, 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮物聚沉。向
胶体,使水中悬浮物聚沉。向 胶体中逐滴加入HCl稀溶液至过量,会出现的现象是:
胶体中逐滴加入HCl稀溶液至过量,会出现的现象是:(8)实验室制备
 胶体的离子方程式:
胶体的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钠能形成多种化合物,如Na2O、Na2O2、Na2CO3、NaHCO3、NaCl、NaOH、NaH等,向答下列下列问题。
(1)NaHCO3电离方程式为:_______ ,在正盐、含氧酸盐、酸式盐、钠盐等类别中,它不属于其中的_______ 。
(2)从性质角度分类,Na2O属于_______ 氧化物;写出其与盐酸反应的离子方程式_______ 。
(3)区别Na2CO3、NaHCO3两种溶液的试剂是_______ ,实验室可利用复分解反应制备少量NaOH,写出相应的化学方程式:_______ 。
(4)实验室中可利用Na2O2制取一定量O2,写出相应的化学方程式并标出电子转移方向与数目:_______ ,Na2O2有强氧化性,能氧化许多物质,将适量Na2O2加入到FeCl2溶液中,除看到有气泡产生后,还能观察到的主要现象是_______ 。
(1)NaHCO3电离方程式为:
(2)从性质角度分类,Na2O属于
(3)区别Na2CO3、NaHCO3两种溶液的试剂是
(4)实验室中可利用Na2O2制取一定量O2,写出相应的化学方程式并标出电子转移方向与数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有一种制氢储氢材料氢化钠(NaH)在室温下结合CO2制氢,反应为4NaH+3CO2=2Na2CO3+C+2H2,NaH的电子式为_____ ,在化学方程式上标出该反应中电子转移的方向与数目_____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】车用安全气囊中含有叠氮化钠(NaN3)、硝酸钾(KNO3)、二氧化硅(SiO2)粉等。其工作原理如下:
①车辆强碰撞后,激活特定的电路,放电使NaN3迅速分解,生成Na并放出N2
②生成的Na与KNO3发生二次反应:10Na+2KNO3=K2O+5Na2O+N2↑
③SiO2与K2O、Na2O反应生成盐,消除两种碱性氧化物的腐蚀性。
(1)关于KNO3,下列分析正确的是___________。
(2)写出NaN3分解反应中氧化产物和还原产物的物质的量之比为___________ 。
(3)标出二次反应电子转移的数目和方向:___________ 。
(4)能保护司机不受伤害的气囊需要65L的N2.在2个大气压和40℃的条件下,
①65L N2是___________ 摩N2。
②得到这些N2,需要NaN3___________ 克?
(已知2个大气压和40℃气体摩尔体积约为12.84L/mol。列式计算,结果保留一位小数)
①车辆强碰撞后,激活特定的电路,放电使NaN3迅速分解,生成Na并放出N2
②生成的Na与KNO3发生二次反应:10Na+2KNO3=K2O+5Na2O+N2↑
③SiO2与K2O、Na2O反应生成盐,消除两种碱性氧化物的腐蚀性。
(1)关于KNO3,下列分析正确的是___________。
| A.KNO3电离需要通电 |
| B.KNO3是强电解质,其水溶液的导电性一定强 |
C.熔融状态的KNO3中含自由移动的K+和 |
D.固态KNO3不导电,因其中不含K+和 |
(3)标出二次反应电子转移的数目和方向:
(4)能保护司机不受伤害的气囊需要65L的N2.在2个大气压和40℃的条件下,
①65L N2是
②得到这些N2,需要NaN3
(已知2个大气压和40℃气体摩尔体积约为12.84L/mol。列式计算,结果保留一位小数)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)实验室制备氯气的化学方程式为:4HCl(浓)+MnO2═MnCl2+ Cl2+2H2O,其中氧化产物是__________ ,HCl在反应中表现了___________ (填性质)
(2)2Na2O2+2H2O═4NaOH+O2,其中氧化剂和还原剂的物质的量之比为_____ 。当反应中有2mol电子转移时,生成气体的体积为___________ 。(在标准状况下)。
(3)SO2+2H2S═3S+2H2O,其中氧化产物和还原产物的质量之比为___________ 。
(2)2Na2O2+2H2O═4NaOH+O2,其中氧化剂和还原剂的物质的量之比为
(3)SO2+2H2S═3S+2H2O,其中氧化产物和还原产物的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】阅读下列科普短文并回答相应问题。目前,我国的电动汽车约有80%应用的电池为磷酸铁锂电池,2021年将有约9400吨的磷酸铁锂报废,为了避免环境污染,更为了减少资源与经济损失,必须对废弃的电池进行回收。通常采用的湿法冶金回收工艺为:首先用① 溶液浸泡拆解下来的材料,材料中的②
溶液浸泡拆解下来的材料,材料中的② 与③
与③ 溶解得到④
溶解得到④ 溶液和含⑤石墨、
溶液和含⑤石墨、 的滤渣,再用⑥稀
的滤渣,再用⑥稀 和⑦稀
和⑦稀 的混合液浸泡滤渣(产生的⑧
的混合液浸泡滤渣(产生的⑧ 经回收处理转化为硝酸,可循环利用),得到含
经回收处理转化为硝酸,可循环利用),得到含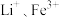 和磷酸的浸出液,再调节浸出液的
和磷酸的浸出液,再调节浸出液的 得到⑨
得到⑨ 沉淀,过滤浸出液,加⑩固体
沉淀,过滤浸出液,加⑩固体 浓缩结晶得
浓缩结晶得 晶体。
晶体。
(1)上述短文中的①~⑩(仅指划线的部分)中,能导电的是___________ (填序号,下同),属于电解质的是___________ ,属于非电解质的是___________ ,既能与强酸反应又能与强碱反应的是___________ 。
(2)上述短文中的 中的铁的化合价为
中的铁的化合价为___________ ,当有标准状况下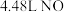 产生时,参加反应的
产生时,参加反应的 的物质的量为
的物质的量为___________  。
。
(3)上述短文中“用 溶液浸泡时,单质
溶液浸泡时,单质 与
与 溶液反应的化学方程式为:
溶液反应的化学方程式为:___________ 。
(4)上述短文中使用稀硫酸的浓度为 ,现需要用98%的浓硫酸(密度为
,现需要用98%的浓硫酸(密度为 )配制该稀硫酸
)配制该稀硫酸 ,需要浓硫酸的体积为
,需要浓硫酸的体积为___________  (保留1位小数),配制过程中用到的仪器有:量筒、烧杯、玻璃棒、胶头滴管、
(保留1位小数),配制过程中用到的仪器有:量筒、烧杯、玻璃棒、胶头滴管、___________ 。
 溶液浸泡拆解下来的材料,材料中的②
溶液浸泡拆解下来的材料,材料中的② 与③
与③ 溶解得到④
溶解得到④ 溶液和含⑤石墨、
溶液和含⑤石墨、 的滤渣,再用⑥稀
的滤渣,再用⑥稀 和⑦稀
和⑦稀 的混合液浸泡滤渣(产生的⑧
的混合液浸泡滤渣(产生的⑧ 经回收处理转化为硝酸,可循环利用),得到含
经回收处理转化为硝酸,可循环利用),得到含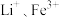 和磷酸的浸出液,再调节浸出液的
和磷酸的浸出液,再调节浸出液的 得到⑨
得到⑨ 沉淀,过滤浸出液,加⑩固体
沉淀,过滤浸出液,加⑩固体 浓缩结晶得
浓缩结晶得 晶体。
晶体。(1)上述短文中的①~⑩(仅指划线的部分)中,能导电的是
(2)上述短文中的
 中的铁的化合价为
中的铁的化合价为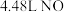 产生时,参加反应的
产生时,参加反应的 的物质的量为
的物质的量为 。
。(3)上述短文中“用
 溶液浸泡时,单质
溶液浸泡时,单质 与
与 溶液反应的化学方程式为:
溶液反应的化学方程式为:(4)上述短文中使用稀硫酸的浓度为
 ,现需要用98%的浓硫酸(密度为
,现需要用98%的浓硫酸(密度为 )配制该稀硫酸
)配制该稀硫酸 ,需要浓硫酸的体积为
,需要浓硫酸的体积为 (保留1位小数),配制过程中用到的仪器有:量筒、烧杯、玻璃棒、胶头滴管、
(保留1位小数),配制过程中用到的仪器有:量筒、烧杯、玻璃棒、胶头滴管、
您最近一年使用:0次



