过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,在空气中保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入_______ 溶液(填化学式),充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。_______ ,有同学提出该实验装置A、C装置之间没必要增加盛有饱和NaHCO3溶液的洗气瓶,该同学想法是否有道理?且说明理由:_______ 。(答“有”或“无”且说明理由)
②将仪器连接好以后,必须进行的第一步操作是_______ 。
③写出装置C中发生的主要反应的化学方程式:_______ 。
④装置D的作用是_______ ;若无装置D,样品中Na2O2的质量分数_______ (填“偏高”“偏低”或“无影响”)。
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为_______ (用含ρ、m、V的代数式表示)。
(1)探究一包Na2O2样品是否已经变质:取少量样品,加水将其溶解,加入
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计用下图装置来测定过氧化钠的质量分数。
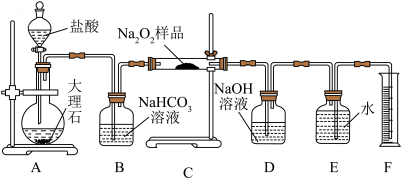
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生的主要反应的化学方程式:
④装置D的作用是
⑤实验结束后,装置F中水的体积为VmL,已知氧气的密度为ρg·mL-1,样品中Na2O2质量分数为
更新时间:2024-01-18 10:42:29
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】如图A、B、C、D五种物质都是含钠元素的单质或化合物,B为淡黄色固体,根据关系图回答下列问题。
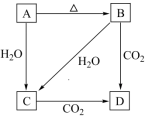
(1)写出下列符号所代表的物质的化学式:
A:_______ ,B:_______ ;C:_______ ,D:_______ 。
(2)写出下列物质转化的化学方程式。
①A→B:_______ 。
②B→D:_______ 。
③A→C:_______ 。

(1)写出下列符号所代表的物质的化学式:
A:
(2)写出下列物质转化的化学方程式。
①A→B:
②B→D:
③A→C:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A~E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质。请回答下列问题。
(1)写出C~E的化学式:
C______ ,D______ ,E______ 。
(2)写出下列反应的化学方程式:
① B→C________________ ;
②C→D________________ ;
③D→E________________ ;
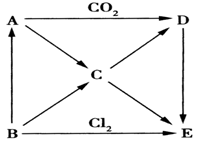
(1)写出C~E的化学式:
C
(2)写出下列反应的化学方程式:
① B→C
②C→D
③D→E
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】为探究碳酸氢钠的热稳定性,并利用其产物验证过氧化钠与二氧化碳的反应,按以下装置图进行实验。
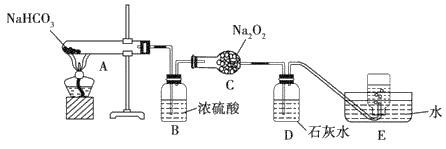
请回答下列问题:
(1)A中反应的化学方程式为______ 。
(2)B中浓硫酸的作用是______ 。
(3)C中发生反应的化学方程式为______ 。
(4)D中现象是______ ,反应的离子方程式是______ 。
(5)E中收集的气体主要是______ 。

请回答下列问题:
(1)A中反应的化学方程式为
(2)B中浓硫酸的作用是
(3)C中发生反应的化学方程式为
(4)D中现象是
(5)E中收集的气体主要是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】三硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子,某化学兴趣小组对Na2CS3的一些性质进行了探究性实验。
实验Ⅰ.探究Na2CS3的性质:
(1)H2CS3是___ (填“强”或“弱”)酸。
(2)已知步骤③中反应的氧化产物是SO42-,则该反应的离子方程式为:____ 。
(3)某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测定产生的白色沉淀的质量即可求出实验中所用的Na2CS3的质量。你是否同意他的观点,并说明理由:___ 。
实验Ⅱ.测定Na2CS3溶液的浓度:
按如图所示装置进行实验:将50.0mLNa2CS3溶液置于三颈烧瓶中,打开仪器M的活塞,滴入足量2.0mol·L-1的稀H2SO4,关闭活塞。

已知:CS32- +2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(4)仪器M的名称是___ 。反应开始前需要先通入一段时间N2,其作用为____ 。
(5)B中发生反应的离子方程式为:____ 。
(6)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉淀质量之前需要进行的实验操作是___ 。若B中生成沉淀的质量为8.4g,则Na2CS3溶液的物质的量浓度是____ 。
实验Ⅰ.探究Na2CS3的性质:
| 步骤 | 操作及现象 |
| ① | 取少量Na2CS3固体溶于蒸馏水中,配制成溶液并分成两等份 |
| ② | 向其中一份溶液中滴加几滴酚酞试剂,溶液变成红色 |
| ③ | 向另一份溶液中滴加用硫酸酸化的KMnO4溶液,紫色褪去 |
(2)已知步骤③中反应的氧化产物是SO42-,则该反应的离子方程式为:
(3)某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测定产生的白色沉淀的质量即可求出实验中所用的Na2CS3的质量。你是否同意他的观点,并说明理由:
实验Ⅱ.测定Na2CS3溶液的浓度:
按如图所示装置进行实验:将50.0mLNa2CS3溶液置于三颈烧瓶中,打开仪器M的活塞,滴入足量2.0mol·L-1的稀H2SO4,关闭活塞。

已知:CS32- +2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(4)仪器M的名称是
(5)B中发生反应的离子方程式为:
(6)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉淀质量之前需要进行的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
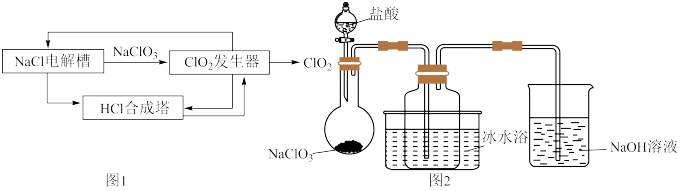
【推荐2】二氧化氯(ClO2)是一种高效、安全的消毒剂,常温下是一种黄绿色气体,11℃时液化成红棕色液体,易溶于水但不与水反应。工业上著名的开斯汀法制备二氧化氯的部分流程图如图1。某研究小组用图2装置模拟ClO2发生器中的反应来制备ClO2(夹持装置已略去)。
(1)写出NaClO3与盐酸制备ClO2的离子方程式:___ 。
(2)冰水浴的作用是___ 。
(3)NaOH溶液中发生的主要反应的离子方程式为___ 。
(4)ClO2常用作自来水消毒剂,碘量法可以检测水中ClO2的浓度,步骤如下:
①取500mL水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝(已知ClO2全部转化为NaClO2);
②用1.0×10-3mol/L的Na2SO3溶液滴定,消耗Na2SO3溶液10.00mL(已知:2S2O +I2=S4O
+I2=S4O +2I-);确定操作②达到滴定终点的现象是
+2I-);确定操作②达到滴定终点的现象是___ ;经计算,水样中ClO2的浓度是__ mg/L。
(5)一定温度和电压下,电解精制食盐水可制得NaClO3和H2。已知3Cl2+6OH-=ClO +5Cl-+3H2O,电解时应选用
+5Cl-+3H2O,电解时应选用___ 交换膜(填“阳离子”或“阴离子”),阴极电极反应式为___ 。

(1)写出NaClO3与盐酸制备ClO2的离子方程式:
(2)冰水浴的作用是
(3)NaOH溶液中发生的主要反应的离子方程式为
(4)ClO2常用作自来水消毒剂,碘量法可以检测水中ClO2的浓度,步骤如下:
①取500mL水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝(已知ClO2全部转化为NaClO2);
②用1.0×10-3mol/L的Na2SO3溶液滴定,消耗Na2SO3溶液10.00mL(已知:2S2O
 +I2=S4O
+I2=S4O +2I-);确定操作②达到滴定终点的现象是
+2I-);确定操作②达到滴定终点的现象是(5)一定温度和电压下,电解精制食盐水可制得NaClO3和H2。已知3Cl2+6OH-=ClO
 +5Cl-+3H2O,电解时应选用
+5Cl-+3H2O,电解时应选用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
资料:氰化钠化学式NaCN(C元素+2价,N元素-3价),白色结晶颗粒、易潮解、有微弱的苦杏仁气味、剧毒、易溶于水、易水解生成氰化氢、水溶液呈碱性。
(1)氰化钠(NaCN)溶液呈碱性,其原因是____________ (用离子方程式解释)。
(2)“8.12”爆炸事故后,当地政府组织群众用双氧水喷洒,用双氧水处理NaCN产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式_____________ 。
某化学兴趣小组在实验室制备硫代硫酸钠,并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过如右图所示装置制备Na2S2O3。

(3)右图a装置中盛装Na2SO3
固体的仪器名称是______________ ;
b装置的作用是________________ 。
(4)装置c中的产物有Na2S2O3和C02气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有________________________ 。
(5)实验结束后,在e处最好连接盛______________ (选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。已知:
①废水中氰化钠的最高排放标准为0.50 mg/L。
② AgI呈黄色,且CN -优先与Ag+反应。
AgI呈黄色,且CN -优先与Ag+反应。
实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中并滴加几滴KI溶液作指示剂,用1.000 ×10-4 mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6)滴定终点的判断方法是_______________ 。
(7)处理后的废水中氰化钠的含量为_____________ mg/L。
资料:氰化钠化学式NaCN(C元素+2价,N元素-3价),白色结晶颗粒、易潮解、有微弱的苦杏仁气味、剧毒、易溶于水、易水解生成氰化氢、水溶液呈碱性。
(1)氰化钠(NaCN)溶液呈碱性,其原因是
(2)“8.12”爆炸事故后,当地政府组织群众用双氧水喷洒,用双氧水处理NaCN产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式
某化学兴趣小组在实验室制备硫代硫酸钠,并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过如右图所示装置制备Na2S2O3。

(3)右图a装置中盛装Na2SO3
固体的仪器名称是
b装置的作用是
(4)装置c中的产物有Na2S2O3和C02气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有
(5)实验结束后,在e处最好连接盛
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。已知:
①废水中氰化钠的最高排放标准为0.50 mg/L。
②
 AgI呈黄色,且CN -优先与Ag+反应。
AgI呈黄色,且CN -优先与Ag+反应。实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中并滴加几滴KI溶液作指示剂,用1.000 ×10-4 mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6)滴定终点的判断方法是
(7)处理后的废水中氰化钠的含量为
您最近一年使用:0次



