现有八种物质: ①铁粉 ②NH3 ③稀盐酸 ④熔融FeCl3 ⑤CH4 ⑥CaCO3固体 ⑦CuSO4溶液 ⑧Fe3O4。
(1)①-⑥属于电解质的是_______ 。
(2)写出③与⑧反应的离子方程式_______ 。将③与⑧反应后的溶液和⑦混合,再加入过量的①,反应结束后,一定没有的阳离子为_________ 。
(3)标准状况下,4.8g⑤中所含氢原子数与______ molH2O所含氢原子数相等。
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为______ mol/L ,溶质的质量分数为_______ 。
(1)①-⑥属于电解质的是
(2)写出③与⑧反应的离子方程式
(3)标准状况下,4.8g⑤中所含氢原子数与
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为
更新时间:2024-01-21 21:32:00
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】简单计算题,只填写结果。
(1)标准状况下33.6 L H2中,所含质子个数是___________ 。
(2)所含电子的物质的量为4mol的H2 ,标况下的体积是___________ 。
(3)20℃时45gH2O ,所含原子个数是___________ 。
(4)标况下,16gO2与14gN2的混合气体所占的体积是___________ 。
(5)含原子总数约为1.204×1024的NH3 的质量是___________ 。
(1)标准状况下33.6 L H2中,所含质子个数是
(2)所含电子的物质的量为4mol的H2 ,标况下的体积是
(3)20℃时45gH2O ,所含原子个数是
(4)标况下,16gO2与14gN2的混合气体所占的体积是
(5)含原子总数约为1.204×1024的NH3 的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】物质的量是化学计算的重要工具,按要求完成下列计算
(1) 中含
中含 0.4mol,则
0.4mol,则 的摩尔质量为
的摩尔质量为_______ 。
(2)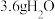 中含有的电子数为
中含有的电子数为_______ 。
(3)某人的血糖化验单显示血液中葡萄糖( ;
;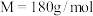 )为
)为 ,此人1mL血液中含葡萄糖
,此人1mL血液中含葡萄糖_______ mg。
(4)用1L1.0mol/LNaOH溶液吸收 ,所得溶液中的
,所得溶液中的 和
和 的浓度之比为
的浓度之比为_______ 。
(5)在标准状况下,CO和 混合气体的质量为36g,体积为22.4L,则其中
混合气体的质量为36g,体积为22.4L,则其中 的物质的量为
的物质的量为_______ 。
(1)
 中含
中含 0.4mol,则
0.4mol,则 的摩尔质量为
的摩尔质量为(2)
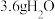 中含有的电子数为
中含有的电子数为(3)某人的血糖化验单显示血液中葡萄糖(
 ;
;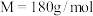 )为
)为 ,此人1mL血液中含葡萄糖
,此人1mL血液中含葡萄糖(4)用1L1.0mol/LNaOH溶液吸收
 ,所得溶液中的
,所得溶液中的 和
和 的浓度之比为
的浓度之比为(5)在标准状况下,CO和
 混合气体的质量为36g,体积为22.4L,则其中
混合气体的质量为36g,体积为22.4L,则其中 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】按要求填写下列空格(设阿伏加德罗常数的值为NA)
(1)在标准状况下,0.5molO2的体积为_______ L;
(2)某2LMgCl2溶液中含有4molCl-,MgCl2溶液的物质的量浓度为_______ mol/L;
(3)在标准状况下,44.8L的氢气质量为_______ g;
(4)39gNa2O2中的Na+数目为_______ NA。
(1)在标准状况下,0.5molO2的体积为
(2)某2LMgCl2溶液中含有4molCl-,MgCl2溶液的物质的量浓度为
(3)在标准状况下,44.8L的氢气质量为
(4)39gNa2O2中的Na+数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】常温下,计算浓度为0.05mol/L的硫酸溶液的pH。______
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】室温下,向 100 mL NaOH、Ba(OH)2 的混合溶液中加入 100 mL 0.3 mol·L-1 的 H2SO4 溶液,充分反应,得沉淀 2.33 g,反应后测得溶液的 pH=13(假设反应后溶液的总体积为 200 mL)。 请计算:
(1)原混合溶液中所含的Ba(OH)2物质的量是_______ mol。
(2)原混合溶液中 NaOH 的物质的量浓度是_______ mol·L-1
(1)原混合溶液中所含的Ba(OH)2物质的量是
(2)原混合溶液中 NaOH 的物质的量浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有下列一组物质:①云雾② ③CaO④Na⑤
③CaO④Na⑤ ⑥有色玻璃⑦
⑥有色玻璃⑦ ⑧
⑧ 溶液⑨
溶液⑨ ⑩
⑩ ,回答下列问题:
,回答下列问题:
(1)属于同素异形体的是___________ (填序号)。
(2)具有丁达尔效应的是___________ (填序号)。
(3)能与水剧烈反应,且熔融状态能导电的电解质是_______ (填序号)。
(4)属于单质,且常温下能与水反应,写出该反应的离子方程式:___________ 。
(5)某试管中盛有⑨⑩的混合物,用酒精灯加热过程中产生能使澄清石灰水变浑浊的气体,则试管中反应的化学方程式是___________ 。
 ③CaO④Na⑤
③CaO④Na⑤ ⑥有色玻璃⑦
⑥有色玻璃⑦ ⑧
⑧ 溶液⑨
溶液⑨ ⑩
⑩ ,回答下列问题:
,回答下列问题:(1)属于同素异形体的是
(2)具有丁达尔效应的是
(3)能与水剧烈反应,且熔融状态能导电的电解质是
(4)属于单质,且常温下能与水反应,写出该反应的离子方程式:
(5)某试管中盛有⑨⑩的混合物,用酒精灯加热过程中产生能使澄清石灰水变浑浊的气体,则试管中反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中,
(1)氧化剂是__ ,氧化产物是__ .
(2)写出该反应的离子方程式.__ .
(3)若有219gHCl参加反应,产生Cl2的体积(标况下)为__ L,转移电子__ mol.
(4)Cl2有毒,多余的Cl2通常用氢氧化钠溶液吸收,反应的离子方程式为:__ .
(1)氧化剂是
(2)写出该反应的离子方程式.
(3)若有219gHCl参加反应,产生Cl2的体积(标况下)为
(4)Cl2有毒,多余的Cl2通常用氢氧化钠溶液吸收,反应的离子方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】有下列物质:①Ba(OH)2固体;②KHSO4固体;③稀盐酸;④铜;⑤SO2;⑥Al(OH)3;⑦浓氨水;⑧乙醇;⑨Cl2。
(1)上述物质中属于电解质的是_______ (填序号,下同),能导电的是_______ 。
(2)写出物质②在水中的电离方程式:_______ ,写出①和③反应的离子反应方程式:_______ 。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉。以上物质能用于治疗胃酸过多的是_______ (填序号),医疗上在X射线照射下检查胃有无病变,常用“钡餐”作为造影剂,“钡餐”主要成分的化学式为_______ (填“BaCO3”或“BaSO4”)。
(1)上述物质中属于电解质的是
(2)写出物质②在水中的电离方程式:
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉。以上物质能用于治疗胃酸过多的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。请写出反应的化学方程式____________
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.下表是生活、生产中常见的物质,表中列出了它们的一种主要成分(其他成分未列出)。
(1)请你对表中①~⑧的主要成分进行分类(填编号):属于盐的是________ ,属于电解质的是________ ,属于非电解质的是________________ 。
(2)写出②与⑦反应的离子方程式:____________________________________ ,少量盐酸与③反应的离子方程式为__________________________________________________________ 。
Ⅱ.在Fe(OH)3胶体中逐渐滴入HI稀溶液,会出现一系列变化:
(3)①先出现红褐色沉淀,原因是________________________________________________ 。
②随后沉淀溶解,溶液呈黄色,此反应的离子方程式是____________________________
③最后溶液颜色加深,此反应的离子方程式是____________________________________
(4)若用稀盐酸代替HI稀溶液,能出现(3)中所述变化现象中的________ (填写上面各题序号)。
| 编号 | ① | ② | ③ | ④ |
| 名称 | 绿矾 | 醋 | 苏打 | 酒精 |
| 主要成分 | FeSO4 | CH3COOH | Na2CO3 | CH3CH2OH |
| 编号 | ⑤ | ⑥ | ⑦ | ⑧ |
| 名称 | 铜导线 | 蔗糖 | 烧碱 | 铁锈 |
| 主要成分 | Cu | C12H22O11 | NaOH | Fe2O3 |
(1)请你对表中①~⑧的主要成分进行分类(填编号):属于盐的是
(2)写出②与⑦反应的离子方程式:
Ⅱ.在Fe(OH)3胶体中逐渐滴入HI稀溶液,会出现一系列变化:
(3)①先出现红褐色沉淀,原因是
②随后沉淀溶解,溶液呈黄色,此反应的离子方程式是
③最后溶液颜色加深,此反应的离子方程式是
(4)若用稀盐酸代替HI稀溶液,能出现(3)中所述变化现象中的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某化学兴趣小组为探究Fe2+、Fe3+的性质进行了一系列试验。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑, 其目的是________________ 。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明氯水可将Fe2+氧 化。FeCl2溶液与氯水反应的离子方程式为________________________________ 。
(3)乙组同学认为甲组同学的实验不够严谨,请你改进一下,并简述实验方案:(可选用药品:01mol• L-1 FeCl2溶液、氯水、KSCN溶液、煤油)______________________________________________________________ 。
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________________________________ 。
(5)丁组同学取10mL 0.1mol• L-1 KI溶液,加入6mL0.1mol• L-1 FeCl3溶液,充分反应。取1mL反应后溶液加入1mLCCl4充分振荡、静置,观察到的现象是________________________________ 。
(6)四个小组的同学通过实验探究,得出结论:Fe2+有____________ 性;Fe3+、Cl2、I2的氧化性由大到小的顺序是________________________ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑, 其目的是
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明氯水可将Fe2+氧 化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组同学的实验不够严谨,请你改进一下,并简述实验方案:(可选用药品:01mol• L-1 FeCl2溶液、氯水、KSCN溶液、煤油)
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(5)丁组同学取10mL 0.1mol• L-1 KI溶液,加入6mL0.1mol• L-1 FeCl3溶液,充分反应。取1mL反应后溶液加入1mLCCl4充分振荡、静置,观察到的现象是
(6)四个小组的同学通过实验探究,得出结论:Fe2+有
您最近一年使用:0次



