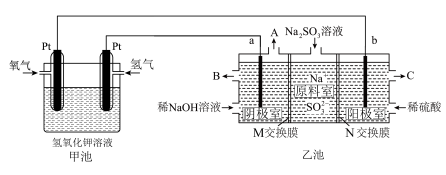
工业上常用 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。_______ 极(填“正”或“负”),写出通入氢气的电极反应式_______ 。
(2)①乙池中阳极室 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为_______ (填“阳”或“阴”)离子交换膜,写出阳极室的电极反应式_______ 。
②阴极室中 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的_______ (用离子符号或化学式填空,下同)得电子反应生成_______ ,其浓度减小,使溶液中_______ 浓度增大,为了保持阴极室溶液中阴阳离子电荷平衡,_______ 从原料室向阴极室迁移,从而使阴极室中 的浓度增大。
的浓度增大。
(3)在标准状况下,若甲池中有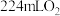 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成_______ 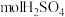 。
。
(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上, 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为_______ 。
 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。
(2)①乙池中阳极室
 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为②阴极室中
 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的 的浓度增大。
的浓度增大。(3)在标准状况下,若甲池中有
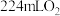 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成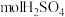 。
。(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上,
 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为
更新时间:2024-01-21 22:32:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据有关知识,填写下列空白:
(1)已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ,则由1 mol氢气和1 mol碘反应生成HI会放出_______ kJ的热量
(2)某同学做如下实验,以检验反应中的能量变化。

①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是_______ 热反应;
②根据能量守恒定律,(b)中反应物的总能量应该_______ 其生成物的总能量(填“>”或“<”)。
(3)下列过程中不一定放热的是_______ (填字母)。
a.铝热反应 b.炸药爆炸 c.燃料燃烧 d.分解反应 e.酸碱中和
(4)分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。回答下列问题:
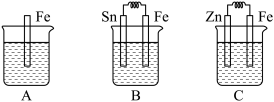
①下列叙述中,正确的是_______ 。
A.B 、C 中铁片均是为负极 B.三个烧杯中铁片表面均无气泡产生
C.产生气泡的速率 A 中比B中慢 D.C 溶液中SO 向Fe片电极移动
向Fe片电极移动
②若把Ba(OH)2·8H2O 晶体与 NH4Cl晶体反应设计成原电池,你认为是否可行?_______ (填“是”或“否”)。
(1)已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ,则由1 mol氢气和1 mol碘反应生成HI会放出
(2)某同学做如下实验,以检验反应中的能量变化。

①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
②根据能量守恒定律,(b)中反应物的总能量应该
(3)下列过程中不一定放热的是
a.铝热反应 b.炸药爆炸 c.燃料燃烧 d.分解反应 e.酸碱中和
(4)分别按下图 A、B、C 所示装置进行实验,三个烧杯里的溶液为同浓度的稀硫酸。回答下列问题:

①下列叙述中,正确的是
A.B 、C 中铁片均是为负极 B.三个烧杯中铁片表面均无气泡产生
C.产生气泡的速率 A 中比B中慢 D.C 溶液中SO
 向Fe片电极移动
向Fe片电极移动②若把Ba(OH)2·8H2O 晶体与 NH4Cl晶体反应设计成原电池,你认为是否可行?
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)依据氧化还原反应2Fe3+(aq) +Cu(s)=Cu2+(aq)+2Fe2+(aq)设计的原电池如图所示:
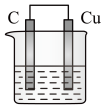
请回答下列问题:
①电解质溶液是_________ (填化学式)溶液。
②石墨电极上发生反应的类型为_________ (填“氧化”或“还原”)反应。
(2)某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如图。则电极a是电池的___ (填“正”或“负")极,该电池的总反应式为________________ 。
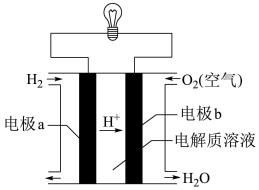

请回答下列问题:
①电解质溶液是
②石墨电极上发生反应的类型为
(2)某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如图。则电极a是电池的

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图所示的是曾经在实验是观察过的实验。
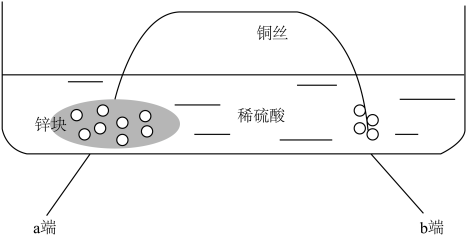
(1)实验中在b端观察到有气泡产生,此时根据氧化还原反应的原理,发生的反应过程可以表示为___________ ,由此可以推测在a端,除可见的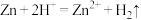 以外,还发生有的反应过程有
以外,还发生有的反应过程有___________ 。
(2)在某次实验中,有同学设计以下实验方案,取0.650g的Zn粒与足量的稀硫酸反应,待反应完全以后,设法收集到在b端产生的氢气有22.3mL(折算为实验条件下H2的质量为0.002g)。请计算在a、b两端产生的氢气的质量比。___________

(1)实验中在b端观察到有气泡产生,此时根据氧化还原反应的原理,发生的反应过程可以表示为
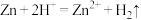 以外,还发生有的反应过程有
以外,还发生有的反应过程有(2)在某次实验中,有同学设计以下实验方案,取0.650g的Zn粒与足量的稀硫酸反应,待反应完全以后,设法收集到在b端产生的氢气有22.3mL(折算为实验条件下H2的质量为0.002g)。请计算在a、b两端产生的氢气的质量比。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图,C、D、E、F、X、Y都是惰性电极,A、B为电源,丙为精炼铜装置。接通电源一段时间后,X极液体颜色变深[ 胶粒带正电荷]。
胶粒带正电荷]。
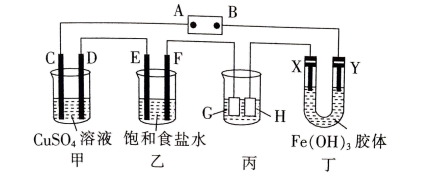
(1)A为电源的___________ (填“正极”或“负极”)。
(2)若甲中装有100mL0.5
 溶液,工作一段时间后,
溶液,工作一段时间后, 恰好完全被消耗,停止通电,此时,测得溶液的pH=
恰好完全被消耗,停止通电,此时,测得溶液的pH=___________ (假设溶液的体积不变)。
(3)通电后,E极的电极反应式为___________ ;检验F极产物的方法是___________ 。
(4)G和H极分别是___________ (填“粗铜”或“纯铜”,下同)和___________ 。
(5)若装置中的溶液都足量,当电路中有0.02mol电子转移时,乙中产生的气体在标准状况下的体积为___________ mL;C、D、G、H极中质量增加的是___________ 极,丙中两极质量变化的绝对值的关系是___________ (填标号)。
a.G极变化大 b.H极变化大 c.两极变化一样大 d.无法确定
 胶粒带正电荷]。
胶粒带正电荷]。
(1)A为电源的
(2)若甲中装有100mL0.5

 溶液,工作一段时间后,
溶液,工作一段时间后, 恰好完全被消耗,停止通电,此时,测得溶液的pH=
恰好完全被消耗,停止通电,此时,测得溶液的pH=(3)通电后,E极的电极反应式为
(4)G和H极分别是
(5)若装置中的溶液都足量,当电路中有0.02mol电子转移时,乙中产生的气体在标准状况下的体积为
a.G极变化大 b.H极变化大 c.两极变化一样大 d.无法确定
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;AB为离子交换膜。
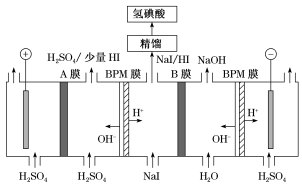
①B膜最佳应选择___________ 。
②阳极的电极反应式是___________ 。
③少量的I-因浓度差通过BPM膜,若撤去A膜,其缺点是___________ 。
(2)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚(C6H5OH)废水更加高效,装置如下图所示。已知a极主要发生的反应是O2生成H2O2,然后在电解液中产生·OH并迅速与苯酚反应。

①b极连接电源的___________ 极(填“正”或“负”)。
②a极的电极反应式为___________ 。
③除电极反应外,电解液中主要发生的反应方程式有___________ 。
(1)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;AB为离子交换膜。

①B膜最佳应选择
②阳极的电极反应式是
③少量的I-因浓度差通过BPM膜,若撤去A膜,其缺点是
(2)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚(C6H5OH)废水更加高效,装置如下图所示。已知a极主要发生的反应是O2生成H2O2,然后在电解液中产生·OH并迅速与苯酚反应。

①b极连接电源的
②a极的电极反应式为
③除电极反应外,电解液中主要发生的反应方程式有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】用NaCl做原料可以得到多种产品。
(1)工业上由NaCl制备金属钠的化学方程式是______________ 。
(2)实验室用惰性电极电解100mL 0.1mol/LNaCl溶液。写出阳极的电极反应方程式:_______________ 。
(3)某学生想制作一种家用环保型消毒液发生器,用石墨做电极电解饱和NaCl溶液。为使Cl2被完全吸收,制得有较强杀菌能力的消毒液(“84消毒液”),设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是________ ;
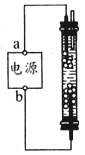
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极'b为阳极;HClO和NaCl
假设最后所得溶液中仅含一种溶质,则整个过程用一个化学方程式表示为:________________ 。
(1)工业上由NaCl制备金属钠的化学方程式是
(2)实验室用惰性电极电解100mL 0.1mol/LNaCl溶液。写出阳极的电极反应方程式:
(3)某学生想制作一种家用环保型消毒液发生器,用石墨做电极电解饱和NaCl溶液。为使Cl2被完全吸收,制得有较强杀菌能力的消毒液(“84消毒液”),设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是

A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极'b为阳极;HClO和NaCl
假设最后所得溶液中仅含一种溶质,则整个过程用一个化学方程式表示为:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】认真观察下列装置,回答下列问题:
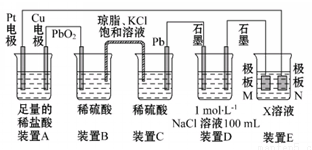
(1)装置B中PbO2上发生的电极反应为____________________________ 。
(2)装置A中总反应的离子方程式为______________________________ 。
(3)若装置E的目的是在铜上镀银,则X为____ ,极板N的材料为____ 。
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为____ (标准状况)。

(1)装置B中PbO2上发生的电极反应为
(2)装置A中总反应的离子方程式为
(3)若装置E的目的是在铜上镀银,则X为
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某同学设计了如下燃料电池,并探究氯碱工业原理的相关问题(其中乙装置中为正离子交换膜)。

(1)乙中石墨电极(C)作___________ 极。若丙中W为 溶液,且滴有酚酞,当实验开始后观察到的现象是
溶液,且滴有酚酞,当实验开始后观察到的现象是_______________________ 。
(2)若消耗2.24L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为___________ L。
(3)若丙中以 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 。
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 。
(4)若丙中以稀 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜。则该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜。则该电极反应式为___________________ 。
(5)假设乙装置中氯化钠溶液足够多,且装置中X为正离子交换膜,则反应后左侧溶液质量将___________ (填“增大”“减小”或“不变”)。

(1)乙中石墨电极(C)作
 溶液,且滴有酚酞,当实验开始后观察到的现象是
溶液,且滴有酚酞,当实验开始后观察到的现象是(2)若消耗2.24L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为
(3)若丙中以
 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 。
溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 。| A.b电极为粗铜 | B.粗铜接电源正极,发生还原反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 | D.利用阳极泥可回收Ag、Pt、Au等金属 |
(4)若丙中以稀
 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜。则该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜。则该电极反应式为(5)假设乙装置中氯化钠溶液足够多,且装置中X为正离子交换膜,则反应后左侧溶液质量将
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
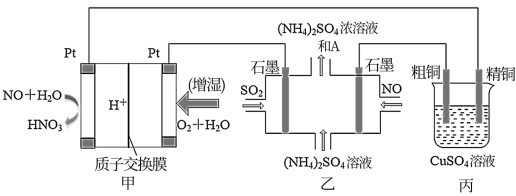
(1)燃料电池放电过程中正极的电极反应式________ 。
(2)乙装置中物质A是________ (填化学式),该装置电解过程阴极的电极反应式________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将________ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有________ mol;丙装置中阴极析出的质量为________ g。
 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
(1)燃料电池放电过程中正极的电极反应式
(2)乙装置中物质A是
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有
您最近半年使用:0次



