海洋是资源的宝库,蕴藏着丰富的氯、溴、碘等元素。氯、溴、碘是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素;卤素单质都具有氧化性。
(1)氯在元素周期表中的位置___________
(2)氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2.写出该电解过程的离子方程式___________
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为: 。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式
。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式___________ 。
(4)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应: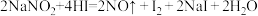
Ⅰ.上述反应的还原剂是___________
Ⅱ.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有___________ (填字母)。
A.③⑤ B.①②⑤ C.①②④
Ⅲ.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是___________ 。(填字母)
A.NaCl B. C.
C. D.浓
D.浓
(1)氯在元素周期表中的位置
(2)氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2.写出该电解过程的离子方程式
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为:
 。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式
。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式(4)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
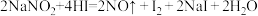
Ⅰ.上述反应的还原剂是
Ⅱ.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有
A.③⑤ B.①②⑤ C.①②④
Ⅲ.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是
A.NaCl B.
 C.
C. D.浓
D.浓
更新时间:2024/01/19 09:41:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下列反应均有氢氧化钠生成。回答下列问题:
①Na2O+H2O=2NaOH;
②2Na2O2+2H2O=4NaOH+O2↑;
③2Na+2H2O=2NaOH+H2↑;
④NaH+H2O=NaOH+H2↑。
(1)O2与O3互为__ 。
(2)不属于氧化还原反应的是__ (填方程式序号,下同),同一元素发生氧化还原反应的是__ 。
(3)根据②可推断Na2O2的用途为__ 。
(4)将③改为离子方程式:__ 。
(5)反应④中氧化剂是__ (填化学式,下同),还原产物是__ 。
(6)配平下面这个方程式:__ 。
H2S+ HNO3(浓)= S+ NO2+ H2O
①Na2O+H2O=2NaOH;
②2Na2O2+2H2O=4NaOH+O2↑;
③2Na+2H2O=2NaOH+H2↑;
④NaH+H2O=NaOH+H2↑。
(1)O2与O3互为
(2)不属于氧化还原反应的是
(3)根据②可推断Na2O2的用途为
(4)将③改为离子方程式:
(5)反应④中氧化剂是
(6)配平下面这个方程式:
H2S+ HNO3(浓)= S+ NO2+ H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】数字化实验是化学研究的重要手段,某化学实验小组向 溶液中匀速滴加相同浓度的
溶液中匀速滴加相同浓度的 溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
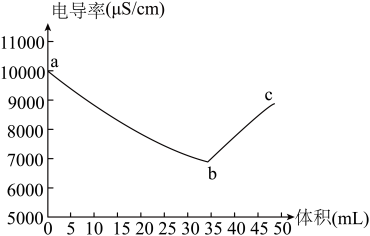
(1)用离子方程式解释图中a→b段曲线变化的原因:___________ 。
(2)对b、c两处溶液的氢离子浓度进行比较,b___________ c(选A表示“>”、B表示“=”或C表示“<”),说明原因___________ 。
(3)用等浓度的 溶液替换
溶液替换 溶液。则电导率最低点与图中b点的位置关系为___________。
溶液。则电导率最低点与图中b点的位置关系为___________。
 溶液中匀速滴加相同浓度的
溶液中匀速滴加相同浓度的 溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
溶液,测得溶液导电能力的变化如图所示:(电导率越大,溶液导电能力越强)。
(1)用离子方程式解释图中a→b段曲线变化的原因:
(2)对b、c两处溶液的氢离子浓度进行比较,b
(3)用等浓度的
 溶液替换
溶液替换 溶液。则电导率最低点与图中b点的位置关系为___________。
溶液。则电导率最低点与图中b点的位置关系为___________。| A.在b上方 | B.与b重合 | C.在b下方 | D.无法确定 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】2Al+Fe2O3 2Fe+Al2O3。氧化剂
2Fe+Al2O3。氧化剂___ ;还原剂___ ;氧化产物___ ;还原产物___ 。
 2Fe+Al2O3。氧化剂
2Fe+Al2O3。氧化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】有下列反应:
①Fe+CuSO4=Cu+FeSO4
②CaO+H2O=Ca(OH)2
③Ba(OH)2+H2SO4 =BaSO4↓+2H2O
④Zn+2HCl=ZnCl2+H2↑
⑤2KClO3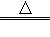 2KCl+3O2↑
2KCl+3O2↑
⑥CaCO3 CaO+CO2↑
CaO+CO2↑
⑦2CO+O2 2CO2
2CO2
⑧SO42-+Ba2+=BaSO4↓
(1)反应①中,氧化剂是______________________ 。
(2)反应③的离子反应方程式为_________________________________________ 。
(3)写出一个符合⑧的化学反应方程式___________________________________ 。
①Fe+CuSO4=Cu+FeSO4
②CaO+H2O=Ca(OH)2
③Ba(OH)2+H2SO4 =BaSO4↓+2H2O
④Zn+2HCl=ZnCl2+H2↑
⑤2KClO3
 2KCl+3O2↑
2KCl+3O2↑ ⑥CaCO3
 CaO+CO2↑
CaO+CO2↑⑦2CO+O2
 2CO2
2CO2 ⑧SO42-+Ba2+=BaSO4↓
(1)反应①中,氧化剂是
(2)反应③的离子反应方程式为
(3)写出一个符合⑧的化学反应方程式
您最近一年使用:0次
【推荐3】回答下列问题
(1)已知:KClO3+NH4NO2→KCl+NH4NO3
①以上反应中的氧化剂是___________ ,被氧化的元素是___________ 。
②用化合价升降法配平上述反应方程式___________ 。
(2)有些发达城市用ClO2代替氯气给自来水消毒,已知ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O。
2ClO2↑+K2SO4+2CO2↑+2H2O。
①请用双线桥法标出上述反应电子转移的方向及数目___________ 。
②产生1molClO2时,转移的电子的物质的量为___________ mol;1molKClO3参加反应时,生成标况下的气体体积为___________ L。
③上述反应中,氧化剂是___________ ,还原剂是___________ ;氧化产物是___________ ,还原产物是___________ 。
(1)已知:KClO3+NH4NO2→KCl+NH4NO3
①以上反应中的氧化剂是
②用化合价升降法配平上述反应方程式
(2)有些发达城市用ClO2代替氯气给自来水消毒,已知ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4
 2ClO2↑+K2SO4+2CO2↑+2H2O。
2ClO2↑+K2SO4+2CO2↑+2H2O。①请用双线桥法标出上述反应电子转移的方向及数目
②产生1molClO2时,转移的电子的物质的量为
③上述反应中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某小组同学欲探究 的性质,经历如下探究过程:
的性质,经历如下探究过程:
聚焦 中的O作为核心元素,进行如下预测:
中的O作为核心元素,进行如下预测:
① 有氧化性 ②
有氧化性 ② 有还原性 ③
有还原性 ③ 既有氧化性又有还原性
既有氧化性又有还原性
(1)预测其具有氧化性的思路是______ .
实验和观察:
小组同学分别选用酸性溶液、酸化的KI溶液与5% 溶液反应以验证预测.
溶液反应以验证预测.______ (填“氧化性”或者“还原性”),该实验中,证明 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有______ .
(3)实验②是为了验证 的
的______ (填“氧化性”或者“还原性”),在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式______ .
(4)综合以上实验,可得出的结论是:______ .
 的性质,经历如下探究过程:
的性质,经历如下探究过程:聚焦
 中的O作为核心元素,进行如下预测:
中的O作为核心元素,进行如下预测:①
 有氧化性 ②
有氧化性 ② 有还原性 ③
有还原性 ③ 既有氧化性又有还原性
既有氧化性又有还原性(1)预测其具有氧化性的思路是
实验和观察:
小组同学分别选用酸性溶液、酸化的KI溶液与5%
 溶液反应以验证预测.
溶液反应以验证预测.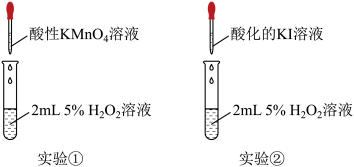
 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有(3)实验②是为了验证
 的
的(4)综合以上实验,可得出的结论是:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】高铁酸钠(Na2FeO4)能有效杀灭水中的病菌,同时自身被还原为新生态的 Fe(OH)3,这是一种品质优 良的无机絮凝剂,能高效除去水中的微粒悬浮物,从氧化还原角度分析,杀灭细菌充分利用了其强_____ (“氧化性”或“还原性”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】近日,中国科学院深圳先进技术研究院某研究团队发现,二维铜铟磷硫(CuInP2S6)能作纳米药物,用于未来安全有效的抗SARS-CoV-2治疗,以降低SARS-CoV-2的传染性。
请回答下列问题:
(1)中国科学院张青莲院士主持测定的铟(49In)元素的相对原子质量的新值已被采用为国际新标准。已知铟与铷同周期,则In在元素周期表中的位置为______ ;其最高价氧化物能用于金属反射镜面的保护涂层、光电显示半导体薄膜,则铟元素的最高价氧化物的化学式为______ 。
(2)已知Cu2O在酸性条件下易歧化,据此写出Cu2O与稀硫酸反应的离子方程式:____________ 。
(3)磷、硫元素的最高价氧化物对应水化物的酸性由强到弱的顺序为______ (用化学式表示),结合元素周期律解释其原因:____________ 。
(4)已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测正确的是______ (填序号)。
a.含有离子键和共价键
b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
请回答下列问题:
(1)中国科学院张青莲院士主持测定的铟(49In)元素的相对原子质量的新值已被采用为国际新标准。已知铟与铷同周期,则In在元素周期表中的位置为
(2)已知Cu2O在酸性条件下易歧化,据此写出Cu2O与稀硫酸反应的离子方程式:
(3)磷、硫元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测正确的是
a.含有离子键和共价键
b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,根据表中给出10种元素(其中X、Y分别代表某种化学元素),按要求作答。
(1)X、Y两种元素符号分别是___________ 和___________ ;
(2)最外层电子数为4的原子,其元素符号是___________ ;
(3)某阴离子结构示意图为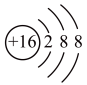 ,该离子符号是
,该离子符号是___________ ;
(4)C与N原子半径较小的是___________ ;
(5)保存在煤油中的金属是___________ ;
(6)化学性质最不活泼的单质是___________ ;
(7)HF与HCl热稳定性较强的是___________ ;
(8) 与
与 酸性较强的是
酸性较强的是___________ ;NaOH与 碱性较弱的是
碱性较弱的是___________ ;
(9)写出Y元素组成的单质与氧气反应的化学方程式:___________ 。
周期 族 | IA | IIA | ⅢA | IVA | VA | ⅥA | ⅦA | O |
| 2 | C | N | X | F | Ne | |||
| 3 | Na | Mg | Y | S | Cl |
(1)X、Y两种元素符号分别是
(2)最外层电子数为4的原子,其元素符号是
(3)某阴离子结构示意图为
 ,该离子符号是
,该离子符号是(4)C与N原子半径较小的是
(5)保存在煤油中的金属是
(6)化学性质最不活泼的单质是
(7)HF与HCl热稳定性较强的是
(8)
 与
与 酸性较强的是
酸性较强的是 碱性较弱的是
碱性较弱的是(9)写出Y元素组成的单质与氧气反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】请根据下图中的信息回答问题。
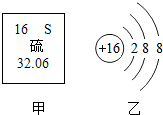
(1)硫属于________ (填“金属”或“非金属”)元素;硫元素的原子序数为_________ 。
(2)图乙所表示粒子的化学符号是____________ 。
(3)硫在空气中燃烧的化学方程式为____________________ 。

(1)硫属于
(2)图乙所表示粒子的化学符号是
(3)硫在空气中燃烧的化学方程式为
您最近一年使用:0次



