含氯消毒剂会与水中有机物发生氯代反应,生成物会在人体内积留产生慢性累积中毒,诱发癌症,而 ClO2 是国际上公认的最理想的更换替代产品,我国从2000年起就逐渐用它取代了其它含氯消毒剂。市面上销售的二氧化氯消毒片都是二氧化氯的前体:亚氯酸钠,亚氯酸钠溶液与酸、有机物、还原剂或者氯供体接触,将会发生反应生成二氧化氯气体。
(1)亚氯酸钠溶液和盐酸反应产生ClO2的化学方程式为___________ 。
(2)此反应中氧化剂与还原剂的物质的量之比为____ ,反应中盐酸的作用是____ (填编号)。
A.只有还原性 B.还原性和酸性 C.只有酸性 D.氧化性和酸性
(3)将二氧化氯通入含 CN-的废水中,产生两种对环境友好的气体,氯被还原成最低价离子,发生反应的离子方程式为______ 。
(4)(CN)2、(OCN)2、(SCN)2 等通称为拟卤素,它们的性质与卤素相似,氧化性强弱顺序是:F2>(OCN)2>Cl2>(CN)2>(SCN)2>I2,下列方程式中错误的是____(填编号)。
(5)在ClO2的制备方法中,有下列两种制备方法:
方法 1:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法 2:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O:
①分析方法1的化学反应方程式,用双线桥标出电子转移方向和数目______ ,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
②方法2在实际制备过程中,NaClO3与H2O2的物质的量之比小于2,可能的原因是______ 。
③用方法2制备的ClO2更适合用于饮用水的消毒,其主要原因是_______ 。
(6)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的 ,其含量应不超过0.2mg/L,可用FeCl2溶液处理饮用水中残留的
,其含量应不超过0.2mg/L,可用FeCl2溶液处理饮用水中残留的 ,反应后的溶液中可以产生丁达尔现象,写出反应的离子方程式
,反应后的溶液中可以产生丁达尔现象,写出反应的离子方程式_________ 。
(7)饮用水中的ClO2、 含量可用连续碘量法进行测定。ClO2被I-还原为
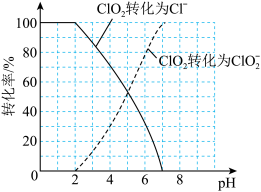
含量可用连续碘量法进行测定。ClO2被I-还原为 、Cl-的转化率与溶液pH的关系如图所示,当pH≤2.0时,
、Cl-的转化率与溶液pH的关系如图所示,当pH≤2.0时, 也能被I-完全还原为Cl-,反应生成的I-的量可以用已知浓度的Na2S2O3溶液来确定:2Na2S2O3+I2=Na2S4O6+2NaI。
也能被I-完全还原为Cl-,反应生成的I-的量可以用已知浓度的Na2S2O3溶液来确定:2Na2S2O3+I2=Na2S4O6+2NaI。
①请写出pH≤2.0时 与I-反应的离子方程式:
与I-反应的离子方程式:_________ 。
②请完成相应的实验步骤:
步骤 1:准确量取V mL水样加入到锥形瓶中;
步骤 2:调节水样的pH为7.0~8.0;
步骤 3:加入足量的KI晶体,充分反应后,滴入少量淀粉溶液,溶液显蓝色;
步骤 4:当加入的c mol/LNa2S2O3溶液体积为V1 mL,恰好完全反应,溶液蓝色恰好褪去;
步骤 5:_____ ,溶液再次显蓝色;
步骤 6:当加入的 c mol/L Na2S2O3 溶液体积达到 V2 mL,溶液蓝色恰好再次褪去。
③根据上述分析数据,测得该饮用水中 的浓度为
的浓度为_______ mol/L(用含字母的代数式表示)。
(1)亚氯酸钠溶液和盐酸反应产生ClO2的化学方程式为
(2)此反应中氧化剂与还原剂的物质的量之比为
A.只有还原性 B.还原性和酸性 C.只有酸性 D.氧化性和酸性
(3)将二氧化氯通入含 CN-的废水中,产生两种对环境友好的气体,氯被还原成最低价离子,发生反应的离子方程式为
(4)(CN)2、(OCN)2、(SCN)2 等通称为拟卤素,它们的性质与卤素相似,氧化性强弱顺序是:F2>(OCN)2>Cl2>(CN)2>(SCN)2>I2,下列方程式中错误的是____(填编号)。
| A.2NaSCN+MnO2+2H2SO4=Na2SO4+(SCN)2↑+MnSO4+2H2O |
| B.(CN)2+2KI=2KCN+I2 |
| C.Cl2+2NaOCN= (OCN)2+2NaCl |
| D.2AgCN=2Ag+(CN)2 |
(5)在ClO2的制备方法中,有下列两种制备方法:
方法 1:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法 2:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O:
①分析方法1的化学反应方程式,用双线桥标出电子转移方向和数目
②方法2在实际制备过程中,NaClO3与H2O2的物质的量之比小于2,可能的原因是
③用方法2制备的ClO2更适合用于饮用水的消毒,其主要原因是
(6)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的
 ,其含量应不超过0.2mg/L,可用FeCl2溶液处理饮用水中残留的
,其含量应不超过0.2mg/L,可用FeCl2溶液处理饮用水中残留的 ,反应后的溶液中可以产生丁达尔现象,写出反应的离子方程式
,反应后的溶液中可以产生丁达尔现象,写出反应的离子方程式(7)饮用水中的ClO2、
 含量可用连续碘量法进行测定。ClO2被I-还原为
含量可用连续碘量法进行测定。ClO2被I-还原为 、Cl-的转化率与溶液pH的关系如图所示,当pH≤2.0时,
、Cl-的转化率与溶液pH的关系如图所示,当pH≤2.0时, 也能被I-完全还原为Cl-,反应生成的I-的量可以用已知浓度的Na2S2O3溶液来确定:2Na2S2O3+I2=Na2S4O6+2NaI。
也能被I-完全还原为Cl-,反应生成的I-的量可以用已知浓度的Na2S2O3溶液来确定:2Na2S2O3+I2=Na2S4O6+2NaI。
①请写出pH≤2.0时
 与I-反应的离子方程式:
与I-反应的离子方程式:②请完成相应的实验步骤:
步骤 1:准确量取V mL水样加入到锥形瓶中;
步骤 2:调节水样的pH为7.0~8.0;
步骤 3:加入足量的KI晶体,充分反应后,滴入少量淀粉溶液,溶液显蓝色;
步骤 4:当加入的c mol/LNa2S2O3溶液体积为V1 mL,恰好完全反应,溶液蓝色恰好褪去;
步骤 5:
步骤 6:当加入的 c mol/L Na2S2O3 溶液体积达到 V2 mL,溶液蓝色恰好再次褪去。
③根据上述分析数据,测得该饮用水中
 的浓度为
的浓度为
更新时间:2024-01-19 12:33:15
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】已知:4NH3+5O2 4NO+6H2O,4NO+3O2+2H2O→4HNO3
4NO+6H2O,4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80。
(1)amolNO完全转化为HNO3理论上需要氧气___ mol。
(2)为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数___ (用小数表示)为(保留2位小数)。
(3)20.0molNH3用空气氧化,产生混合物的组成为:NO18.0mol、O212.0mol、N2150.0mol和一定量硝酸,以及其他成分(高温下NO与O2不化合)。计算氨转化为NO和HNO3的总转化率___ 。
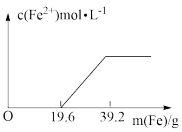
(4)20.0molNH3和一定量空气充分反应后,再转化为硝酸。通过计算,在图中画出HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线___ 。

 4NO+6H2O,4NO+3O2+2H2O→4HNO3
4NO+6H2O,4NO+3O2+2H2O→4HNO3设空气中氧气的体积分数为0.20,氮气的体积分数为0.80。
(1)amolNO完全转化为HNO3理论上需要氧气
(2)为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数
(3)20.0molNH3用空气氧化,产生混合物的组成为:NO18.0mol、O212.0mol、N2150.0mol和一定量硝酸,以及其他成分(高温下NO与O2不化合)。计算氨转化为NO和HNO3的总转化率
(4)20.0molNH3和一定量空气充分反应后,再转化为硝酸。通过计算,在图中画出HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】将128g铜置于一定量的浓硝酸中并微热。当铜片完全消失时,共收集到NO2和NO的混合气体44.8L(标准状况下)。
(1)写出上述过程中,有关反应的离子方程式______________ 、_____________ 。
(2)完成该反应至少需要量取10mol/L的浓硝酸__________ mL。
(3)混合气体中NO2的体积为__________ L,NO的体积为__________ L(均为标准状况下)。
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的O2的物质的量为____________ mol。
(1)写出上述过程中,有关反应的离子方程式
(2)完成该反应至少需要量取10mol/L的浓硝酸
(3)混合气体中NO2的体积为
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的O2的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】实验室可用氯酸钾和浓盐酸反应来制取氯气,反应方程式如下:KClO3 + 6HCl(浓)== KCl + 3Cl2↑+ 3H2O
(1)该反应中发生还原反应的物质是__________ 。氧化产物是___________ 。
(2)当有0.2mol电子发生转移时,生成的氯气的体积为________ L(标准状况)。被氧化的HCl的物质的量为______ mol。
(3)将生成的氯气通入到石灰乳中,当两者恰好反应时,可制得漂白粉_________ g。
(1)该反应中发生还原反应的物质是
(2)当有0.2mol电子发生转移时,生成的氯气的体积为
(3)将生成的氯气通入到石灰乳中,当两者恰好反应时,可制得漂白粉
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】危化仓库中往往存有钠、钾、硫、白磷(P4)、硝酸铵和氰化钠(NaCN)等危险品。请回答下列问题:
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3 =4N2 ↑+ 2HNO3 + 9H2O
则被氧化和被还原的氮元素质量之比为_____________ ;
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂:1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为______________ mol;
(3)NaCN属于剧毒物质,有一种处理方法其原理为:CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色弱电解质,另一种与H+作用产生能使品红溶液腿色的刺激性气体,写出离子反应方程式:_________________________________ 。
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3 =4N2 ↑+ 2HNO3 + 9H2O
则被氧化和被还原的氮元素质量之比为
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂:1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为
(3)NaCN属于剧毒物质,有一种处理方法其原理为:CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色弱电解质,另一种与H+作用产生能使品红溶液腿色的刺激性气体,写出离子反应方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】完成下列问题
(1)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O 被还原为Cr3+。样品中CuCl的质量分数为
被还原为Cr3+。样品中CuCl的质量分数为_______ 。
(2)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2 沉淀,密封静置,加入适量稀H2SO4,待MnO(OH)2 与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:O2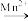 MnO(OH)2
MnO(OH)2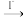 I2
I2 S4O
S4O 。O2将Mn2+氧化成MnO(OH)2的离子方程式:
。O2将Mn2+氧化成MnO(OH)2的离子方程式:_______ 。取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水样的溶解氧,消耗0.010 00 mol·L-1 Na2S2O3标准溶液13.50 mL。该水样中的溶解氧_______ (以mg·L-1表示)。
(3)某铁的氧化物(FexO)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112 mL Cl2,恰好将Fe2+完全氧化。x值为_______ 。
(4)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_______ 。联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是_______ 。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1 kg的联氨可除去水中溶解的O2_______ kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是_______ 。
(1)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O
 被还原为Cr3+。样品中CuCl的质量分数为
被还原为Cr3+。样品中CuCl的质量分数为(2)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2 沉淀,密封静置,加入适量稀H2SO4,待MnO(OH)2 与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:O2
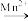 MnO(OH)2
MnO(OH)2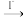 I2
I2 S4O
S4O 。O2将Mn2+氧化成MnO(OH)2的离子方程式:
。O2将Mn2+氧化成MnO(OH)2的离子方程式:(3)某铁的氧化物(FexO)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112 mL Cl2,恰好将Fe2+完全氧化。x值为
(4)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】现取一定量的硫酸酸化的硫酸锰( )溶液,向其中依次加入下列试剂,对应的现象如下表所示:
)溶液,向其中依次加入下列试剂,对应的现象如下表所示:
已知:①金属铋(Bi)价态为+3价时较稳定, 无色;
无色;
②铋酸钠( )无色,难溶于水;
)无色,难溶于水;
③淀粉溶液遇到 变成蓝色。
变成蓝色。
(1)由上述现象可得 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ ;
(2)根据上述结论,请写出 与硫酸锰溶液在酸性条件下反应的离子方程式
与硫酸锰溶液在酸性条件下反应的离子方程式___________ ;
(3)硫酸酸化的 溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:
溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:_________

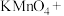



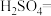



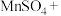

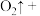

___________
(4)软锰矿的主要成分为 ,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中
,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中 和FeS发生反应,化学方程式为
和FeS发生反应,化学方程式为 。
。
①该反应中,氧化剂是___________ ,氧化产物是___________ 。
②用双线桥法标出该反应的电子转移情况:___________ 。
③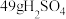 参加反应时转移电子的个数为
参加反应时转移电子的个数为___________ 。
 )溶液,向其中依次加入下列试剂,对应的现象如下表所示:
)溶液,向其中依次加入下列试剂,对应的现象如下表所示:| 试剂 | 少量铋酸钠 | 过量的双氧水 | 适量KI—淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
 无色;
无色;②铋酸钠(
 )无色,难溶于水;
)无色,难溶于水;③淀粉溶液遇到
 变成蓝色。
变成蓝色。(1)由上述现象可得
 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)根据上述结论,请写出
 与硫酸锰溶液在酸性条件下反应的离子方程式
与硫酸锰溶液在酸性条件下反应的离子方程式(3)硫酸酸化的
 溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:
溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:
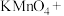



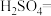



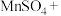

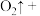

(4)软锰矿的主要成分为
 ,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中
,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中 和FeS发生反应,化学方程式为
和FeS发生反应,化学方程式为 。
。①该反应中,氧化剂是
②用双线桥法标出该反应的电子转移情况:
③
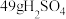 参加反应时转移电子的个数为
参加反应时转移电子的个数为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)写出下列反应的离子方程式。
①酸性KMnO4溶液和草酸(H2C2O4)溶液反应_____ 。
②硫代硫酸钠与稀硫酸反应_____ 。
③用硫氰化钾溶液检验Fe3+_____ 。
(2)利用电解技术,以氯化氢为原料回收氯气的过程如图所示,回答下列问题:H+由_____ 极区向_____ 极区迁移(填阴、阳);阳极电极反应式:____ ;阴极电极反应式:______ 。
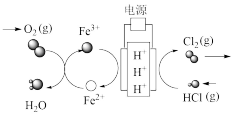
(3)燃料种类很多,如氢氧燃料电池(如KOH为电解液)。写出该电池电极反应式正极:______ ;负极:_____ 。
(4)氯碱工业原理的化学方程式:______ 。如图为用阳离子交换膜法进行该工业生产的装置示意图,标出a~f处所对应的原料或产品:_____ 。

生成0.4kg烧碱时,转移电子的物质的量是____ mol。(相对原子质量Na-23、H-1、O-16)
①酸性KMnO4溶液和草酸(H2C2O4)溶液反应
②硫代硫酸钠与稀硫酸反应
③用硫氰化钾溶液检验Fe3+
(2)利用电解技术,以氯化氢为原料回收氯气的过程如图所示,回答下列问题:H+由
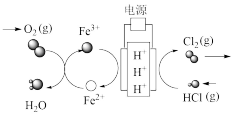
(3)燃料种类很多,如氢氧燃料电池(如KOH为电解液)。写出该电池电极反应式正极:
(4)氯碱工业原理的化学方程式:

生成0.4kg烧碱时,转移电子的物质的量是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1) 利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g) △H1=44.0 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H4
则△H4=_______ kJ·mol-1。
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
① 写出该反应的离子方程式:________ 。
② 在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:________ ;为抑制肼的分解,可采取的合理措施有________ (任写一种)。
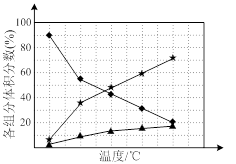
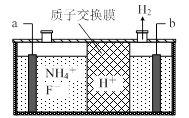
图1 图2
(3)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
① 氮化硅的化学式为___________________ 。
② a电极为电解池的_____________ (填“阴”或“阳”)极,写出该电极的电极反应式:________________ ;电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是_______________ 。
(1) 利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g) △H1=44.0 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H4
则△H4=
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
① 写出该反应的离子方程式:
② 在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:


图1 图2
(3)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
① 氮化硅的化学式为
② a电极为电解池的
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】DCCNa(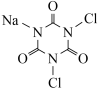 )是一种高效、安全的消毒杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。实验室利用NaClO溶液和氰尿酸(
)是一种高效、安全的消毒杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。实验室利用NaClO溶液和氰尿酸( )溶液反应制备DCCNa,实验装置如图所示:
)溶液反应制备DCCNa,实验装置如图所示:

已知: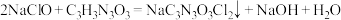
回答下列问题:
(1)仪器a的名称为______ 。
(2)装置A中发生的离子反应方程式为______ 。
(3)实验发现装置B中NaOH溶液的利用率较低,改进方法是______ 。
(4)当装置B的三颈烧瓶内液面上方有黄绿色气体时,再加入氰尿酸溶液。并在整个过程中不断通入一定量的氯气,其原因是______ 。
(5)实验过程中B的温度必须保持为7~12℃,pH控制在6.5~8.5的范围。若温度过高,pH过低, 在溶液中会与
在溶液中会与 发生副反应生成
发生副反应生成 和
和 等,写出该副反应的化学方程式:
等,写出该副反应的化学方程式:______ 。
(6)装置C的试剂可选用______ (填标号)。
a. b.NaCl c.
b.NaCl c. d。
d。
(7)反应结束后,装置B中的浊液经过滤、______ 、干燥得DCCNa粗产品。
 )是一种高效、安全的消毒杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。实验室利用NaClO溶液和氰尿酸(
)是一种高效、安全的消毒杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。实验室利用NaClO溶液和氰尿酸( )溶液反应制备DCCNa,实验装置如图所示:
)溶液反应制备DCCNa,实验装置如图所示:
已知:
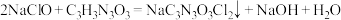
回答下列问题:
(1)仪器a的名称为
(2)装置A中发生的离子反应方程式为
(3)实验发现装置B中NaOH溶液的利用率较低,改进方法是
(4)当装置B的三颈烧瓶内液面上方有黄绿色气体时,再加入氰尿酸溶液。并在整个过程中不断通入一定量的氯气,其原因是
(5)实验过程中B的温度必须保持为7~12℃,pH控制在6.5~8.5的范围。若温度过高,pH过低,
 在溶液中会与
在溶液中会与 发生副反应生成
发生副反应生成 和
和 等,写出该副反应的化学方程式:
等,写出该副反应的化学方程式:(6)装置C的试剂可选用
a.
 b.NaCl c.
b.NaCl c. d。
d。
(7)反应结束后,装置B中的浊液经过滤、
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】化学工业为疫情防控提供了强有力的物质支撑。次氯酸溶液是常用的消毒剂,可利用Cl2O与水反应得到。根据该原理,某化学兴趣小组利用如下装置制备一定浓度的次氯酸溶液。已知:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42℃以上会分解为Cl2和O2。实验时,将氯气和空气(不参与反应)按体积比为1:3混合通入含水8%的碳酸钠糊状物中,请回答下列问题:
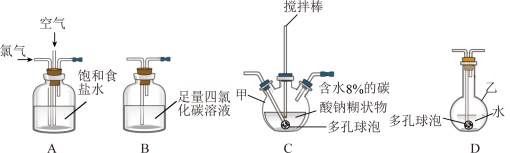
(1)实验室一般通过MnO2与浓盐酸加热制备氯气,发生反应的离子方程式为_______ 。
(2)装置C中的仪器甲的名称为_______ ,仪器甲中发生反应的化学方程式为_______ ,为了提高 的产率,需控制反应在合适的温度,可采取的操作为
的产率,需控制反应在合适的温度,可采取的操作为_______ 。
(3)装置 的作用为
的作用为_______ ,有同学建议将装置 中的仪器乙换为棕色瓶,原因是
中的仪器乙换为棕色瓶,原因是_______ 。
(4)测定装置D中得到的次氯酸的物质的量浓度。量取 装置D中得到的次氯酸溶液,并稀释至
装置D中得到的次氯酸溶液,并稀释至 ,再从中取出
,再从中取出 至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (滴定反应为
(滴定反应为 )。
)。
①次氯酸与KI溶液反应时氧化剂与还原剂的物质的量之比为_______ 。
②达到滴定终点的现象为_______ 。
③装置D中得到的次氯酸的物质的量浓度为_______ mol/L。
④若滴定开始前滴定管尖嘴有气泡,滴定结束后气泡消失,则测定的次氯酸的物质的量浓度将_______ (填“偏低”、“偏高”或“无影响”)。

(1)实验室一般通过MnO2与浓盐酸加热制备氯气,发生反应的离子方程式为
(2)装置C中的仪器甲的名称为
 的产率,需控制反应在合适的温度,可采取的操作为
的产率,需控制反应在合适的温度,可采取的操作为(3)装置
 的作用为
的作用为 中的仪器乙换为棕色瓶,原因是
中的仪器乙换为棕色瓶,原因是(4)测定装置D中得到的次氯酸的物质的量浓度。量取
 装置D中得到的次氯酸溶液,并稀释至
装置D中得到的次氯酸溶液,并稀释至 ,再从中取出
,再从中取出 至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (滴定反应为
(滴定反应为 )。
)。①次氯酸与KI溶液反应时氧化剂与还原剂的物质的量之比为
②达到滴定终点的现象为
③装置D中得到的次氯酸的物质的量浓度为
④若滴定开始前滴定管尖嘴有气泡,滴定结束后气泡消失,则测定的次氯酸的物质的量浓度将
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式:_____________________ 。
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
15.8gKMnO4能氧化_______ molHCl,产生的Cl2在标准状况下的体积为_____ L。
(2)常温下,氯气与烧碱溶液反应得84消毒液,NaClO是84消毒液的有效成分,在抗击新型冠状病毒中发挥了重要作用。浸泡衣物时加入84消毒液在空气中放置一段时间漂白效果更好,原因用离子方程式表示:____________________________ (已知酸性:H2CO3>HClO> )。
)。
(3)某温度下,将aL(已换算成标况体积)氯气通入由24gNaOH配成的溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与 的个数比为1:3。
的个数比为1:3。
①a=______ L;
②写出该反应的化学方程式:______________________________ 。
(1)①写出实验室中制取氯气的离子方程式:
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
15.8gKMnO4能氧化
(2)常温下,氯气与烧碱溶液反应得84消毒液,NaClO是84消毒液的有效成分,在抗击新型冠状病毒中发挥了重要作用。浸泡衣物时加入84消毒液在空气中放置一段时间漂白效果更好,原因用离子方程式表示:
 )。
)。(3)某温度下,将aL(已换算成标况体积)氯气通入由24gNaOH配成的溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与
 的个数比为1:3。
的个数比为1:3。①a=
②写出该反应的化学方程式:
您最近一年使用:0次