W、X、Y、Z、Q、R是核电荷数依次增大的六种短周期主族元素。W的一种核素可用于考古,X原子的最外层电子数是其内层电子数的3倍,Y在短周期元素中金属性最强,Z是地壳中含量最多的金属元素,Q与X同主族。
请回答下列问题:
(1)W的元素名称为___________ ,R的元素符号为___________ 。
(2)X、Y、Z、Q的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)W、X、Q的最简单氢化物中,沸点最高的是___________ (用化学式表示),原因是___________ 。
(4)将R的单质通入Y2Q溶液中能够证明R的非金属性强于Q的,请写出该反应的化学方程式:___________ 。
(5)向Y2WX3溶液中滴加少量稀H2SO4,发生反应的离子方程式为___________ 。
(6)Z的氧化物能与R的最高价氧化物对应的水化物反应,该反应的离子方程式为___________ 。
请回答下列问题:
(1)W的元素名称为
(2)X、Y、Z、Q的简单离子半径由大到小的顺序为
(3)W、X、Q的最简单氢化物中,沸点最高的是
(4)将R的单质通入Y2Q溶液中能够证明R的非金属性强于Q的,请写出该反应的化学方程式:
(5)向Y2WX3溶液中滴加少量稀H2SO4,发生反应的离子方程式为
(6)Z的氧化物能与R的最高价氧化物对应的水化物反应,该反应的离子方程式为
更新时间:2024-01-24 15:57:28
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。完成下列填空:

(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol·L-1),需要的玻璃仪器有___________
(2)上述装置中,A是___________ 溶液,其作用是___________ 。
(3)上述装置中,B物质是___________ 。
(4)一次性饭盒中石蜡和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
①从物质分类的角度分析,石蜡属于有机物中的____________ 类,为了将石蜡从饭盒中溶出,应选用下列试剂中的__________ 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d 正己烷
②饭盒中的碳酸钙常用稀醋酸将其溶出,试写出其反应的离子方程式__________ 。

(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol·L-1),需要的玻璃仪器有
(2)上述装置中,A是
(3)上述装置中,B物质是
(4)一次性饭盒中石蜡和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
①从物质分类的角度分析,石蜡属于有机物中的
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d 正己烷
②饭盒中的碳酸钙常用稀醋酸将其溶出,试写出其反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】已知实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2+2H2O,据此回答下列问题;
MnCl2+Cl2+2H2O,据此回答下列问题;
(1)MnO2+4HCl(浓) MnCl2+Cl2+2H2O,用双线桥法表示电子转移的方向和数目:
MnCl2+Cl2+2H2O,用双线桥法表示电子转移的方向和数目:_______ 。
(2)有一种“地康法”制取氯气的反应原理如下所示:

①反应Ⅰ的离子方程式为_______ 。
②反应Ⅱ属于_______ 反应。(填四种基本反应类型之一)
(3)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为_______ (填化学式)。将少量金属钠投入到硫酸铜溶液中发生反应的离子方程式_______ 。
 MnCl2+Cl2+2H2O,据此回答下列问题;
MnCl2+Cl2+2H2O,据此回答下列问题;(1)MnO2+4HCl(浓)
 MnCl2+Cl2+2H2O,用双线桥法表示电子转移的方向和数目:
MnCl2+Cl2+2H2O,用双线桥法表示电子转移的方向和数目:(2)有一种“地康法”制取氯气的反应原理如下所示:

①反应Ⅰ的离子方程式为
②反应Ⅱ属于
(3)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铝土矿是工业上制备金属铝的主要原料,其主要成分是 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题。(提示:
,其工业流程如图所示。根据图示信息,请回答下列问题。(提示: 不与稀盐酸反应)
不与稀盐酸反应)
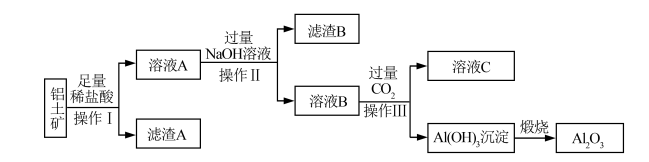
(1)操作I的名称是_______ ,写出溶液A中加入过量NaOH溶液生成溶液B的离子方程式_______ ,滤渣B的主要成分是_______ (填化学式)。
(2)写出溶液B中通入过量 产生沉淀的离子方程式是
产生沉淀的离子方程式是_______ ,该步骤中_______ (填“能”或“不能”)改用盐酸代替通入 ,原因是
,原因是_______ 。
(3)实验室中进行煅烧时最适合用来盛放 固体的实验仪器名称是
固体的实验仪器名称是_______ 。
(4)用 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是_______ 。
(5)工业上通过电解熔融氧化铝制备金属铝时,常用石墨作电极,但其在电解过程中易损耗需要定期更换,原因是_______ 。
 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题。(提示:
,其工业流程如图所示。根据图示信息,请回答下列问题。(提示: 不与稀盐酸反应)
不与稀盐酸反应)
(1)操作I的名称是
(2)写出溶液B中通入过量
 产生沉淀的离子方程式是
产生沉淀的离子方程式是 ,原因是
,原因是(3)实验室中进行煅烧时最适合用来盛放
 固体的实验仪器名称是
固体的实验仪器名称是(4)用
 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是(5)工业上通过电解熔融氧化铝制备金属铝时,常用石墨作电极,但其在电解过程中易损耗需要定期更换,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y和Z都是元素周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为W2Y的化合物;
②Y 和Z属同族元素,他们能形成两种常见化合物;
③X和Z属同一周期元素,他们能形成两种气态化合物;
④W和Z能形成组成为W2Z和W2Z2的化合物;
⑤X和Y不在同一周期,他们能形成组成为XY2的化合物。请回答:
(1)Y元素名称是___________ 。
(2)用一方程式证明Y与X非金属性的强弱___________ ,证明Y与Z非金属性的强弱___________ 。
(3)标准状况22.4LXZ2通过足量的W2Z2时,转移的电子数是___________ ,W2Z2的质量将增加___________ g。
(4)观察W元素的焰色的操作注意事项___________ 。
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为W2Y的化合物;
②Y 和Z属同族元素,他们能形成两种常见化合物;
③X和Z属同一周期元素,他们能形成两种气态化合物;
④W和Z能形成组成为W2Z和W2Z2的化合物;
⑤X和Y不在同一周期,他们能形成组成为XY2的化合物。请回答:
(1)Y元素名称是
(2)用一方程式证明Y与X非金属性的强弱
(3)标准状况22.4LXZ2通过足量的W2Z2时,转移的电子数是
(4)观察W元素的焰色的操作注意事项
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,请回答下列问题:
(1)元素⑩在周期表中的位置是_______ ;⑦的原子结构示意图为_______ ;
(2)④⑤⑥的简单离子半径由小到大的顺序为_______ (用离子符号和“<”表示);
(3)②③的简单气态氢化物中沸点高的是_______ (用化学式表示);
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式_______ ;
(5)下列五种物质中,① ②
② ③
③ ④
④ ⑤
⑤ ,只存在共价键的是
,只存在共价键的是_______ ;只存在离子键的是_______ ;既存在离子键又存在共价键的是_______ (填序号)。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑩ |
(2)④⑤⑥的简单离子半径由小到大的顺序为
(3)②③的简单气态氢化物中沸点高的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)下列五种物质中,①
 ②
② ③
③ ④
④ ⑤
⑤ ,只存在共价键的是
,只存在共价键的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】如表是元素周期表的一部分,回答下列有关问题:
(1)写出⑥的元素符号:_______ ,画出⑨的原子结构示意图_______ 。
(2)写出③的单质在空气中燃烧后产物的电子式:_______ 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ ,呈两性氢氧化物的是_______ 。(填化学式)
(4)用电子式表示出④的氯化物的形成过程:_______ 。
(5)写出实验室制取⑧的单质的化学方程式:_______ 。
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)写出③的单质在空气中燃烧后产物的电子式:
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)用电子式表示出④的氯化物的形成过程:
(5)写出实验室制取⑧的单质的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、X、D、E、Y为短周期元素,原子序数依次增大,有关信息如表中所示:
(1)六种元素中原子半径最大的是_______ ( 填元素符号)。
(2)A在周期表中的位置是_______ 。
(3)A和B的最简单氢化物中较稳定的是_______ (填化学式)。
(4)B、X以原子个数比为1:1组成的化合物W,常用于呼吸面具中做供氧剂。写出W的电子式_______ ,其所含化学键的类型为_______ 。
(5)D的氧化物与X的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(6)Y的最高价氧化物对应的水化物的化学式为_______ 。
(7)下列说法中能证明Y的非金属性强于E的是_______( 填字母)。
| A | 一种同位素常用于文物年代的测定 |
| B | 最外层电子数是电子层数的3倍 |
| X | M层有1个电子,单质需保存在煤油中 |
| D | 地壳中含量最多的金属元素 |
| E | 与B可形成EB2和EB3两种物质,EB2是形成酸雨的主要物质 |
| Y | 单质可用于生产漂白液、漂白粉 |
(2)A在周期表中的位置是
(3)A和B的最简单氢化物中较稳定的是
(4)B、X以原子个数比为1:1组成的化合物W,常用于呼吸面具中做供氧剂。写出W的电子式
(5)D的氧化物与X的最高价氧化物对应的水化物反应的离子方程式是
(6)Y的最高价氧化物对应的水化物的化学式为
(7)下列说法中能证明Y的非金属性强于E的是_______( 填字母)。
| A.E的单质在常温下为固体而Y的单质为气体 |
| B.与Fe反应时,Y的单质能生成高价铁化合物,E的单质只能生成低价铁化合物 |
| C.简单气态氢化物的稳定性:Y>E |
| D.H2EO3的酸性弱于HYO3 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】锂离子电池是目前广泛应用的二次电池。由于锂资源储量有限,科学家将目光转向钾离子电池。
(1) 用作钾离子电池的电解液溶剂,可由
用作钾离子电池的电解液溶剂,可由 与有机物X经加成反应得到。
与有机物X经加成反应得到。
① 中碳原子杂化方式为
中碳原子杂化方式为_______ 。
②X的结构简式为_______ 。
(2)由于离子半径:
_______  (填“>”或“<”),在充、放电过程中,
(填“>”或“<”),在充、放电过程中, 的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。
的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。
(3)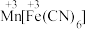 可用作钾离子电池的正极材料,其晶胞结构如下图所示。
可用作钾离子电池的正极材料,其晶胞结构如下图所示。

①距离 最近的
最近的 有
有_______ 个。
②第三电离能 :
: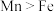 ,结合原子结构解释原因:
,结合原子结构解释原因:_______ 。
③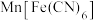 放电后转化为
放电后转化为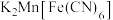 ,充电时物质的变化如下:
,充电时物质的变化如下: 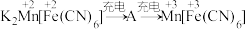 。充电时生成A的电极反应式:
。充电时生成A的电极反应式:_______ (请标注A中 和
和 的化合价)。
的化合价)。
(1)
 用作钾离子电池的电解液溶剂,可由
用作钾离子电池的电解液溶剂,可由 与有机物X经加成反应得到。
与有机物X经加成反应得到。①
 中碳原子杂化方式为
中碳原子杂化方式为②X的结构简式为
(2)由于离子半径:

 (填“>”或“<”),在充、放电过程中,
(填“>”或“<”),在充、放电过程中, 的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。
的嵌入、脱出会破坏锂离子电池正极材料的结构,应研发新的正极材料。(3)
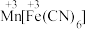 可用作钾离子电池的正极材料,其晶胞结构如下图所示。
可用作钾离子电池的正极材料,其晶胞结构如下图所示。
①距离
 最近的
最近的 有
有②第三电离能
 :
: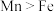 ,结合原子结构解释原因:
,结合原子结构解释原因:③
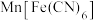 放电后转化为
放电后转化为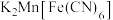 ,充电时物质的变化如下:
,充电时物质的变化如下: 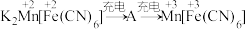 。充电时生成A的电极反应式:
。充电时生成A的电极反应式: 和
和 的化合价)。
的化合价)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z 是原子序数依次增大的同一短周期主族元素,W、X是金属元素,它们的最高价氧化物对应的水化物可以反应生成盐和水,Y、Z 是非金属元素。
(1)W 与 Y 可形成化合物 W2Y,该化合物在溶液中与氯气发生反应的离子方程式为_______ 。
(2)Y 的低价氧化物通入 Z 单质的水溶液中,发生反应的化学方程式为_______ 。
(3)比较 Y、Z 气态氢化物的稳定性:_______ >_______ (用化学式表示)。
(4)W、X、Y、Z 四种元素简单离子的离子半径由大到小的顺序是_______ >_______ >_______ >_______ 。
(5)Z 的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,写出该反应的化学方程式:_______ 。
(1)W 与 Y 可形成化合物 W2Y,该化合物在溶液中与氯气发生反应的离子方程式为
(2)Y 的低价氧化物通入 Z 单质的水溶液中,发生反应的化学方程式为
(3)比较 Y、Z 气态氢化物的稳定性:
(4)W、X、Y、Z 四种元素简单离子的离子半径由大到小的顺序是
(5)Z 的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,写出该反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D为短周期元素,核电荷数依次增大,且 A、B、C三种元素的原子核外电子层数之和为5。已知 A 是原子结构最简单的元素;B元素原子最外层的电子数是其电子层数的2倍;A 和C之间可形成 A2C和 A2C2 两种化合物;D 在同周期主族元素中原子半径最大。请回答下列问题:
(1)C元素在元素周期表中的位置是_________ ;写出BC2的电子式:______ 。
(2)C、D两种元素所形成的简单离子,半径由大到小的顺序是____________ 。(用离子符号表示)
(3)在恒温下,体积为2L 的恒容容器中加入一定量的B单质和1mol A2C蒸气,发生:B(s)+A2C(g)⇌BC(g)+A2(g)。2min后,容器的压强增加了20%,则2min内 A2C的平均反应速率为_____ mol/(L·min)。一段时间后达到平衡,下列说法正确的是___________ 。
A.增加B单质的量,反应速率加快
B.恒温恒容时在该容器中通入 Ar,反应速率加快
C.各气体的浓度不再变化可以判断该反应达到了平衡
D.2min时,A2C的转化率为80%
(4)BA4与C2在DCA 溶液中可形成一种燃料电池。该电池的负极反应式为:____ 。
(5)写出D的单质与乙醇反应的化学方程式:_________ 。
(1)C元素在元素周期表中的位置是
(2)C、D两种元素所形成的简单离子,半径由大到小的顺序是
(3)在恒温下,体积为2L 的恒容容器中加入一定量的B单质和1mol A2C蒸气,发生:B(s)+A2C(g)⇌BC(g)+A2(g)。2min后,容器的压强增加了20%,则2min内 A2C的平均反应速率为
A.增加B单质的量,反应速率加快
B.恒温恒容时在该容器中通入 Ar,反应速率加快
C.各气体的浓度不再变化可以判断该反应达到了平衡
D.2min时,A2C的转化率为80%
(4)BA4与C2在DCA 溶液中可形成一种燃料电池。该电池的负极反应式为:
(5)写出D的单质与乙醇反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素X、Y、Z、D与第Ⅷ族元素E的信息如表:
回答下列问题:
(1)X在元素周期表中的位置为______ ;Z的氢化物电子式为_____ 。
(2)Y、Z的最高价氧化物对应的水化物酸性较强的是______ (填化学式)。X、Y、D形成的简单离子的半径由大到小的顺序为______ (用离子符号表示)。
(3)D的最高价氧化物对应的水化物与强碱反应的离子方程式为______ 。
(4)E元素与Y元素可形成EY2和EY3两种化合物,下列说法不正确的是_____ (填序号)。
①保存EY2溶液时,需向溶液中加入少量E单质
②EY2、EY3均只能通过化合反应生成
③铁片、碳棒和EY3溶液可组成原电池,电子由铁片沿导线流向碳棒
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物既能溶于强酸又能溶于强碱 |
| E | 单质是生活中常见金属,其中一种氧化物具有磁性 |
(1)X在元素周期表中的位置为
(2)Y、Z的最高价氧化物对应的水化物酸性较强的是
(3)D的最高价氧化物对应的水化物与强碱反应的离子方程式为
(4)E元素与Y元素可形成EY2和EY3两种化合物,下列说法不正确的是
①保存EY2溶液时,需向溶液中加入少量E单质
②EY2、EY3均只能通过化合反应生成
③铁片、碳棒和EY3溶液可组成原电池,电子由铁片沿导线流向碳棒
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】在A、B、C、D、E五种短周期元素中,A、B、C三种元素的原子序数依次增大,A、C都能与B按原子个数比为1:1或2:1形成化合物,但常温时A、B形成的化合物呈液态,C、B形成的化合物呈固态。D的原子最外层电子数最多,E的核电荷数最大,D与E能形成气态物质ED4 。
(1)五种元素原子半径从大到小的顺序是______________________ (填元素符号);
(2)A与B形成的化合物中,含非极性键的化合物的结构式为_______________ ;
(3)C与B按原子个数比为1:1形成化合物的电子式是_______ ,ED4的电子式是______ ;
(4)D、E所形成氢化物的稳定性由强到弱的顺序是_______________ (填具体的化学式);
(5)由短周期元素组成的微粒,如,SO2、O3、NO ,可互称为等电子体,则与B、D同周期元素组成的微粒中,能与N
,可互称为等电子体,则与B、D同周期元素组成的微粒中,能与N 、CS2互称为等电子体的微粒是
、CS2互称为等电子体的微粒是____________ (填二种符合要求微粒的名称)。
(1)五种元素原子半径从大到小的顺序是
(2)A与B形成的化合物中,含非极性键的化合物的结构式为
(3)C与B按原子个数比为1:1形成化合物的电子式是
(4)D、E所形成氢化物的稳定性由强到弱的顺序是
(5)由短周期元素组成的微粒,如,SO2、O3、NO
 ,可互称为等电子体,则与B、D同周期元素组成的微粒中,能与N
,可互称为等电子体,则与B、D同周期元素组成的微粒中,能与N 、CS2互称为等电子体的微粒是
、CS2互称为等电子体的微粒是
您最近一年使用:0次



