A—E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质,C是常见的碱。
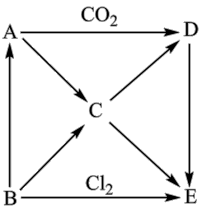
(1)B在氯气中燃烧的现象是____________________ 。
(2)写出下列反应的离子方程式
①单质B投入水中______________________________ 。
②D的饱和溶液中通
____________________ 。
(3)下列说法不正确的是(不定项选择)__________ 。
a.物质E是工业生产物质D的一种原料
b.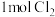 与物质C充分反应,转移
与物质C充分反应,转移 电子
电子
c.氯减工业的产品包括 和物质C
和物质C
d.A→D的反应是氧化还原反应
e.检验D物质所含的金属元素,可用玻璃棒蘸取少量D,在酒精灯外焰上灼烧

(1)B在氯气中燃烧的现象是
(2)写出下列反应的离子方程式
①单质B投入水中
②D的饱和溶液中通

(3)下列说法不正确的是(不定项选择)
a.物质E是工业生产物质D的一种原料
b.
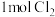 与物质C充分反应,转移
与物质C充分反应,转移 电子
电子c.氯减工业的产品包括
 和物质C
和物质Cd.A→D的反应是氧化还原反应
e.检验D物质所含的金属元素,可用玻璃棒蘸取少量D,在酒精灯外焰上灼烧
更新时间:2024-01-29 09:26:27
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】市政污泥含大量金属(Cu、Zn、Ni、Fe、Ag等),不经处理直接填埋会对环境造成严重的污染。市政污泥的综合利用能够使其得到科学、妥善的处置,并可以作为资源再次被我们利用,同时可以带来一定的经济价值。某科研团队利用市政污泥回收皓矾(ZnSO4·7H2O)的工艺流程如下:

已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有_______ (任写一条)。
(2)“一系列操作”主要包括_______ 、_______ 、过滤、洗涤,干燥。
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为_______ 。
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:_______ ,则反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为_______ 。

已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)“一系列操作”主要包括
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有NaHCO3、CuCl2、Ca(OH)2、HNO3中的一种。某中学环保小组对河水检测时发现:①甲处河水无色,可以使紫色石蕊变红,②乙处产生气泡,河水仍清,③往丙处河水通入过量的 CO2先变浑浊再变澄清,④丁处河水呈蓝色,⑤M 处水样的 pH 大于 7。请判断:

(1)四座工厂排出的废液里含有的污染物:甲_________ ,乙 ________ ,丙__________ ,丁________ 。
(2)写出乙、丁两处发生反应的离子方程式:
乙:____________________ 丁:_______________________ 。
(3)M 处取出的河水中,肯定大量存在的离子是________________________ 。

(1)四座工厂排出的废液里含有的污染物:甲
(2)写出乙、丁两处发生反应的离子方程式:
乙:
(3)M 处取出的河水中,肯定大量存在的离子是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含碑废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如下。

已知:I. ;
;
Ⅱ.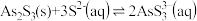 ;
;
Ⅲ.砷酸(H3AsO4)在酸性条件下有强氧化性,能被SO2、碘化钾等还原。
(1)“沉砷”过程中FeS是否可以用过量的Na2S替换:_______ (填“是”或“否”);请从平衡移动的角度解释原因:_______ 。
(2)向滤液Ⅱ中加入NaClO进行“氧化脱硫”,请写出脱硫的离子反应方程式:_______ 。
(3)欲检验“还原”后溶液中的砷酸,则还需要的实验试剂或试纸为_______ 。
(4)已知:H3AsO4第三步电离方程式 的电离常数为Ka3,则pKa3=
的电离常数为Ka3,则pKa3=_______ (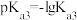 )。常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。当溶液pH介于3~5之间时,吸附剂对五价砷的平衡吸附量随pH的升高而增大,试分析其原因:
)。常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。当溶液pH介于3~5之间时,吸附剂对五价砷的平衡吸附量随pH的升高而增大,试分析其原因:_______ 。


已知:I.
 ;
;Ⅱ.
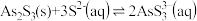 ;
;Ⅲ.砷酸(H3AsO4)在酸性条件下有强氧化性,能被SO2、碘化钾等还原。
(1)“沉砷”过程中FeS是否可以用过量的Na2S替换:
(2)向滤液Ⅱ中加入NaClO进行“氧化脱硫”,请写出脱硫的离子反应方程式:
(3)欲检验“还原”后溶液中的砷酸,则还需要的实验试剂或试纸为
(4)已知:H3AsO4第三步电离方程式
 的电离常数为Ka3,则pKa3=
的电离常数为Ka3,则pKa3=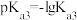 )。常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。当溶液pH介于3~5之间时,吸附剂对五价砷的平衡吸附量随pH的升高而增大,试分析其原因:
)。常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。当溶液pH介于3~5之间时,吸附剂对五价砷的平衡吸附量随pH的升高而增大,试分析其原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A为常见的金属单质,根据如图所示的关系,回答下列问题。

(1)A为______ ,B为______ 。
(2)C→D溶液的颜色变化为________________________________ 。
(3)⑤的离子方程式为_________________________________ 。
(4)⑧的化学方程式为_________________________________ 。

(1)A为
(2)C→D溶液的颜色变化为
(3)⑤的离子方程式为
(4)⑧的化学方程式为
您最近一年使用:0次
【推荐2】为探究某固体化合物X(仅合两种元素)的组成和性质,设计并完成如图实验,请回答:

(1)X中的非金属元素是___ ;能使品红溶液褪色体现了无色气体___ 性质。
(2)黑色化合物 红棕色化合物的化学方程式是
红棕色化合物的化学方程式是___ 。
(3)设计实验方案检验黄色溶液中的金属阳离子___ 。

(1)X中的非金属元素是
(2)黑色化合物
 红棕色化合物的化学方程式是
红棕色化合物的化学方程式是(3)设计实验方案检验黄色溶液中的金属阳离子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】利用氯元素价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①~⑩均含氯元素。回答下列问题:

(1)③的化学式__________ 。
(2)⑥的电离方程式__________ 。
(3)“84消毒液”是常用含氯消毒剂,其有效成分是图中物质⑨,“84消毒液”不可与洁厕灵(主要成分稀盐酸)混合使用的原因是__________ (用离子方程式说明)。
(4)若将①通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为15:1时,混合液中
的个数比为15:1时,混合液中 和
和 的个数比为
的个数比为__________ 。
(5)含⑩的溶液可与盐酸反应生成气体①、③和⑧,反应的化学方程式为__________ 。

(1)③的化学式
(2)⑥的电离方程式
(3)“84消毒液”是常用含氯消毒剂,其有效成分是图中物质⑨,“84消毒液”不可与洁厕灵(主要成分稀盐酸)混合使用的原因是
(4)若将①通入热的烧碱溶液中,可以得到NaCl、NaClO和
 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为15:1时,混合液中
的个数比为15:1时,混合液中 和
和 的个数比为
的个数比为(5)含⑩的溶液可与盐酸反应生成气体①、③和⑧,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知有以下物质相互转化,其中A为常见金属,C为碱。
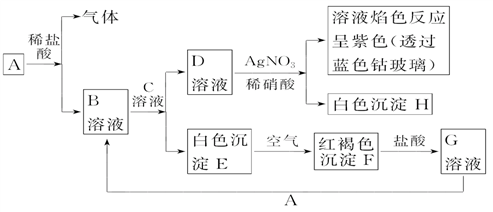
试回答:
(1)写出F的化学式________ ,H的化学式___________________________________ 。
(2)写出由E转变成F的化学方程式:________________________________ 。
(3)向G溶液加入A的有关反应离子方程式:________________________________________ 。
(4)写出A在一定条件下与水反应的化学方程式:_________________________________ 。

试回答:
(1)写出F的化学式
(2)写出由E转变成F的化学方程式:
(3)向G溶液加入A的有关反应离子方程式:
(4)写出A在一定条件下与水反应的化学方程式:
您最近一年使用:0次
【推荐2】植物(草本和木本植物)燃烧后的残余物,称草木灰。草木灰中含有可溶性钾盐(主要成分是K2SO4、K2CO3、KCl)。某学生按下列操作提取草木灰中的钾盐①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
(1)在①②③④的操作中需要用到玻璃棒的是___ (填序号)。
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
(3)由草木灰提取钾盐并检验钾元素存在的下列实验操作中,错误的___ 。
A.溶解 B.过滤
B.过滤 C.蒸发
C.蒸发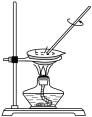 D.
D.
(4)步骤Ⅲ所得的结论,你认为是否正确?___ (填“是”或“否”);如果错应该如何改进(如果正解说明理由):___ 。
(1)在①②③④的操作中需要用到玻璃棒的是
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
| 实验步骤 | 实验现象 | 实验结论 |
Ⅰ.取第一份溶液和适量加入下列装置的试管中,把澄清的石灰水加入烧杯中 | 证明含有碳酸根离子 | |
| Ⅱ.取第二份溶液,先滴加 | 证明含有硫酸根离子 | |
| Ⅲ.取第三份溶液加入过量Ba(NO3)2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有氯离子 |
| Ⅳ.取第四份溶液进行焰色反应 | 透过蓝色钴玻璃火焰呈 | 证明含有K+ |
A.溶解
 B.过滤
B.过滤 C.蒸发
C.蒸发 D.
D.
(4)步骤Ⅲ所得的结论,你认为是否正确?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行):
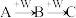
Ⅰ.若A为有刺激性气味的气体,水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
(1)A的电子式为___ 。
(2)A的催化氧化反应的化学方程式为__ 。
Ⅱ.若A、C、W都是常见气体,C是导致酸雨的主要气体,常温下A与C反应生成B,
(1)A与C反应生成B的化学方程式为___ 。
(2)某化学活动小组将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:___ 。
Ⅲ.A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。则C的化学式为___ 。
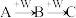
Ⅰ.若A为有刺激性气味的气体,水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
(1)A的电子式为
(2)A的催化氧化反应的化学方程式为
Ⅱ.若A、C、W都是常见气体,C是导致酸雨的主要气体,常温下A与C反应生成B,
(1)A与C反应生成B的化学方程式为
(2)某化学活动小组将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:
Ⅲ.A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。则C的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】将一小快金属钠投入到盛放FeCl2溶液的烧杯中,观察到的现象是__________________ 有关的离子方程式是______ 、_____ 、________ 。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】用如图装置(气密性好)研究Na与 的反应。
的反应。
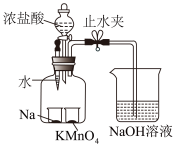
实验步骤:
①将一定量浓盐酸滴在 粉末上,立即产生黄绿色气体。
粉末上,立即产生黄绿色气体。
②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
回答下列问题:
(1)步骤①,黄绿色气体是 ,则
,则 的作用是
的作用是_______ (填“氧化剂”或“还原剂”)。
(2)步骤③引起钠燃烧的原因是_______ 。
(3)写出生成白色固体的电子式_______ 。
(4)右侧烧杯中发生反应的离子方程式为_______ 。
 的反应。
的反应。
实验步骤:
①将一定量浓盐酸滴在
 粉末上,立即产生黄绿色气体。
粉末上,立即产生黄绿色气体。②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
回答下列问题:
(1)步骤①,黄绿色气体是
 ,则
,则 的作用是
的作用是(2)步骤③引起钠燃烧的原因是
(3)写出生成白色固体的电子式
(4)右侧烧杯中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】I.某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
请你帮助该同学整理并完成实验报告:
实验目的:探究同周期元素的金属性和非金属性的递变规律。
实验用品:
仪器:①试管 ②酒精灯 ③胶头滴管 ④试管夹⑤镊子⑥小刀⑦玻璃片⑧砂纸 ⑨烧杯等。
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、饱和的H2S溶液等。
(1)实验内容:(填写与实验方案相对应的实验现象)
①________ ②________ ③________ ④________ ⑤________ (用A-E表示)
写出③的离子方程式_____________________________________ 。
(2)实验结论:________________________________________ 。
Ⅱ. 实验室利用如图装置进行中和热的测定,请回答下列问题:
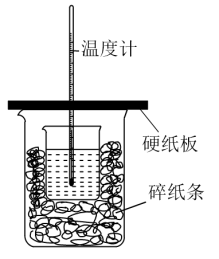
(3)从实验装置上看,图中尚缺少一种玻璃仪器是______________________ 。
(4)做1次完整的中和热测定实验,温度计需使用__________________ 次。
(5)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?____________________________________ 。
| 实验方案 | 实验现象 |
| ①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 | (B)产生气体,可在空气中燃烧,溶液变成浅红色 |
| ③钠与滴有酚酞试液的冷水反应 | (C)反应不十分强烈,产生的气体可以在空气中燃烧 |
| ④镁带与2 mol·L-1的盐酸反应 | (D)剧烈反应,产生可燃性气体 |
| ⑤铝条与2 mol·L-1的盐酸反应 | (E) 生成淡黄色沉淀 |
实验目的:探究同周期元素的金属性和非金属性的递变规律。
实验用品:
仪器:①试管 ②酒精灯 ③胶头滴管 ④试管夹⑤镊子⑥小刀⑦玻璃片⑧砂纸 ⑨烧杯等。
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、饱和的H2S溶液等。
(1)实验内容:(填写与实验方案相对应的实验现象)
①
写出③的离子方程式
(2)实验结论:
Ⅱ. 实验室利用如图装置进行中和热的测定,请回答下列问题:

(3)从实验装置上看,图中尚缺少一种玻璃仪器是
(4)做1次完整的中和热测定实验,温度计需使用
(5)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?
您最近一年使用:0次



