Ⅰ.实验室用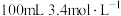 的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中
的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中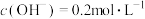 ,
, 和
和 的物质的量浓度之比为
的物质的量浓度之比为 。(不考虑反应前后溶液的体积变化)。
。(不考虑反应前后溶液的体积变化)。
(1)吸收氯气所消耗的氢氧化钠物质的量为__________ 。
(2)被氧化与被还原的氯气的物质的量之比为__________ 。
Ⅱ.无水 与
与 作用会生成
作用会生成 。现有
。现有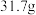 无水
无水 ,吸收
,吸收 后变成
后变成 ,试回答下列问题:
,试回答下列问题:
(3) 中
中
__________ 。
(4) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到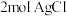 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为__________ 。
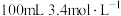 的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中
的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中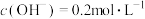 ,
, 和
和 的物质的量浓度之比为
的物质的量浓度之比为 。(不考虑反应前后溶液的体积变化)。
。(不考虑反应前后溶液的体积变化)。(1)吸收氯气所消耗的氢氧化钠物质的量为
(2)被氧化与被还原的氯气的物质的量之比为
Ⅱ.无水
 与
与 作用会生成
作用会生成 。现有
。现有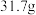 无水
无水 ,吸收
,吸收 后变成
后变成 ,试回答下列问题:
,试回答下列问题:(3)
 中
中
(4)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到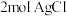 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为
更新时间:2024-01-30 22:26:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】向Ba(OH)2溶液中先滴加一定量CuSO4溶液,直至沉淀质量为m克,再不断滴加H2SO4溶液。整个过程中,产生沉淀的质量与加入溶液的质量关系如图所示。
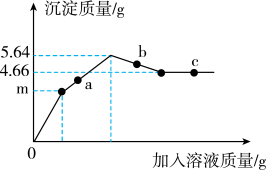
(1)a点对应溶液pH___________ (选填“>”、“=”或“<”)7。
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是___________ 。
(3)通过计算确定m的值___________ 。(写出计算过程)

(1)a点对应溶液pH
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是
(3)通过计算确定m的值
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】今有Fe与足量的稀盐酸反应共放出H2 8.96L(标准状况),求:反应中消耗HCl物质的量是多少______ (写出计算过程)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】已知反应PbS+O2 Pb+SO2。
Pb+SO2。
(1)请将上述反应用单线桥法标出电子转移的方向和数目:________________________________________
(2)上述反应的氧化剂是_________________ ,还原剂是_______________ ,氧化产物是________________ ,还原产物是_________________ 。
 Pb+SO2。
Pb+SO2。(1)请将上述反应用单线桥法标出电子转移的方向和数目:
(2)上述反应的氧化剂是
您最近一年使用:0次
【推荐2】在下列括号中填上系数,并完成相应空格:
(1)( ) CO + ( ) NO = ( ) N2 + ( ) CO2在此反应中属于氧化剂的是 _____ ,CO在反应中表现出 ____ 性。
(2)( ) ClO— + ( ) Fe3+ + 10 OH— = ( ) FeO +
+ ( ) Cl— + 5H2O在此反应中属于还原剂的是 _____ ,属于氧化产物的是 ____ 。
(1)
(2)
 +
+
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)铁元素是构成人体的必不可少的元素之一,缺铁会影响到人体的健康和发育,最大的影响是缺铁性贫血。此类病人需要服用补铁药品。

一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________ 。
A Fe B Fe2+ C e3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_________ 性。下列不能实现上述转化的物质是_________ 。
A Cl2 B O2 C FeCl3 D KMnO4(H+)
(3)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
①被氧化的元素是______ ,被还原的元素是________ ,发生氧化反应的物质是________ ,发生还原反应的物质是________ 。
②用双线桥法表示反应电子得失的方向和数目:_____________ 。
③请写出反应的离子方程式:__________
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了________ 性和________ 性,则生成1分子NO转移电子数为________ ;56 g Fe参加反应时,被还原的HNO3为________ g。

一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A Fe B Fe2+ C e3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A Cl2 B O2 C FeCl3 D KMnO4(H+)
(3)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
①被氧化的元素是
②用双线桥法表示反应电子得失的方向和数目:
③请写出反应的离子方程式:
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】Kraus用阴离子树脂交换法提取一种组成元素为氯和铍的阴离子,该阴离子内铍原子最外层达到8电子稳定结构,则该阴离子内存在的微粒间的作用力是_______ ,阴离子的结构式为_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】金属钛密度小、强度高、抗腐蚀性能好,是应用广泛的金属。含钛的矿石主要有金红石和钛铁矿。
(1)基态Ti原子的价层电子排布式为___________ ,含有未成对电子___________ 个,Ti元素在周期表中的位置是___________ 。
(2)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知 Ti3+的配位数为 6,TiCl3·4H2O 的化学式用配合物的形式表示为___________ 。
(1)基态Ti原子的价层电子排布式为
(2)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知 Ti3+的配位数为 6,TiCl3·4H2O 的化学式用配合物的形式表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】元素化学是化学的基石,不同的元素往往呈现不同的特性。回答下列问题:
(1)Sn为第五周期元素,与C同主族,基态Sn的价电子排布式为_______ 。
(2)已知 的熔点为1040℃,
的熔点为1040℃, 的熔点为194℃,分析其差异的原因:
的熔点为194℃,分析其差异的原因:_______ 。
(3)基态碳原子的核外电子有_______ 种不同的运动状态。
(4)检验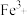 时,
时, 以S原子配位而不以N原子配位的原因是
以S原子配位而不以N原子配位的原因是_______ 。
(5)碳酰肼的结构为 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。
①碳酰肼中氮原子的杂化轨道类型为_______ 。
② 碳酰肼中含有的
碳酰肼中含有的 键数目为
键数目为_______  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(6)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有_______ (填字母)。 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键
(1)Sn为第五周期元素,与C同主族,基态Sn的价电子排布式为
(2)已知
 的熔点为1040℃,
的熔点为1040℃, 的熔点为194℃,分析其差异的原因:
的熔点为194℃,分析其差异的原因:(3)基态碳原子的核外电子有
(4)检验
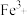 时,
时, 以S原子配位而不以N原子配位的原因是
以S原子配位而不以N原子配位的原因是(5)碳酰肼的结构为
 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。①碳酰肼中氮原子的杂化轨道类型为
②
 碳酰肼中含有的
碳酰肼中含有的 键数目为
键数目为 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(6)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有

 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键
您最近一年使用:0次



