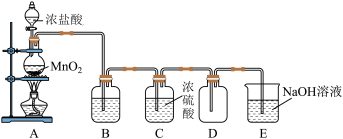
已知实验室常用二氧化锰粉末和浓盐酸制取氯气,其反应的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,某实验小组用下图所示装置制取纯净干燥的氯气。
MnCl2+Cl2↑+2H2O,某实验小组用下图所示装置制取纯净干燥的氯气。
请回答下列问题:
(1)B是除杂装置,盛放的试剂是___________ (填“饱和食盐水”或“饱和NaHCO3溶液”)。
(2)该制取过程中,收集氯气的方法是___________ (填“A”或“B”)。
A.向下排空气法 B.向上排空气法
(3)为防止Cl2污染环境,E烧杯中盛装冷的NaOH溶液,请写出该反应的化学方程式___________ 。
(4)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为___________ g。(写出计算过程)
 MnCl2+Cl2↑+2H2O,某实验小组用下图所示装置制取纯净干燥的氯气。
MnCl2+Cl2↑+2H2O,某实验小组用下图所示装置制取纯净干燥的氯气。
请回答下列问题:
(1)B是除杂装置,盛放的试剂是
(2)该制取过程中,收集氯气的方法是
A.向下排空气法 B.向上排空气法
(3)为防止Cl2污染环境,E烧杯中盛装冷的NaOH溶液,请写出该反应的化学方程式
(4)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为
更新时间:2024-02-01 12:55:45
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】用含砷氧化铜矿[含CuO、Cu2(OH)2CO3、As2O3及重金属盐等]制取Cu2(OH)2SO4的工艺流程如下:

(1) 步骤Ⅰ“氨浸”时,控制温度为50~55 ℃,pH约为9.5,含铜化合物转化为[Cu(NH3)4]SO4溶液。
① CuO被浸取的离子方程式为________ 。
②浸取温度不宜超过55 ℃,其原因是________ 。
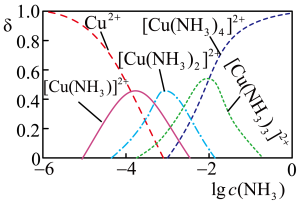
③ Cu2+与NH3结合时,溶液中含铜微粒的物质的量分布分数(δ)与溶液中游离的c(NH3)的对数值的关系如图所示。若用1 L浸取液(由等物质的量NH3和NH4+组成)将amolCu2(OH)2CO3全部浸出为[Cu(NH3)4]2+(CO32-转变为HCO3-,不考虑其他反应,溶液体积变化忽略不计),原浸取液中起始时c(NH3)应满足的条件是________ 。
(2) “除AsO2-”时,FeSO4需过量,一方面使AsO2-沉淀完全,另一目的是________ 。
(3) “蒸氨”时发生反应的化学方程式为________ 。
(4) 为了实现生产过程中物质循环利用,可采取的措施为________ 。

(1) 步骤Ⅰ“氨浸”时,控制温度为50~55 ℃,pH约为9.5,含铜化合物转化为[Cu(NH3)4]SO4溶液。
① CuO被浸取的离子方程式为
②浸取温度不宜超过55 ℃,其原因是
③ Cu2+与NH3结合时,溶液中含铜微粒的物质的量分布分数(δ)与溶液中游离的c(NH3)的对数值的关系如图所示。若用1 L浸取液(由等物质的量NH3和NH4+组成)将amolCu2(OH)2CO3全部浸出为[Cu(NH3)4]2+(CO32-转变为HCO3-,不考虑其他反应,溶液体积变化忽略不计),原浸取液中起始时c(NH3)应满足的条件是

(2) “除AsO2-”时,FeSO4需过量,一方面使AsO2-沉淀完全,另一目的是
(3) “蒸氨”时发生反应的化学方程式为
(4) 为了实现生产过程中物质循环利用,可采取的措施为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上以铝土矿(主要成分为 ,含少量
,含少量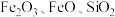 等杂质)为主要原料制备氧化铝,流程如下。
等杂质)为主要原料制备氧化铝,流程如下。

(1)“氧化”时发生反应的离子方程式是___________ 。
(2)“沉淀”时,逐滴滴加 溶液来调节总溶液的
溶液来调节总溶液的 ,目的是将
,目的是将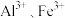 转化为
转化为 和
和 沉淀。溶液不同
沉淀。溶液不同 时对
时对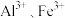 沉淀率的影响如图所示。为获得较高的铝、铁沉淀率,应控制溶液
沉淀率的影响如图所示。为获得较高的铝、铁沉淀率,应控制溶液 为
为___________ (填选项字母)。

A. B.
B. C.
C.
(3)“碱溶”时,加入足量 溶液的目的是
溶液的目的是___________ 。
(4)“碳分”时,向“碱溶”后的溶液中通入足量 气体,生成
气体,生成 沉淀和
沉淀和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(5)“碱溶”后分离得到的副产物 沉淀,可用于制备绿矾
沉淀,可用于制备绿矾 。
。
①由 沉淀先制备
沉淀先制备 溶液时,需向沉淀中加入试剂的化学式为
溶液时,需向沉淀中加入试剂的化学式为_______ (按照试剂顺序填写)。
②绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体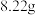 溶于稀盐酸后,加入足量的
溶于稀盐酸后,加入足量的 溶液,过滤得沉淀
溶液,过滤得沉淀 ;再通入
;再通入 (标准状况)氯气恰好将其中的
(标准状况)氯气恰好将其中的 完全氧化。为确定绿矾未被全部氧化,可选择的最佳试剂是
完全氧化。为确定绿矾未被全部氧化,可选择的最佳试剂是___________ (填选项字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
③请通过上述小题②中数据计算,得出所取绿矾晶体样品中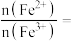
___________ 。
 ,含少量
,含少量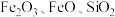 等杂质)为主要原料制备氧化铝,流程如下。
等杂质)为主要原料制备氧化铝,流程如下。
(1)“氧化”时发生反应的离子方程式是
(2)“沉淀”时,逐滴滴加
 溶液来调节总溶液的
溶液来调节总溶液的 ,目的是将
,目的是将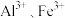 转化为
转化为 和
和 沉淀。溶液不同
沉淀。溶液不同 时对
时对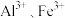 沉淀率的影响如图所示。为获得较高的铝、铁沉淀率,应控制溶液
沉淀率的影响如图所示。为获得较高的铝、铁沉淀率,应控制溶液 为
为
A.
 B.
B. C.
C.
(3)“碱溶”时,加入足量
 溶液的目的是
溶液的目的是(4)“碳分”时,向“碱溶”后的溶液中通入足量
 气体,生成
气体,生成 沉淀和
沉淀和 ,该反应的化学方程式为
,该反应的化学方程式为(5)“碱溶”后分离得到的副产物
 沉淀,可用于制备绿矾
沉淀,可用于制备绿矾 。
。①由
 沉淀先制备
沉淀先制备 溶液时,需向沉淀中加入试剂的化学式为
溶液时,需向沉淀中加入试剂的化学式为②绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体
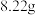 溶于稀盐酸后,加入足量的
溶于稀盐酸后,加入足量的 溶液,过滤得沉淀
溶液,过滤得沉淀 ;再通入
;再通入 (标准状况)氯气恰好将其中的
(标准状况)氯气恰好将其中的 完全氧化。为确定绿矾未被全部氧化,可选择的最佳试剂是
完全氧化。为确定绿矾未被全部氧化,可选择的最佳试剂是A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液③请通过上述小题②中数据计算,得出所取绿矾晶体样品中
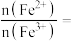
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁( ),进一步制备高纯度还原铁粉。
),进一步制备高纯度还原铁粉。

已知: 难溶于水;
难溶于水; 是二元弱酸,溶于水。
是二元弱酸,溶于水。
(1)步骤②中H2C2O4稍过量的目的是:_____________________ ;
(2)步骤②中得到FeC2O4.2H2O的离子反应方程式为:_________________________ 。
(3)实现步骤④,必须在______ (填仪器名称)中进行,该步骤发生的化学反应方程式为:______________
(4)为实现步骤⑤,不宜用碳粉直接还原Fe2O3,理由是________________________ 。
(5)若将固体 放在一个可称出质量的容器内加热,
放在一个可称出质量的容器内加热, ( Mr=180)首先逐步失去结晶水,温度继续升高时.
( Mr=180)首先逐步失去结晶水,温度继续升高时. (Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g
(Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g ,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
根据上述数据计算并推断:150℃剩余的固体物质是________________ (填化学式,下同);800℃剩余的固体物质是________________ 。
 ),进一步制备高纯度还原铁粉。
),进一步制备高纯度还原铁粉。
已知:
 难溶于水;
难溶于水; 是二元弱酸,溶于水。
是二元弱酸,溶于水。(1)步骤②中H2C2O4稍过量的目的是:
(2)步骤②中得到FeC2O4.2H2O的离子反应方程式为:
(3)实现步骤④,必须在
(4)为实现步骤⑤,不宜用碳粉直接还原Fe2O3,理由是
(5)若将固体
 放在一个可称出质量的容器内加热,
放在一个可称出质量的容器内加热, ( Mr=180)首先逐步失去结晶水,温度继续升高时.
( Mr=180)首先逐步失去结晶水,温度继续升高时. (Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g
(Mr=144)会逐渐转变为铁的各种氧化物。称取18.00g ,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):
,持续加热,剩余固体的质量随温度变化的部分数据如下表(其中450℃以前是隔绝空气加热,450℃以后是在空气中加热):| 温度/℃ | 25 | 150 | 300 | 350 | 400 | 450 | 500 | 600 | 700 | 800 |
| 固体质量/g | 18.00 | 16.20 | 14.40 | 14.40 | 7.20 | 7.20 | 8.00 | 8.00 | 7.73 | 7.73 |
根据上述数据计算并推断:150℃剩余的固体物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
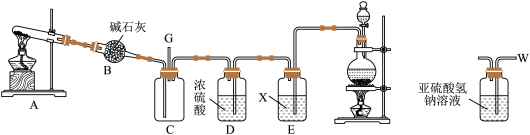
【推荐1】FeCl3能用于金属蚀刻、污水处理、印染工业。某化学研究性学习小组模拟工业生产流程制备氯化铁并对产物做如下探究实验(部分夹持装置省略)。

已知:三氯化铁易升华,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。
(1)A中装MnO2的仪器名称___________ ,D中装碱石灰的仪器名称___________ 。
(2)实验中制取氯气的离子方程式为___________ 。
(3)装置的连接顺序为:a→___________ →f。
(4)碱石灰的作用是___________ 。
(5)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

用离子方程式表示淡红色溶液中加入过量H2O2后,溶液颜色变深的原因有:
a:___________ ;
b: 。
。

已知:三氯化铁易升华,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。
(1)A中装MnO2的仪器名称
(2)实验中制取氯气的离子方程式为
(3)装置的连接顺序为:a→
(4)碱石灰的作用是
(5)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

用离子方程式表示淡红色溶液中加入过量H2O2后,溶液颜色变深的原因有:
a:
b:
 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室中所用少量氯气是用下列方法制取的,试回答下列问题:

(1)发生装置中的反应的化学方程式___ 。是氧化还原反应吗?___ ,如果是氧化还原反应,请指出___ 是氧化剂,___ 是还原剂。
(2)集气瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯化氢在饱和食盐水中的溶解度则很大),其作用是__ 。
(3)氯气溶入水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用__ 溶液来吸收有毒的氯气。
(4)一次实验中,用浓盐酸800mL,其密度为1.19g·cm-3、HCl的质量分数为36.5%,跟一定量的MnO2充分反应,产生了5.6L(STP)的氯气。试计算浓盐酸的物质的量浓度和被氧化的HCl的物质的量___ 、___ 。

(1)发生装置中的反应的化学方程式
(2)集气瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯化氢在饱和食盐水中的溶解度则很大),其作用是
(3)氯气溶入水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用
(4)一次实验中,用浓盐酸800mL,其密度为1.19g·cm-3、HCl的质量分数为36.5%,跟一定量的MnO2充分反应,产生了5.6L(STP)的氯气。试计算浓盐酸的物质的量浓度和被氧化的HCl的物质的量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO。

已知:3Cl2+6KOH KClO3+5KCl+3H2O
KClO3+5KCl+3H2O
(1)烧瓶内发生的离子反应方程式是______ 。其中盐酸的实际用量大于理论量的原因是______ 。
(2)装置a中试剂的作用是______ 。
(3)装置c中发生的离子反应方程式是______ 。
(4)d装置的作用为______ 。

已知:3Cl2+6KOH
 KClO3+5KCl+3H2O
KClO3+5KCl+3H2O(1)烧瓶内发生的离子反应方程式是
(2)装置a中试剂的作用是
(3)装置c中发生的离子反应方程式是
(4)d装置的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
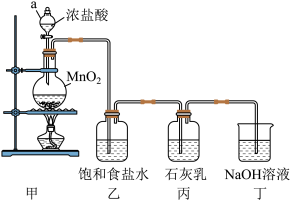
【推荐2】某兴趣小组模拟工业制漂白粉,设计了下列图5的实验装置,已知:①氯气和碱反应放出热量;②6Cl2+6Ca(OH)2 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
回答下列问题:
(1)甲装置中仪器a的名称是_______ ,MnO2在反应中所起的作用是(填“氧化剂”或“还原剂”)______________ 。
(2)装置乙中饱和食盐水的作用是____________________________ 。
(3)①制取漂白粉的化学方程式是____________________________ 。
②该小组制得的漂白粉中n(CaCl2) 远大于n[Ca(ClO)2],其主要原因是_________ 。
③为提高Ca(ClO)2的含量,可采取的措施是_______________ (任写一种即可)。
(4)漂白粉应密封保存,原因是______________________ (用化学方程式表示)。
 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
回答下列问题:
(1)甲装置中仪器a的名称是
(2)装置乙中饱和食盐水的作用是
(3)①制取漂白粉的化学方程式是
②该小组制得的漂白粉中n(CaCl2) 远大于n[Ca(ClO)2],其主要原因是
③为提高Ca(ClO)2的含量,可采取的措施是
(4)漂白粉应密封保存,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用如图所示实验装置可完成中学化学中的一些实验。请回答下列问题:

(1)仪器A的名称为___ 。
(2)若要证明非金属性:Cl>S,则可在A中加浓盐酸,B中加KMnO4(已知:KMnO4与浓盐酸常温下反应可生成氯气),C中加入Na2S溶液,观察到C中产生淡黄色浑浊的现象,即可证明,C中发生反应的离子方程式为___ ,若从环境保护的角度考虑,此装置还缺少尾气处理装置,可用___ 溶液吸收尾气。
(3)现有稀硝酸、稀盐酸、稀硫酸、碳酸钠粉末、硅酸钠溶液五种试剂。选择三种试剂利用如图装置证明酸性强弱:H2SO4>H2CO3>H2SiO3,回答下列问题:
①A中试剂为___ ,B中试剂为___ 。
②要得出酸性H2SO4>H2CO3>H2SiO3的结论,则C中应观察到的现象为___ 。
(4)利用如图装置证明SO2气体具有漂白性。已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O。在装置A中加入70%的硫酸溶液,B中加入Na2SO3粉末,C中加入品红溶液。打开分液漏斗活塞,一段时间后C中观察到的现象是___ ,待反应完全后,将试管C加热一段时间发生的现象是___ ,即可证明SO2气体具有漂白性。

(1)仪器A的名称为
(2)若要证明非金属性:Cl>S,则可在A中加浓盐酸,B中加KMnO4(已知:KMnO4与浓盐酸常温下反应可生成氯气),C中加入Na2S溶液,观察到C中产生淡黄色浑浊的现象,即可证明,C中发生反应的离子方程式为
(3)现有稀硝酸、稀盐酸、稀硫酸、碳酸钠粉末、硅酸钠溶液五种试剂。选择三种试剂利用如图装置证明酸性强弱:H2SO4>H2CO3>H2SiO3,回答下列问题:
①A中试剂为
②要得出酸性H2SO4>H2CO3>H2SiO3的结论,则C中应观察到的现象为
(4)利用如图装置证明SO2气体具有漂白性。已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O。在装置A中加入70%的硫酸溶液,B中加入Na2SO3粉末,C中加入品红溶液。打开分液漏斗活塞,一段时间后C中观察到的现象是
您最近一年使用:0次