现需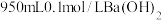 溶液,称取氢氧化钡晶体[
溶液,称取氢氧化钡晶体[ ](
](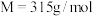 )配制。下列说法正确的是
)配制。下列说法正确的是
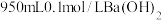 溶液,称取氢氧化钡晶体[
溶液,称取氢氧化钡晶体[ ](
](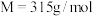 )配制。下列说法正确的是
)配制。下列说法正确的是A.应称量氢氧化钡晶体质量为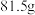 |
| B.容量瓶需用自来水、蒸馏水洗涤,干燥后才可用 |
| C.定容时俯视刻度线导致所配溶液物质的量浓度偏小 |
D.取所配溶液并加等体积水稀释,得到 溶液 溶液 |
更新时间:2024-02-01 15:25:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关浓度的说法正确的是
| A.10℃时,100 mL 0.35 mol/L的KCl饱和溶液蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度大于0. 35 mol/L |
| B.将标准状况下22. 4L HCl溶于1 L水中可得1 mol/L盐酸 |
| C.将78 gNa2O2溶于水,配成1 L溶液可得到浓度为1mol/L的溶液 |
| D.将25.0 g胆矾(CuSO4·5H2O)溶于水后配成100 mL溶液,所得溶液浓度为1 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于溶液的叙述中错误的是( )
| A.将20 mL2 mo/L的H2SO4溶液加水稀释至40 mL,浓度变为1mo/L |
| B.配制0.1 mol/L的NaCl溶液240 mL,需称量NaCl固体1.5g |
| C.配制溶液时,转移操作之后没有对烧杯和玻璃棒进行洗涤会导致浓度偏低 |
| D.在标准状况下将22.4 L HCl气体溶于1 L水中,得到1mol/L的盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】现有两份溶液A和B,若A溶液中含有H+、Al3+、SO 三种离子,其中H+的浓度为0.5mol•L-1,Al3+的浓度为0.3mol•L-1,B溶液中含有Fe3+、Cl-、Ba2+三种离子,其中Cl-的浓度为0.4mol•L-1,将两溶液等体积混合(忽略溶液体积的变化),则混合后SO
三种离子,其中H+的浓度为0.5mol•L-1,Al3+的浓度为0.3mol•L-1,B溶液中含有Fe3+、Cl-、Ba2+三种离子,其中Cl-的浓度为0.4mol•L-1,将两溶液等体积混合(忽略溶液体积的变化),则混合后SO 的浓度可能是
的浓度可能是
 三种离子,其中H+的浓度为0.5mol•L-1,Al3+的浓度为0.3mol•L-1,B溶液中含有Fe3+、Cl-、Ba2+三种离子,其中Cl-的浓度为0.4mol•L-1,将两溶液等体积混合(忽略溶液体积的变化),则混合后SO
三种离子,其中H+的浓度为0.5mol•L-1,Al3+的浓度为0.3mol•L-1,B溶液中含有Fe3+、Cl-、Ba2+三种离子,其中Cl-的浓度为0.4mol•L-1,将两溶液等体积混合(忽略溶液体积的变化),则混合后SO 的浓度可能是
的浓度可能是| A.0.2mol•L-1 | B.0.3mol•L-1 | C.0.4mol•L-1 | D.0.5mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学实验室里有一瓶盐酸,上面的标签如图所示。下列说法正确的是
| 产品名称:盐酸 化学式:HCl 产品等级:分析纯 质量分数:36.5% 密度:1.19g/cm3 |
| A.该盐酸物质的量浓度为11.9 mol·L-1 |
| B.等体积的该盐酸与水混合后质量分数约为18.25% |
| C.配制500 mL 0.400 mol/L的稀盐酸需该盐酸1.68 mL |
| D.中和含0.4 g NaOH的NaOH溶液需取0.400 mol/L的稀盐酸2.5 mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】如图是硫酸试剂瓶标签上的部分内容。据此下列说法中,正确的是
| 硫酸 化学纯(CP) (500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g·cm-3 质量分数:98% |
| A.该硫酸可以用来干燥硫化氢气体 |
| B.若需200 mL 4.6 mol·L-1的稀硫酸需取该硫酸50 mL进行配制 |
| C.1 mol Zn与足量的该硫酸反应能产生2 g H2 |
| D.若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.用CC14萃取碘水中的碘单质,振荡过程中需进行放气操作 |
| B.用容量瓶配制溶液,定容时仰视刻度线,则所配溶液浓度偏高 |
| C.量筒上标有“0”刻度、温度和规格 |
| D.用棕色的碱式滴定管准确量取10.00mL溴水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是

| A.酸碱中和滴定时,滴定管和锥形瓶在使用前均需用待装液润洗 |
| B.清洗碘升华实验所用试管,先用稀盐酸清洗,再用水清洗 |
C.实验室从海带提取单质碘的方法是:取样 灼烧 灼烧 溶解 溶解 过滤 过滤 萃取 萃取 |
D.配制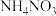 溶液时未恢复至室温就转移并定容,所得溶液浓度偏小 溶液时未恢复至室温就转移并定容,所得溶液浓度偏小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】按下列实验方案能达到要求的是
| A.托盘天平称量25.20g NaCl固体 | B.用量筒量出11.4mL 0.1mol/L的盐酸 |
| C.用100mL量筒量取2.50mL稀盐酸 | D.用PH试纸测得某溶液的pH为5.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验不宜使用锥形瓶的是
| A.蒸馏 | B.用高锰酸钾与浓盐酸制Cl2 |
| C.中和滴定 | D.配制500mL 0.2 mol·L-1的H2SO4溶液 |
您最近一年使用:0次