如下图为铁及其化合物的“价一类”二维图。
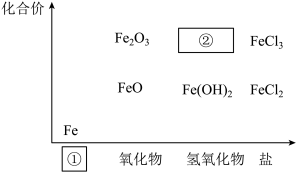
(1)填写二维图缺失的类别①___________ 和化学式②___________ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe③NaOH④H2SO4⑤AgNO3
i.从物质类别上看,FeCl3属于___________ ,可能与___________ 发生反应(填序号)。
ii.从化合价角度看,Fe3+具有___________ 性,可能与___________ 发生反应(填序号)。
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①FeCl3在反应中作___________ 剂。
②该反应的离子方程式为___________ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe③NaOH④H2SO4⑤AgNO3
i.从物质类别上看,FeCl3属于
ii.从化合价角度看,Fe3+具有
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①FeCl3在反应中作
②该反应的离子方程式为
更新时间:2024-02-13 20:16:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
现有以下物质:①H2O ②Fe ③BaCO3 ④Fe(OH)3胶体 ⑤NaHSO4溶液 ⑥干冰 ⑦稀硫酸⑧酒精⑨碳酸氢钠
(1)以上物质中属于混合物的是___________ (填序号,下同),属于电解质的是___________ 。
(2)向④中逐滴滴加⑦,可观察到的现象是___________ 。
(3)虽然分类的方法不同,但四种基本反应类型和离子反应之间也存在着一定的关系。请从以上物质中写出一个既属于置换反应,又属于离子反应的离子方程式:___________ 。
(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)___________ 。
现有以下物质:①H2O ②Fe ③BaCO3 ④Fe(OH)3胶体 ⑤NaHSO4溶液 ⑥干冰 ⑦稀硫酸⑧酒精⑨碳酸氢钠
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
(3)虽然分类的方法不同,但四种基本反应类型和离子反应之间也存在着一定的关系。请从以上物质中写出一个既属于置换反应,又属于离子反应的离子方程式:
(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)
您最近一年使用:0次
【推荐2】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
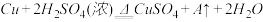 试通过计算和推理完成下面的问题:
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。A应该属于________ (用字母代号填写)。
a. 酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
(2)A物质可以使酸性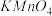 溶液褪色,此反应中(填写化学式,下同)
溶液褪色,此反应中(填写化学式,下同)_______ 失去电子,氧化剂是________ 。
(3)足量的铜片与10mL 18mol/L的浓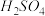 充分反应,如果该反应过程中转移了0.1mol电子,生成的
充分反应,如果该反应过程中转移了0.1mol电子,生成的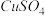 的物质的量为
的物质的量为_______ mol,生成的A气体在标准状况下体积为________ L(假设气体全部逸出)。
(4)计算:将反应后得到的溶液与足量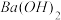 溶液混合,充分反应。反应后所得沉淀的质量为
溶液混合,充分反应。反应后所得沉淀的质量为______ g。
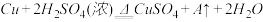 试通过计算和推理完成下面的问题:
试通过计算和推理完成下面的问题:(1)A物质可以导致酸雨的形成。A应该属于
a. 酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
(2)A物质可以使酸性
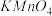 溶液褪色,此反应中(填写化学式,下同)
溶液褪色,此反应中(填写化学式,下同)(3)足量的铜片与10mL 18mol/L的浓
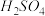 充分反应,如果该反应过程中转移了0.1mol电子,生成的
充分反应,如果该反应过程中转移了0.1mol电子,生成的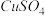 的物质的量为
的物质的量为(4)计算:将反应后得到的溶液与足量
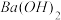 溶液混合,充分反应。反应后所得沉淀的质量为
溶液混合,充分反应。反应后所得沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列几种物质:①NaHCO3;②Ba(OH)2;③Fe2O3;④HCl;⑤H2SO4;⑥NaOH,请回答下列问题:
(1)以上物质属于酸的是____________ ,属于碱的是_______________ 属于盐的是____________ ,属于氧化物的是__________________ 。(填序号)
(2)写出③与④的离子方程式:_________________________________
(3)写出②与⑤的离子方程式:________________
(4)写出①与⑥的水溶液反应的离子反应方程式:_________________
(1)以上物质属于酸的是
(2)写出③与④的离子方程式:
(3)写出②与⑤的离子方程式:
(4)写出①与⑥的水溶液反应的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】H、C、N、O、Mg、Al、Si 、Cl、Fe是中学化学中的常见元素。
(1)Si元素在周期表中的位置是_____ ;C元素的一种同位素可测定文物年代,这种同位素的符号是_____ ;MgCl2中包含的化学键类型为____ 。
(2)用“>”、“<”或“= ”填空:
(3)一定温度下在一容积不变的密闭容器中发生可逆反应 N2(g)+3H2(g) 2NH3(g),以下能说明该反应达到化学平衡状态的是
2NH3(g),以下能说明该反应达到化学平衡状态的是_____ 。
A.混合气体的密度不再变化
B.体系的压强不再改变
C.单位时间内3mol H-H键断裂,同时6mol N-H 键也断裂
D.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。写出化学方程式并用单线桥标出电子转移的方向和数目:________ 。
(1)Si元素在周期表中的位置是
(2)用“>”、“<”或“= ”填空:
| 酸性 | 金属性 | 离子半径 |
| H2CO3 | Fe | O2- |
(3)一定温度下在一容积不变的密闭容器中发生可逆反应 N2(g)+3H2(g)
 2NH3(g),以下能说明该反应达到化学平衡状态的是
2NH3(g),以下能说明该反应达到化学平衡状态的是A.混合气体的密度不再变化
B.体系的压强不再改变
C.单位时间内3mol H-H键断裂,同时6mol N-H 键也断裂
D.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。写出化学方程式并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜是人类发现最早并广泛使用的一种金属。回答下列问题:
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为___________ 。
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式________ ,配制的FeCl3溶液应保持____ (填“酸性”“碱性”或“中性”),原因是_____ 。
(3)把铁片放入CuSO4 溶液中,充分反应后,溶液质量比反应前______ 。(填增大、减小或不变)
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式
(3)把铁片放入CuSO4 溶液中,充分反应后,溶液质量比反应前
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在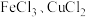 混合溶液中,加入铁粉与铜粉的混合物。
混合溶液中,加入铁粉与铜粉的混合物。
(1)若金属无剩余,则溶液中一定存在的金属阳离子有_______ ,可能存在的有_______ 。
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有_______ ,一定不存在_______ 。
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有_______ ,可能存在的有_______ ,一定不存在_______ 。
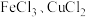 混合溶液中,加入铁粉与铜粉的混合物。
混合溶液中,加入铁粉与铜粉的混合物。(1)若金属无剩余,则溶液中一定存在的金属阳离子有
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)下列状态的物质既属于电解质又能导电的是_______ (填标号)。
(2)一定条件下,下列物质不能通过化合反应制得的有_______ (填序号)。
①小苏打 ②硫酸铝 ③磁性氧化铁 ④铜绿(碱式碳酸铜) ⑤氢氧化铁
(3)生活中若将“84”消毒液(有效成分是NaClO)和洁厕灵(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:_______ 。
(4)500mLamol•L-1Al2(SO4)3溶液中含b个SO ,则阿伏加德罗常数的表达为
,则阿伏加德罗常数的表达为_______ (用a、b表示)。
(5)为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,若生成标准状况下4.48LN2,则转移的电子数目为
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,若生成标准状况下4.48LN2,则转移的电子数目为_______ 个。
(6)写出用覆铜板制作印刷电路板的原理的化学方程式:_______ 。
(1)下列状态的物质既属于电解质又能导电的是
| A.熔融的NaCl | B.BaSO4 | C.盐酸 | D.CO2 |
①小苏打 ②硫酸铝 ③磁性氧化铁 ④铜绿(碱式碳酸铜) ⑤氢氧化铁
(3)生活中若将“84”消毒液(有效成分是NaClO)和洁厕灵(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
(4)500mLamol•L-1Al2(SO4)3溶液中含b个SO
 ,则阿伏加德罗常数的表达为
,则阿伏加德罗常数的表达为(5)为了降低饮用水中NO
 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,若生成标准状况下4.48LN2,则转移的电子数目为
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,若生成标准状况下4.48LN2,则转移的电子数目为(6)写出用覆铜板制作印刷电路板的原理的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列方程式
(1)化学方程式
①铁粉和水蒸气___________ 。
②金属钠在氧气中燃烧___________ 。
③工业制备漂白粉___________ 。
④过氧化钠和二氧化碳___________ 。
⑤铝热反应(铝和三氧化二铁)___________ 。
(2)离子方程式
①氯气溶于水___________ 。
②金属钠溶于水___________ 。
③铜片溶于氯化铁溶液___________ 。
④铝粉溶于氢氧化钠溶液___________ 。
⑤溴化亚铁溶液中通入足量氯气___________ 。
(1)化学方程式
①铁粉和水蒸气
②金属钠在氧气中燃烧
③工业制备漂白粉
④过氧化钠和二氧化碳
⑤铝热反应(铝和三氧化二铁)
(2)离子方程式
①氯气溶于水
②金属钠溶于水
③铜片溶于氯化铁溶液
④铝粉溶于氢氧化钠溶液
⑤溴化亚铁溶液中通入足量氯气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求书写化学方程式或离子方程式。
(1)除去氯化亚铁溶液中的氯化铁杂质,相应的离子方程式为___________ 。
(2)工业上用FeCl3溶液腐蚀铜线路板,相应的离子方程式为___________ 。
(3)浓硫酸和铜反应,相应的化学方程式为___________ 。
(4)Fe(OH)2在空气中被氧化,相应的化学方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子方程式为___________ 。
(1)除去氯化亚铁溶液中的氯化铁杂质,相应的离子方程式为
(2)工业上用FeCl3溶液腐蚀铜线路板,相应的离子方程式为
(3)浓硫酸和铜反应,相应的化学方程式为
(4)Fe(OH)2在空气中被氧化,相应的化学方程式为
(5)SO2能使氯水褪色,相应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业上利用高钛炉渣(主要成分为TiO2、CaTiO3及SiO2、Fe2O3等)制备TiO2。
产品中TiO2的纯度测定:准确称取0.2000 g样品,加入适量浓硫酸,加热至样品完全溶解,冷却后用水稀释,冷却至室温后再加入铝片将TiO2+还原为Ti3+,用0.1000mol·L-1 NH4Fe(SO4)2溶液滴定至终点,平行滴定3次,平均消耗NH4Fe(SO4)2溶液 。计算样品中TiO2的纯度为
。计算样品中TiO2的纯度为___________ (已知:TiO2可将Fe3+还原为Fe2+)。
产品中TiO2的纯度测定:准确称取0.2000 g样品,加入适量浓硫酸,加热至样品完全溶解,冷却后用水稀释,冷却至室温后再加入铝片将TiO2+还原为Ti3+,用0.1000mol·L-1 NH4Fe(SO4)2溶液滴定至终点,平行滴定3次,平均消耗NH4Fe(SO4)2溶液
 。计算样品中TiO2的纯度为
。计算样品中TiO2的纯度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、氨水、HI(强酸)溶液、 溶液、NaCl溶液、NaOH溶液
溶液、NaCl溶液、NaOH溶液
①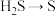 的离子方程式:
的离子方程式:____________ 。
② 的离子方程式:
的离子方程式:____________ 。
③ (两性氧化物)
(两性氧化物) 的
的化学方程式 :____________ 。
(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:化学方程式 :____________ 。
②写出氧化步骤时发生的主要反应的离子方程式:____________ 。
③写出沉铜步骤时发生的主要反应的离子方程式:____________ 。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、氨水、HI(强酸)溶液、
 溶液、NaCl溶液、NaOH溶液
溶液、NaCl溶液、NaOH溶液①
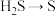 的离子方程式:
的离子方程式:②
 的离子方程式:
的离子方程式:③
 (两性氧化物)
(两性氧化物) 的
的(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:
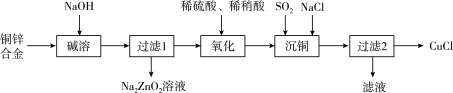
②写出氧化步骤时发生的主要反应的离子方程式:
③写出沉铜步骤时发生的主要反应的离子方程式:
您最近一年使用:0次



