模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
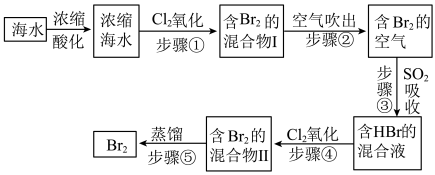
请回答下列问题。
(1)将海水浓缩的方法是___________ 。
(2)步骤②通入热空气吹出 ,利用了
,利用了 的
的___________ 性质。
(3)步骤①中的氯气改为过氧化氢,则其反应的离子方程式是___________ ,步骤③反应的离子方程式是___________ 。从理论上分析,下列也能吸收溴的是___________ (不定项选择)。
A. B.
B. C.
C. D.
D.
(4)已知海水中 含量为
含量为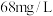 ,在上述流程步骤①的氯气氧化过程中,若将
,在上述流程步骤①的氯气氧化过程中,若将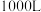 海水中的溴元素完全氧化得到含
海水中的溴元素完全氧化得到含 的混合物Ⅰ,至少需要标准状况下
的混合物Ⅰ,至少需要标准状况下 的体积
的体积___________ L(Cl2在水中溶解和与水反应均忽略)。

请回答下列问题。
(1)将海水浓缩的方法是
(2)步骤②通入热空气吹出
 ,利用了
,利用了 的
的(3)步骤①中的氯气改为过氧化氢,则其反应的离子方程式是
A.
 B.
B. C.
C. D.
D.
(4)已知海水中
 含量为
含量为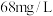 ,在上述流程步骤①的氯气氧化过程中,若将
,在上述流程步骤①的氯气氧化过程中,若将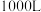 海水中的溴元素完全氧化得到含
海水中的溴元素完全氧化得到含 的混合物Ⅰ,至少需要标准状况下
的混合物Ⅰ,至少需要标准状况下 的体积
的体积
更新时间:2024-02-17 10:30:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】叠氮化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。下面是工业水合肼法制备叠氮
化钠的工艺流程:

已知 NaN3能与 AgNO3反应生成白色难溶于水的 AgN3;Ag2CrO4呈红色,可溶于水。有关物质的物理性质如下表:
请回答:
(1)步骤Ⅰ中NaNO2与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为另一种气体)的离子方程式为_____ ;步骤Ⅱ中生成 NaN3的化学方程式为_____
(2)实验室模拟步骤Ⅱ实验装置如图(装置中冷却水省略,下同):根据实验发现温度在 20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此需要采取的措施是_____ 。
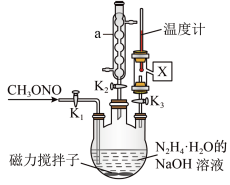
(3)步骤Ⅱ、Ⅲ中制备叠氮化钠并对溶液 A 进行蒸馏的合理操作顺序是_____ 。
①打开 K1、K2,关闭 K3 ②打开 K3 ③加热 ④关闭 K1、K2
(4)步骤Ⅳ对溶液B 加热蒸发至溶液体积的 1/3,NaN3结晶析出。
①步骤Ⅴ最好选用_____ 洗涤晶体。
A.水 B.乙醇 C.乙醚
②沉淀滴定法测定产品纯度,是以淡黄色 K2CrO4溶液作指示剂,将 AgNO3标准溶液滴入样品溶液, 滴定终点现象为_________ 。AgNO3溶液要装在_____ 滴定管里进行滴定。下列说法正确的是_____ 。
A.滴定管和移液管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若发现滴液过量,可回滴样品溶液
E.若未等滴定管液面稳定就读数会导致测定结果偏高
化钠的工艺流程:

已知 NaN3能与 AgNO3反应生成白色难溶于水的 AgN3;Ag2CrO4呈红色,可溶于水。有关物质的物理性质如下表:
| 熔点℃ | 沸点℃ | 溶解性 | |
| CH3OH | -9 | 64.7 | 与水互溶 |
| 水合肼(N2H4•H2O) | 2 | 113.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 难溶于水,可溶于乙醇、乙醚 |
| NaN3 | 275 | 300 | 易溶于水,难溶于乙醇 |
(1)步骤Ⅰ中NaNO2与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为另一种气体)的离子方程式为
(2)实验室模拟步骤Ⅱ实验装置如图(装置中冷却水省略,下同):根据实验发现温度在 20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此需要采取的措施是

(3)步骤Ⅱ、Ⅲ中制备叠氮化钠并对溶液 A 进行蒸馏的合理操作顺序是
①打开 K1、K2,关闭 K3 ②打开 K3 ③加热 ④关闭 K1、K2
(4)步骤Ⅳ对溶液B 加热蒸发至溶液体积的 1/3,NaN3结晶析出。
①步骤Ⅴ最好选用
A.水 B.乙醇 C.乙醚
②沉淀滴定法测定产品纯度,是以淡黄色 K2CrO4溶液作指示剂,将 AgNO3标准溶液滴入样品溶液, 滴定终点现象为
A.滴定管和移液管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若发现滴液过量,可回滴样品溶液
E.若未等滴定管液面稳定就读数会导致测定结果偏高
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】过氧化氢俗名双氧水,医疗上利用它杀菌消毒的作用来清洗伤口。根据下列反应回答问题:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2 2H2O+O2↑
2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同)_______ ,H2O2既体现氧化性又体现还原性的反应是_______ ,H2O2体现酸性的反应是_______ 。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是_______ 。
(3)储存过氧化氢的试剂瓶上最适合贴上的一个标签是_______ (填序号)。

(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①反应体系选择的酸是_______ (填序号)。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②该反应的离子方程式为_______ 如果上述反应中有6.72L(标准状况)气体生成,转移的电子为_______ mol。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2
 2H2O+O2↑
2H2O+O2↑D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同)
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是
(3)储存过氧化氢的试剂瓶上最适合贴上的一个标签是

(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、
 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。①反应体系选择的酸是
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】次锰酸根离子 ,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分
,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的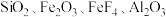 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
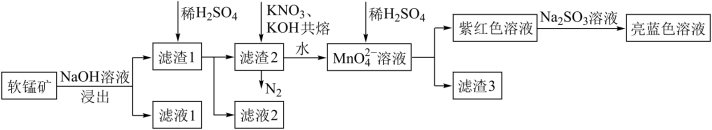
(1)滤渣1的主要成分是____ , 在周期表中的位置
在周期表中的位置___ 。
(2)流程中共熔时发生的主要反应的化学方程式为____ 。
(3)写出 转变为紫红色溶液的离子反应方程式
转变为紫红色溶液的离子反应方程式____ 。
(4)整个流程中的__ (填化学式)能重复利用。
(5) 还原软锰矿制备
还原软锰矿制备 的化学方程式为
的化学方程式为____ 。
(6)往 溶液中加入过量
溶液中加入过量 溶液可以制得
溶液可以制得 ,该反应的离子方程式为
,该反应的离子方程式为__ 。
 ,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分
,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的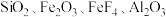 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
(1)滤渣1的主要成分是
 在周期表中的位置
在周期表中的位置(2)流程中共熔时发生的主要反应的化学方程式为
(3)写出
 转变为紫红色溶液的离子反应方程式
转变为紫红色溶液的离子反应方程式(4)整个流程中的
(5)
 还原软锰矿制备
还原软锰矿制备 的化学方程式为
的化学方程式为(6)往
 溶液中加入过量
溶液中加入过量 溶液可以制得
溶液可以制得 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
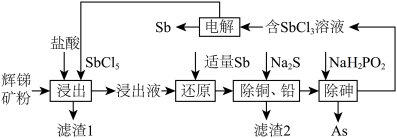
【推荐1】锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________ (填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_________________ 。
(3)“还原”时,被Sb还原的物质为_____________ (填化学式)。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于______ ;所加Na2S也不宜过多,其原因为_____________ 。
(5)“除砷”时有H3PO3生成,该反应的离子方程式为________________ 。
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_______ 。
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有
(2)“浸出”时,Sb2S3发生反应的化学方程式为
(3)“还原”时,被Sb还原的物质为
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于
(5)“除砷”时有H3PO3生成,该反应的离子方程式为
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】实验室用氨法浸出氧化锌烟尘制备活性ZnO,其主要实验流程如图:
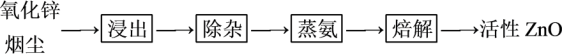
(1)浸出。用一定浓度的氨水和NH4HCO3配成的混合液浸取氧化锌烟尘,得到锌氨[Zn(NH3)4CO3]浸出液。
①烟尘中的主要成分ZnO发生反应的化学方程式为_______ 。
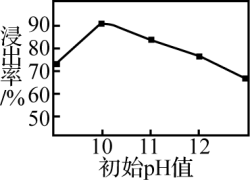
②锌元素的浸出率随浸出液初始pH的变化关系如图所示。当浸出液初始pH大于10时,浸出率随pH增大而减小的原因是_______ 。
(2)除杂。Cu2+、Pb2+等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式_______ 。
(3)蒸氨。加热时溶液中过量的氨和铵被蒸出,锌氨配合物最终以2ZnCO3·3Zn(OH)2沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为_______ 。
(4)已知pH>11时,Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表是几种离子生成氢氧化物沉淀的pH:
设计以锌灰(主要成分为Zn和ZnO,杂质为Fe及其氧化物)为原料制备活性ZnO的实验方案:_______ 。(实验中可供选择的试剂:1.0 mol/L HNO3、1.0 mol/L H2SO4、1.0 mol/L NaOH、20%H2O2)
(5)取mg活性氧化锌样品,预处理后配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为_______ (用代数式表示)。
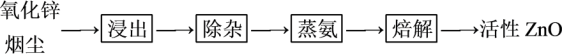
(1)浸出。用一定浓度的氨水和NH4HCO3配成的混合液浸取氧化锌烟尘,得到锌氨[Zn(NH3)4CO3]浸出液。
①烟尘中的主要成分ZnO发生反应的化学方程式为
②锌元素的浸出率随浸出液初始pH的变化关系如图所示。当浸出液初始pH大于10时,浸出率随pH增大而减小的原因是

(2)除杂。Cu2+、Pb2+等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式
(3)蒸氨。加热时溶液中过量的氨和铵被蒸出,锌氨配合物最终以2ZnCO3·3Zn(OH)2沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为
(4)已知pH>11时,Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表是几种离子生成氢氧化物沉淀的pH:
| 开始沉淀的pH | 沉淀完全的pH | |
| Zn2+ | 5.9 | 8.9 |
| Fe2+ | 5.8 | 8.8 |
| Fe3+ | 1.1 | 3.2 |
(5)取mg活性氧化锌样品,预处理后配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴的流程如下:
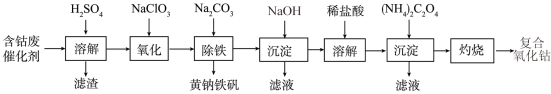
(1)用H2SO4溶解后过滤,得到的滤渣是____ (填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是_________________________________ 。
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是__________ 。
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3− =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是_________________________________ 。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(4)已知CoCl2的溶解度曲线如图所示。
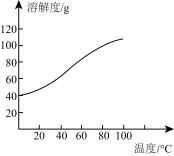
向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是_________________ 。

(1)用H2SO4溶解后过滤,得到的滤渣是
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3− =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4− = Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是
(4)已知CoCl2的溶解度曲线如图所示。

向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】目前工业上常用的一种海水提溴技术“吹出法”,工艺流程图如图:
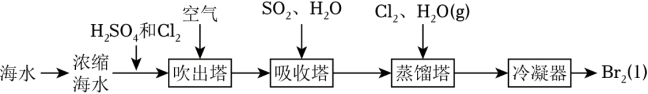
回答下列问题:
(1)溴在元素周期表中的位置___________ 。
(2)下列试剂可用于代替Cl2的是(填标号)___________。
(3)吸收塔内发生的主要反应化学方程式为___________ ;蒸馏塔内发生的主要反应离子方程式为___________ 。
(4)工业生产中,不是将H2SO4酸化和Cl2氧化后的海水直接蒸馏,而是经过“空气吹出”、“SO2吸收”、“Cl2氯化”后再蒸馏得到液溴,目的是___________ 。
(5)工业生产中,测得浓缩海水中溴的含量为800g•m-3,通过吹出塔、吸收塔时共损失了25%的溴,蒸馏和冷凝时共损失了10%的溴。处理10m3该浓缩海水,实际可得到液溴___________ mol。

回答下列问题:
(1)溴在元素周期表中的位置
(2)下列试剂可用于代替Cl2的是(填标号)___________。
| A.I2 | B.H2O2 | C.FeCl3 | D.NaBrO3 |
(4)工业生产中,不是将H2SO4酸化和Cl2氧化后的海水直接蒸馏,而是经过“空气吹出”、“SO2吸收”、“Cl2氯化”后再蒸馏得到液溴,目的是
(5)工业生产中,测得浓缩海水中溴的含量为800g•m-3,通过吹出塔、吸收塔时共损失了25%的溴,蒸馏和冷凝时共损失了10%的溴。处理10m3该浓缩海水,实际可得到液溴
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】海水是资源宝库,下图是对海水资源的综合利用(部分操作或试剂已省略)。

请回答下列问题:
(1)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是___________ ,步骤II将溴吹出的气体X不可能是下列的___________ (填字母)。
A.二氧化硫B.空气C.氩气D.二氧化碳
写出步骤II过程中用硫酸酸化得到单质溴的离子方程式:___________ 。
(2)工业上从卤水中提取镁,常选用作为沉淀剂的碱为___________ (填化学式),选用该物质的主要原因是___________ 。
(3)海水淡化常见的方法有蒸馏法、___________ 、离子交换法,离子交换法净化水过程如图所示。阴离子树脂填充段存在反应的离子方程式为___________ 。
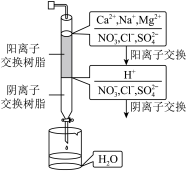

请回答下列问题:
(1)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是
A.二氧化硫B.空气C.氩气D.二氧化碳
写出步骤II过程中用硫酸酸化得到单质溴的离子方程式:
(2)工业上从卤水中提取镁,常选用作为沉淀剂的碱为
(3)海水淡化常见的方法有蒸馏法、

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海洋中储有大量的化学物质,储量可观的化学元素就有80多种,其中70多种可以被人类提取利用,全世界每年都要从海洋中提取大量的食盐、铁、溴、碘、钾等有用物质,海水被誉为“液体工业原料”。从海水中提取食盐、镁和溴的流程如图所示。回答下列问题:
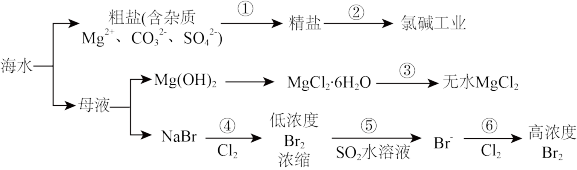
(1)从海水中得到的粗盐中含Mg2+、Ca2+、 等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是
等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是_______ 。
(2)氨碱工业的主要反应是电解饱和氯化钠溶液,写出反应的离子方程式_______ 。
(3)MgCl2·6H2O脱水过程中易水解生成碱式氯化镁,涉及的离子方程式为_______ 。因此工业上常使MgCl2·6H2O晶体在_______ 气体中脱水而得到干燥无水的MgCl2。
(4)第⑤步是用热空气将Br2吹入SO2溶液中,写出反应的化学方程式_______ 。
(5)电解无水MgCl2可得金属镁和氯气,利用副产品氯气还可制备漂白粉,其反应的化学方程式为_______ 。
(6)步骤④中用硫酸酸化可提高Cl2的利用率,理由是_______ 。含高浓度Br2的水溶液经过蒸馏可得到Br2,蒸馏的温度为80~90℃,温度过高或过低都不利于生产,请解释原因:_______ 。

(1)从海水中得到的粗盐中含Mg2+、Ca2+、
 等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是
等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是(2)氨碱工业的主要反应是电解饱和氯化钠溶液,写出反应的离子方程式
(3)MgCl2·6H2O脱水过程中易水解生成碱式氯化镁,涉及的离子方程式为
(4)第⑤步是用热空气将Br2吹入SO2溶液中,写出反应的化学方程式
(5)电解无水MgCl2可得金属镁和氯气,利用副产品氯气还可制备漂白粉,其反应的化学方程式为
(6)步骤④中用硫酸酸化可提高Cl2的利用率,理由是
您最近一年使用:0次



