已知有以下物质相互转化试回答:

(1)写出B、C、D三种溶液中溶质的化学式。
B.___________ 、C.___________ 、D.___________ 。
(2)写出由E转变成F的化学方程式___________ 。
(3)向G溶液加入A的有关离子反应方程式___________ 。
(4)列举一种检验G溶液中金属阳离子的方法:___________ 。

(1)写出B、C、D三种溶液中溶质的化学式。
B.
(2)写出由E转变成F的化学方程式
(3)向G溶液加入A的有关离子反应方程式
(4)列举一种检验G溶液中金属阳离子的方法:
更新时间:2024-02-20 20:19:59
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
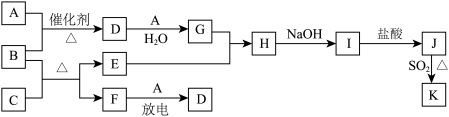
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________ 。
(2)E与G的稀溶液反应的离子方程式为_________ 。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________ 。
(5)B和C反应的化学方程式为__________ 。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______ 。

已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为
(2)E与G的稀溶液反应的离子方程式为
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是
(5)B和C反应的化学方程式为
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A~H等8种物质存在如下转化关系(反应条件,部分产物为标出).已知: A 是酸式盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题:

(1)写出下列物质的化学式:A________ ,B________ ,写出B的一种危害__________ 。
(2)写出下列反应的化学方程式:E→F____________ ;红热的木炭与D的浓溶液反应的方程式:____________ ;铜与H的浓溶液反应的离子方程式:_____________ 。
(3)检验某溶液中是否含A 中阳离子的方法_____________ 。

(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:E→F
(3)检验某溶液中是否含A 中阳离子的方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】化合物X仅含三种元素,通过如下实验推断其组成:
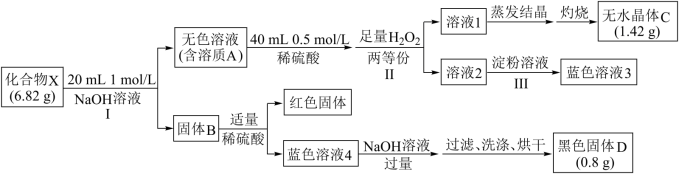
已知:X、A、B、C、D均为单一物质。
请回答:
(1)组成X的元素是___________ (填元素符号),X的化学式是___________ 。
(2)步骤Ⅰ,发生的化学方程式是___________ 。
(3)灼热黑色固体D投入乙醇中,固体变红,写出相应的化学方程式___________ 。
(4)步骤Ⅱ, 与A反应时理论消耗的物质的量之比是1∶2,但
与A反应时理论消耗的物质的量之比是1∶2,但 实际消耗量却明显偏大,其原因是
实际消耗量却明显偏大,其原因是___________ 。请设计实验证明___________ 。

已知:X、A、B、C、D均为单一物质。
请回答:
(1)组成X的元素是
(2)步骤Ⅰ,发生的化学方程式是
(3)灼热黑色固体D投入乙醇中,固体变红,写出相应的化学方程式
(4)步骤Ⅱ,
 与A反应时理论消耗的物质的量之比是1∶2,但
与A反应时理论消耗的物质的量之比是1∶2,但 实际消耗量却明显偏大,其原因是
实际消耗量却明显偏大,其原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】实验探究 、
、 的性质。
的性质。
已知: 可与
可与 溶液反应生成蓝色沉淀。
溶液反应生成蓝色沉淀。
(1)分别取一定量硫酸铁、氯化亚铁固体,均配制成 溶液。配制
溶液。配制 溶液时需加入少量铁屑,目的是
溶液时需加入少量铁屑,目的是_______ 。
(2)甲组同学取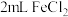 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组实验不够严谨,该组同学用煮沸冷却后的水配制溶液,向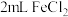 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是_____ 。
(4)丙组同学取 溶液,加入足量
溶液,加入足量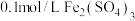 溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
_______  (填“>”或“<”);另取
(填“>”或“<”);另取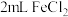 溶液,加入几小块锌片,实验现象为
溶液,加入几小块锌片,实验现象为_______ ,说明 具有
具有_______ 。(填“氧化性”或“还原性”)。
(5)丁组同学为探究维生素C是否可将 转化为
转化为 ,设计了如下实验。
,设计了如下实验。
其他组同学认为:根据该实验现象不能得出“维生素C可将 转化为
转化为 ”的结论,原因是
”的结论,原因是_______ ;认为可另外设计实验验证结论是否正确:取a溶液少许,滴加_______ ,若出现_______ ,则结论正确。
 、
、 的性质。
的性质。已知:
 可与
可与 溶液反应生成蓝色沉淀。
溶液反应生成蓝色沉淀。(1)分别取一定量硫酸铁、氯化亚铁固体,均配制成
 溶液。配制
溶液。配制 溶液时需加入少量铁屑,目的是
溶液时需加入少量铁屑,目的是(2)甲组同学取
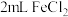 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组实验不够严谨,该组同学用煮沸冷却后的水配制溶液,向
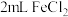 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是(4)丙组同学取
 溶液,加入足量
溶液,加入足量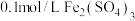 溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
 (填“>”或“<”);另取
(填“>”或“<”);另取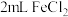 溶液,加入几小块锌片,实验现象为
溶液,加入几小块锌片,实验现象为 具有
具有(5)丁组同学为探究维生素C是否可将
 转化为
转化为 ,设计了如下实验。
,设计了如下实验。| 实验操作 | 实验现象 | 得出结论 |
取一定量 溶液于试管中,加入维生素C片,振荡溶解得到溶液a.取a溶液少许,滴加酸性 溶液于试管中,加入维生素C片,振荡溶解得到溶液a.取a溶液少许,滴加酸性 溶液。 溶液。 | 紫色褪去 | 维生素C可将 转化为 转化为 |
 转化为
转化为 ”的结论,原因是
”的结论,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】沉淀溶解平衡是水溶液体系中常见的平衡,在生产中有重要应用。请回答:
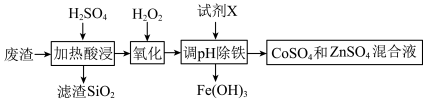
(1)钴在硬质高温合金、催化剂等高新技术领域有广泛应用。下图是某炼锌厂的废渣(含Zn、Co、Fe、 、
、 等)中回收钴和锌工艺流程的一部分:
等)中回收钴和锌工艺流程的一部分:
相关金属离子 形成氢氧化物沉淀的pH范围如表:
形成氢氧化物沉淀的pH范围如表:
①检验溶液中存在 的最佳试剂为
的最佳试剂为__________ (填字母)。
A. B.
B. C.
C. D.
D.
②氧化过程是将 转化为
转化为 ,有关反应的离子方程式为
,有关反应的离子方程式为__________ 。
③试剂X可以为__________ (填化学式),需控制溶液pH的范围为__________ 。
(2)为了除去水垢中的 ,可先用
,可先用 溶液处理,原理是
溶液处理,原理是___________ (用离子方程式表示);已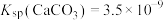 、
、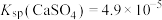 ,上述反应的平衡常数
,上述反应的平衡常数
__________ 。
(1)钴在硬质高温合金、催化剂等高新技术领域有广泛应用。下图是某炼锌厂的废渣(含Zn、Co、Fe、
 、
、 等)中回收钴和锌工艺流程的一部分:
等)中回收钴和锌工艺流程的一部分:
相关金属离子
 形成氢氧化物沉淀的pH范围如表:
形成氢氧化物沉淀的pH范围如表:金属离子 |
|
|
|
|
开始沉淀的pH | 7.2 | 6.3 | 1.5 | 6.2 |
沉淀完全的pH | 9.2 | 8.3 | 2.8 | 8.2 |
 的最佳试剂为
的最佳试剂为A.
 B.
B. C.
C. D.
D.
②氧化过程是将
 转化为
转化为 ,有关反应的离子方程式为
,有关反应的离子方程式为③试剂X可以为
(2)为了除去水垢中的
 ,可先用
,可先用 溶液处理,原理是
溶液处理,原理是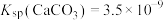 、
、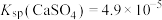 ,上述反应的平衡常数
,上述反应的平衡常数
您最近一年使用:0次
【推荐3】去除空气中SO2的污染,科研人员设计了碘循环工艺。副产品为氢气,具体流程如下:
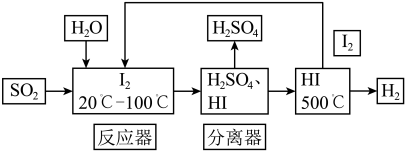
(56.9%的HI水溶液恒沸点127℃,98.3%H2SO4水溶液恒沸点338℃)
回答下列问题:
(1)写出反应器中发生反应的化学方程式_______ 。
(2)取样,检验反应器中碘单质是否消耗完全,应加入的试剂为_______ 。
(3)分离器中的物质分离操作为_______ 。
(4)该循环工艺的总反应化学方程式为_______ 。
(5)在溶液中铁离子可以将碘离子氧化为碘单质,该反应的离子方程式为_______ 。请设计出该反应发生后检验溶液中是否存在铁离子的实验方案_______ 。
(6)500℃分解HI生成碘蒸汽和氢气,利用冷却时碘_______ 可以将二者进行分离。

(56.9%的HI水溶液恒沸点127℃,98.3%H2SO4水溶液恒沸点338℃)
回答下列问题:
(1)写出反应器中发生反应的化学方程式
(2)取样,检验反应器中碘单质是否消耗完全,应加入的试剂为
(3)分离器中的物质分离操作为
(4)该循环工艺的总反应化学方程式为
(5)在溶液中铁离子可以将碘离子氧化为碘单质,该反应的离子方程式为
(6)500℃分解HI生成碘蒸汽和氢气,利用冷却时碘
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
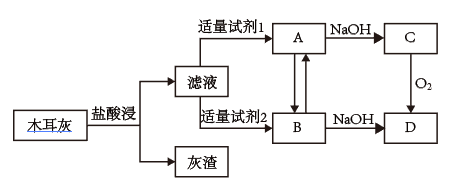
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用上图流程处理,对滤液中的溶质进行研究。
①浸泡液检测不出铁元素的原因是_______ 。
②黑木耳放在_______ (填仪器名称)中高温灼烧。
③试剂l应该是_______ 。
(2)A转化为B可加入的试剂有_______ 。
a.酸性高锰酸钾 b.Cl2 c.H2O2 d.HNO3
(3)C生成D时,当该反应转移8mol电子时,消耗标准状况下O2的体积为_______ L。
(4)若称取a g黑木耳全部烧成灰,将全部灰按照上面流程中加入试剂2的方法,全部转化为D,然后过滤、洗涤加热烘干、称得D质量为b g,_______ (填“能”或“不能”)准确测出该黑木耳铁元素的含量,理由是_______ 。

(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用上图流程处理,对滤液中的溶质进行研究。
①浸泡液检测不出铁元素的原因是
②黑木耳放在
③试剂l应该是
(2)A转化为B可加入的试剂有
a.酸性高锰酸钾 b.Cl2 c.H2O2 d.HNO3
(3)C生成D时,当该反应转移8mol电子时,消耗标准状况下O2的体积为
(4)若称取a g黑木耳全部烧成灰,将全部灰按照上面流程中加入试剂2的方法,全部转化为D,然后过滤、洗涤加热烘干、称得D质量为b g,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】甲、乙丙三种不同的物质中均含有同一种元素,它们之间的转化关系如图示(部分反应物及生成物已略去)。
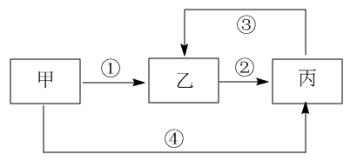
(1)若甲为气态氢化物,乙为黄色固体,写出此时反应①的化学方程式_______ 。
(2)若甲为两性氧化物,乙的水溶液呈酸性,请用离子方程式写出乙的水溶液呈酸性的原因_______ ,写出此时反应④的离子方程式_______ 。
(3)若甲为金属单质,反应④为置换反应,则往乙溶液中滴加KSCN,溶液变为_______ :往丙的溶液中滴加_______ (填化学式),产生蓝色沉淀。
(4)若甲为气体单质,乙为含有极性共价键的非极性分子,请写出甲的分子式_______ ,乙的电子式_______ 。

(1)若甲为气态氢化物,乙为黄色固体,写出此时反应①的化学方程式
(2)若甲为两性氧化物,乙的水溶液呈酸性,请用离子方程式写出乙的水溶液呈酸性的原因
(3)若甲为金属单质,反应④为置换反应,则往乙溶液中滴加KSCN,溶液变为
(4)若甲为气体单质,乙为含有极性共价键的非极性分子,请写出甲的分子式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】三氯化铁溶液可腐蚀印刷电路板上的铜膜,某小组为了从腐蚀废液(含有大量CuCl2、FeCl2和FeCl3)中回收铜,并将铁的化合物全部转化为溶液作为腐蚀液原料循环使用,设计了如下实验步骤:
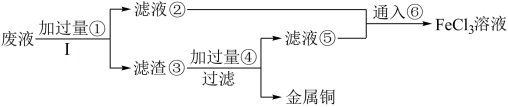
(1)写出下列物质的化学式①___ 、⑥___ 。
(2)步骤Ⅰ的操作名称:___ 。
(3)写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(4)向②中加入NaOH溶液并长时间暴露在空气中,先产生白色沉淀,后迅速变为灰绿色,接着又转化为__ 色沉淀,此过程所涉及反应的化学方程式为:______ 、___ 。
(5)通入⑥发生反应的离子方程式:________ 。
(6)若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是___ (填字母代号)。
A 有铜无铁 B 有铁无铜 C 铁、铜都有 D 铁、铜都无

(1)写出下列物质的化学式①
(2)步骤Ⅰ的操作名称:
(3)写出FeCl3溶液与铜发生反应的离子方程式:
(4)向②中加入NaOH溶液并长时间暴露在空气中,先产生白色沉淀,后迅速变为灰绿色,接着又转化为
(5)通入⑥发生反应的离子方程式:
(6)若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A 有铜无铁 B 有铁无铜 C 铁、铜都有 D 铁、铜都无
您最近一年使用:0次





