NaClO、 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。
(1) 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为___________ (不考虑 的分解)。
的分解)。
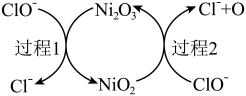
(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是___________ (填“氧化剂”或“还原剂”),当 和
和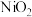 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为___________ 。
②NaClO可在碱性条件下将 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为___________ 。
(3)以氯酸钠、硫酸和二氧化硫为原料制备 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
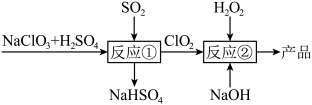
反应①的离子方程式为___________ ;理论上,该流程中参与反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。(1)
 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为 的分解)。
的分解)。(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收
 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是 和
和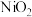 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
②NaClO可在碱性条件下将
 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为(3)以氯酸钠、硫酸和二氧化硫为原料制备
 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
反应①的离子方程式为
 与
与 的物质的量之比为
的物质的量之比为
更新时间:2024-02-21 14:12:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】人们应用原电池原理制作了多种电池,广泛使用于日常生活、生产和科学技术等方面,以满足不同的需要。请按要求回答下列问题:
(1)新一代锂二次电池体系和全固态锂二次电池体系是化学、物理等学科的基础理论研究与应用技术的前沿。
①Li—CuO二次电池的比能量高、工作温度宽。Li—CuO二次电池中,放电时金属锂作____ 极。比能量是指消耗单位质量的电极所释放的电量,可用来衡量电池的优劣,则Li、Na、Al分别作为电极时比能量由大到小的顺序为____ 。
②一种制备CuO的过程如图:

“酸浸反应”中,H2O2作____ (填“氧化剂”或“还原剂”)。写出“混合沉淀”过程产生Cu2(OH)2CO3反应的离子方程式:____ 。
(2)CH3OH可作为燃料使用,使用CH3OH和O2组合设计的燃料电池的结构如图所示,电池总反应为2CH3OH+3O2=2CO2+4H2O,质子(H+)交换膜左右两侧的溶液均为等浓度的稀硫酸。

①物质a为____ (填化学式);电极c上发生的电极反应为____ 。
②电极d为____ 极,电极d上发生的电极反应为____ 。
(1)新一代锂二次电池体系和全固态锂二次电池体系是化学、物理等学科的基础理论研究与应用技术的前沿。
①Li—CuO二次电池的比能量高、工作温度宽。Li—CuO二次电池中,放电时金属锂作
②一种制备CuO的过程如图:

“酸浸反应”中,H2O2作
(2)CH3OH可作为燃料使用,使用CH3OH和O2组合设计的燃料电池的结构如图所示,电池总反应为2CH3OH+3O2=2CO2+4H2O,质子(H+)交换膜左右两侧的溶液均为等浓度的稀硫酸。

①物质a为
②电极d为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)除去铁粉中混有的铝粉选用试剂:___________ ,离子方程式:___________ 。
(2)盛放烧碱等碱性溶液不宜用磨口玻璃塞,相应的离子方程式为:___________ 。
(3)用稀盐酸清洗铜器皿表面上的铜锈的方程式为___________ 。
(4)实验室配制好的硅酸钠溶液保存过程中变质相应化学方程式是___________ 。
(2)盛放烧碱等碱性溶液不宜用磨口玻璃塞,相应的离子方程式为:
(3)用稀盐酸清洗铜器皿表面上的铜锈的方程式为
(4)实验室配制好的硅酸钠溶液保存过程中变质相应化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)化学与人类生产、生活密切相关。请按要求回答下列问题:
①下列我国古代的技术应用中,其工作原理不涉及化学反应的是___________ (填字母)
②下列用品的有效成分及用途对应错误的是_____________ (填字母)
③工业上常用氯气和石灰乳反应生产漂白粉,其原理是_________________ (用化学方程式表示)。
④在生产中,人们曾用浓氨水来检验氯气管道是否漏气。如果氯气管道某处漏气,用浓氨水检查时就会产生白烟的现象,又知此时发生的是有氮气生成的置换反应,则此时发生反应的化学方程式为____________ 。
(2)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
①有下列十种物质:
A.空气 B.O2 C.NaHSO4 D.氨水 E.CuSO4·5H2O F.NaOH G.CO2 H.Fe2O3 I.金刚石 J.H2SO4
其中属于混合物的有_____________ ;属于单质的有_____________ ;属于盐的有_____________ 。(填字母)
②有下列六个反应:
A.Cl2+H2O = HCl+HClO
B.Zn + H2SO4 = ZnSO4 + H2↑
C.2Cu2O + Cu2S 6Cu+SO2↑
6Cu+SO2↑
D.Cl2+2KI = 2KCl+I2
E.H2 + Cl2 2HCl
2HCl
F.2KClO3 2KCl+3O2↑
2KCl+3O2↑
其中属于置换反应的是___________ ,既属于分解反应又属于氧化还原反应的是__________ (填字母)。
③K2FeO4是一种重要的净水剂,可用下列方法制得:
2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O
在该反应中,还原剂是____________ ,当反应中有1mol K2FeO4生成时,转移电子的数目为______________ 。
(3)物质的量是化学计算的核心。请按要求完成下列填空:
①已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是____________ 。
②含0.4 mol Al3+的Al2O3的质量是__________________ 。
③某块光卤石(KCl·MgCl2·6H2O)中含5.3250 g Cl-,则该光卤石的物质的量为___________ 。
④标准状况下,224mL的氨气中含有的氢原子数为________________ 。
①下列我国古代的技术应用中,其工作原理不涉及化学反应的是
| A.火药使用 | B.粮食酿酒 | C.转轮排字 | D.铁的冶炼 |
 |  |  |  |
| A | B | C | D | |
| 用品 |  |  |  |  |
| 有效成分 | NaCl | NaOH | NaHCO3 | Ca(ClO)2 |
| 用途 | 做调味品 | 做治疗胃病的抗酸药 | 做发酵粉 | 做消毒剂 |
④在生产中,人们曾用浓氨水来检验氯气管道是否漏气。如果氯气管道某处漏气,用浓氨水检查时就会产生白烟的现象,又知此时发生的是有氮气生成的置换反应,则此时发生反应的化学方程式为
(2)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
①有下列十种物质:
A.空气 B.O2 C.NaHSO4 D.氨水 E.CuSO4·5H2O F.NaOH G.CO2 H.Fe2O3 I.金刚石 J.H2SO4
其中属于混合物的有
②有下列六个反应:
A.Cl2+H2O = HCl+HClO
B.Zn + H2SO4 = ZnSO4 + H2↑
C.2Cu2O + Cu2S
 6Cu+SO2↑
6Cu+SO2↑D.Cl2+2KI = 2KCl+I2
E.H2 + Cl2
 2HCl
2HClF.2KClO3
 2KCl+3O2↑
2KCl+3O2↑其中属于置换反应的是
③K2FeO4是一种重要的净水剂,可用下列方法制得:
2Fe(OH)3+3Cl2+10KOH
 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O在该反应中,还原剂是
(3)物质的量是化学计算的核心。请按要求完成下列填空:
①已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是
②含0.4 mol Al3+的Al2O3的质量是
③某块光卤石(KCl·MgCl2·6H2O)中含5.3250 g Cl-,则该光卤石的物质的量为
④标准状况下,224mL的氨气中含有的氢原子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g) Fe3O4+4H2。该反应中H2O作
Fe3O4+4H2。该反应中H2O作__________ (填“氧化剂”或“还原剂”);
(2)检验某溶液中是否含有 ,先加盐酸,再加
,先加盐酸,再加______ (填“BaCl2”或“NaCl);
(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是__________ (填“生石灰”或“盐酸”)。
(4)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式:2Na2O2 + 2______ = 2Na2 CO3 +O2 ↑;
(5)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有________ (填“钠”或“钾”)元素;
 Fe3O4+4H2。该反应中H2O作
Fe3O4+4H2。该反应中H2O作(2)检验某溶液中是否含有
 ,先加盐酸,再加
,先加盐酸,再加(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是
(4)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式:2Na2O2 + 2
(5)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有
您最近一年使用:0次
【推荐3】近来,《饮用天然矿泉水》新标准引起热议,其中备受争议的溴酸盐是一种致癌物,新标准中溴酸盐限值为0.01mg/L。已知在酸性条件下有以下反应:
①2BrO3-+I2→2IO3-+Br2;
②2IO3-+10Br-+12H+→I2+5Br2+6H2O;
③5Br-+BrO3-+6H+→3Br2+3H2O。
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由___ 。
(2)反应②中:IO3-→I2发生的是___ 反应(选填“氧化”、“还原”)。
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图所示关系:
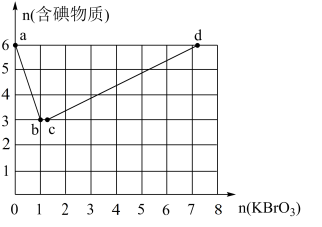
(3)a→b阶段的反应为(写出产物并配平)I-+BrO3-+H+→___ 。
(4)b→c阶段为反应③,其中氧化产物和还原产物的物质的量之比为___ 。
①2BrO3-+I2→2IO3-+Br2;
②2IO3-+10Br-+12H+→I2+5Br2+6H2O;
③5Br-+BrO3-+6H+→3Br2+3H2O。
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由
(2)反应②中:IO3-→I2发生的是
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图所示关系:

(3)a→b阶段的反应为(写出产物并配平)I-+BrO3-+H+→
(4)b→c阶段为反应③,其中氧化产物和还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl H2O2+NaCl
H2O2+NaCl
B.Ag2O+H2O2 Ag+O2↑+H2O
Ag+O2↑+H2O
C.H2O2 H2O+O2↑
H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2O
H2O2仅体现氧化性的反应是___________ (填序号,下同),H2O2仅体现还原性的反应是___________ ,H2O2既体现氧化性又体现还原性的反应是___________ ,H2O2既不做氧化剂又不做还原剂的反应是___________ 。
(2)已知常温下在溶液中可发生如下两个反应:
Br2+2Fe2+=2Fe3++2Br-
2I-+2Fe3+=2Fe2++I2
由此可以确定Br2、I2、Fe3+的氧化性由强到弱的顺序是___________
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
①氧化剂是___________ ,还原剂是___________ 。
②氧化剂与还原剂的分子个数比为___________ 。
③当有68 g NH3参加反应时,被氧化的物质为___________ g,生成的还原产物为___________ g。
A.Na2O2+HCl
 H2O2+NaCl
H2O2+NaClB.Ag2O+H2O2
 Ag+O2↑+H2O
Ag+O2↑+H2OC.H2O2
 H2O+O2↑
H2O+O2↑D.H2O2+Cr2(SO4)3+KOH
 K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2OH2O2仅体现氧化性的反应是
(2)已知常温下在溶液中可发生如下两个反应:
Br2+2Fe2+=2Fe3++2Br-
2I-+2Fe3+=2Fe2++I2
由此可以确定Br2、I2、Fe3+的氧化性由强到弱的顺序是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
①氧化剂是
②氧化剂与还原剂的分子个数比为
③当有68 g NH3参加反应时,被氧化的物质为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题。
(1)现有中学化学中常见的九种物质:①氢氧化钡固体②铁丝③氯化氢气体④纯醋酸⑤二氧化碳气体⑥碳酸氢钾固体⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠。按要求填空(填序号)。
上述状态下可导电的是___________ ,属于非电解质的是___________ 。写出⑦在水溶液中的电离方程式___________ ;写出②与③的水溶液反应的离子方程式___________ 。
(2)已知 与浓盐酸室温下可发生如下反应:
与浓盐酸室温下可发生如下反应:
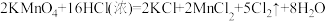 ,氧化剂和还原剂的物质的量之比为
,氧化剂和还原剂的物质的量之比为___________ ,生成标准状况下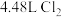 ,时消耗的
,时消耗的 的物质的量为
的物质的量为___________ 。
(3)质量比为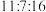 的
的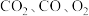 ,其物质的量之比为
,其物质的量之比为___________ 。
(4)某盐混合溶液中含有离子: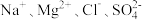 ,测得
,测得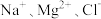 的物质的量浓度依次为:
的物质的量浓度依次为: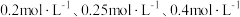 ,则
,则
___________ 。
(1)现有中学化学中常见的九种物质:①氢氧化钡固体②铁丝③氯化氢气体④纯醋酸⑤二氧化碳气体⑥碳酸氢钾固体⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠。按要求填空(填序号)。
上述状态下可导电的是
(2)已知
 与浓盐酸室温下可发生如下反应:
与浓盐酸室温下可发生如下反应: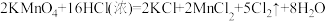 ,氧化剂和还原剂的物质的量之比为
,氧化剂和还原剂的物质的量之比为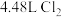 ,时消耗的
,时消耗的 的物质的量为
的物质的量为(3)质量比为
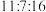 的
的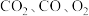 ,其物质的量之比为
,其物质的量之比为(4)某盐混合溶液中含有离子:
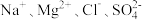 ,测得
,测得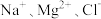 的物质的量浓度依次为:
的物质的量浓度依次为: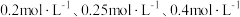 ,则
,则
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关的离子方程式为_______ 。
(4)原溶液可能大量共存的阴离子是_______(填字母)。
(5)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目_______ 。
②若消耗30 g的NO得到还原产物的质量为_______ g。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是_______(填字母)。
| A.OH- | B. | C. | D.Cl- |
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②若消耗30 g的NO得到还原产物的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、酸性KMnO4溶液、MnO2。该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X和一定量O2,该同学推测反应中可能生成了H2O2,并进行实验探究。
(1)写出Na2O2与水反应的化学方程式_______________________________________ 。
(2)试设计实验证明溶液X中含过氧化氢____________________________________ 。
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:______ H2O2+______ Fe2++_____ OH-===______ Fe(OH)3↓,该反应中H2O2表现了_______ (填“氧化”或“还原”)性。
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了______ (填“氧化”或“还原”)性。该反应的离子方程式为____________________ 。
(1)写出Na2O2与水反应的化学方程式
(2)试设计实验证明溶液X中含过氧化氢
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产生活中有很多实际应用:
Ⅰ.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;②2SO2+SeO2+2H2O=Se+2SO +4H+。
+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是_______ 还原剂是________ 。
(2)依据反应①判断SeO2、浓H2SO4的氧化性强弱是:SeO2______ 浓H2SO4(填大于、小于或等于).
(3)用双线桥法标出反应②电子转移的方向和数目:_________________ 。
(4)SeO2、KI和HNO3发生如下反应,配平该反应的化学方程式____________ 。
SeO2+KI+HNO3→Se+I2+KNO3+H2O
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(5)含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为_____________________________________________ 。
(6)硫酸铜溶液能与单质磷反应:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应中,被1mol CuSO4 氧化的P的物质的量__________ 。
Ⅰ.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;②2SO2+SeO2+2H2O=Se+2SO
 +4H+。
+4H+。(1)Se与浓H2SO4的反应中,氧化剂是
(2)依据反应①判断SeO2、浓H2SO4的氧化性强弱是:SeO2
(3)用双线桥法标出反应②电子转移的方向和数目:
(4)SeO2、KI和HNO3发生如下反应,配平该反应的化学方程式
SeO2+KI+HNO3→Se+I2+KNO3+H2O
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(5)含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO
 ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为(6)硫酸铜溶液能与单质磷反应:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应中,被1mol CuSO4 氧化的P的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)写出Mg在CO2中燃烧的化学方程式__________________________________ 。
(2)最近报纸上报导了有人混用洗涤剂发生了中毒事件,当事人先用洁厕灵(强酸性,含盐酸)洗卫生间,再用84消毒液(含NaClO)进行杀菌。
请写出涉及反应的离子方程式______________________________________ 。
(3)碱金属能形成离子型氢化物。如氢化钠的化学式为NaH,其中H-具有较强的还原性。
常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为___________________________ 。
NaH能与水剧烈反应生成对应的碱和氢气,该反应中氧化产物和还原产物的质量比为_____________ 。
(2)最近报纸上报导了有人混用洗涤剂发生了中毒事件,当事人先用洁厕灵(强酸性,含盐酸)洗卫生间,再用84消毒液(含NaClO)进行杀菌。
请写出涉及反应的离子方程式
(3)碱金属能形成离子型氢化物。如氢化钠的化学式为NaH,其中H-具有较强的还原性。
常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为
NaH能与水剧烈反应生成对应的碱和氢气,该反应中氧化产物和还原产物的质量比为
您最近一年使用:0次

 )是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法: (未配平)
(未配平)


