回答下列问题。
(1)下表是元素周期表的一部分,将 Na、Mg、Al 三种元素填入相应位置。___________
(2)Na、Mg、Al这三种元素中,原子半径由大到小的顺序是___________ 。
(3)由于金属离子的氧化性强弱存在差异,使得它们被还原为单质的难易程度不同,因此金属冶炼的方法不同,活泼金属常用电解法冶炼。下列金属需要使用电解法冶炼的是___________。
(1)下表是元素周期表的一部分,将 Na、Mg、Al 三种元素填入相应位置。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | ||||||||
| 三 | ||||||||
(2)Na、Mg、Al这三种元素中,原子半径由大到小的顺序是
(3)由于金属离子的氧化性强弱存在差异,使得它们被还原为单质的难易程度不同,因此金属冶炼的方法不同,活泼金属常用电解法冶炼。下列金属需要使用电解法冶炼的是___________。
| A.Na | B.Fe | C.Cu | D.Au |
更新时间:2024-02-23 18:27:23
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答
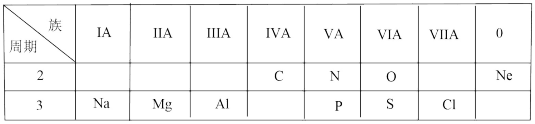
(1)镁元素位于元素周期表中第___ 周期_____ 族;
(2)空气组成中体积分数最大的气体是_____ ;
(3)O与S相比,原子半径较小的是____ ;
(4)金刚石的组成元素是________ ;
(5)单质的化学性质最不活泼的元素是______ ;
(6)Na与Mg元素相比金属性较强的是_________
(7)NH3与PH3相比,热稳定性较弱的是______
(8)H2SO4与H3PO4相比酸性较强的是______
(9)Mg(OH)2与Al(OH)3其中属于两性氢氧化物的是________
(10)单质呈黄绿色的气体组成元素是_____ ,其单质的水溶液呈__ (填“酸性或“碱性”)。

(1)镁元素位于元素周期表中第
(2)空气组成中体积分数最大的气体是
(3)O与S相比,原子半径较小的是
(4)金刚石的组成元素是
(5)单质的化学性质最不活泼的元素是
(6)Na与Mg元素相比金属性较强的是
(7)NH3与PH3相比,热稳定性较弱的是
(8)H2SO4与H3PO4相比酸性较强的是
(9)Mg(OH)2与Al(OH)3其中属于两性氢氧化物的是
(10)单质呈黄绿色的气体组成元素是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第____ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的____ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是___ (填“H”或“O”)。
(4)Na的最高价氧化物的化学式为____ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物的化学式为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】(1)表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界________ 。
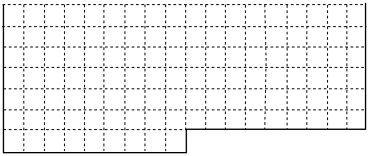
(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)
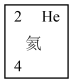
写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:________ >________ (用元素符号表示),甲、乙的最高价氧化物水化物相互反应的离子方程式为:________
(4)元素周期表体现了元素周期律,即元素的性质随着_________ 的递增呈现____ 的变化。

(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)

写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:
(4)元素周期表体现了元素周期律,即元素的性质随着
您最近一年使用:0次
【推荐2】 在元素周期表中的位置是第
在元素周期表中的位置是第___________ 周期___________ 族,除去稀有气体,Cu元素所在周期原子半径最小的元素是___________ (填写元素符号);元素周期表中电负性大于氧元素的是___________ (填写元素符号)。
 在元素周期表中的位置是第
在元素周期表中的位置是第
您最近一年使用:0次
【推荐3】合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的核外电子排布式为______ ,占据最高能级电子的电子云轮廓图为______ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性由大到小的顺序为______ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是______ 。
②比较Mg、Ca的第一电离能:I1(Mg)______ (填“大于”或“小于”)I1(Ca)。
(3)我国科研人员研制出了“Fe-LiH”催化剂,温度、压强分别降到了350℃、1MPa。这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的价电子排布图为______ ,铁在元素周期表中的位置_____ 。
②比较Li+与H-的半径大小关系:r(H-)______ r(Li+)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的核外电子排布式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性由大到小的顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca的第一电离能:I1(Mg)
(3)我国科研人员研制出了“Fe-LiH”催化剂,温度、压强分别降到了350℃、1MPa。这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的价电子排布图为
②比较Li+与H-的半径大小关系:r(H-)
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】依据《第四章化学反应与电能》所学知识填空。
(1)把___________ 的装置叫做电解池。
(2)金属冶炼就是使矿石中的金属离子___________ 的过程。
(3)金属与其表面接触的一些物质(如O2、Cl2、SO2等)___________ 而引起的腐蚀,叫做化学腐蚀。当___________ 时会发生原电池反应,比较活泼的金属发生氧化反应而被腐蚀,这种腐蚀叫做电化学腐蚀。
(4)由于条件不同,钢铁腐蚀可分为___________ 和___________ 。金属的防护措施包括改变金属材料的组成、___________ 、电化学保护法,其中电化学保护法包括___________ 和___________ 。
(1)把
(2)金属冶炼就是使矿石中的金属离子
(3)金属与其表面接触的一些物质(如O2、Cl2、SO2等)
(4)由于条件不同,钢铁腐蚀可分为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】湿法冶炼与火法冶炼相比,湿法冶炼工艺的优点有_______ 。
您最近一年使用:0次




