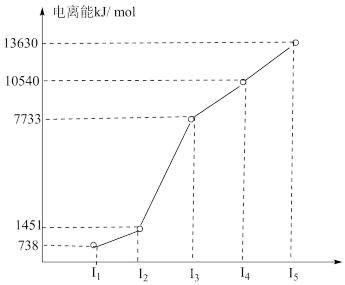
合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的核外电子排布式为______ ,占据最高能级电子的电子云轮廓图为______ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性由大到小的顺序为______ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是______ 。
②比较Mg、Ca的第一电离能:I1(Mg)______ (填“大于”或“小于”)I1(Ca)。
(3)我国科研人员研制出了“Fe-LiH”催化剂,温度、压强分别降到了350℃、1MPa。这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的价电子排布图为______ ,铁在元素周期表中的位置_____ 。
②比较Li+与H-的半径大小关系:r(H-)______ r(Li+)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的核外电子排布式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性由大到小的顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca的第一电离能:I1(Mg)
(3)我国科研人员研制出了“Fe-LiH”催化剂,温度、压强分别降到了350℃、1MPa。这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的价电子排布图为
②比较Li+与H-的半径大小关系:r(H-)
更新时间:2023-04-23 14:07:07
|
相似题推荐
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】下表为元素周期表的一部分,参照元素①-⑧在表中的位置,请回答下列问题。

(1)元素③单质的化学式为_______ ,由①②组成且含有非极性键的物质的结构式为_______ 。
(2)④-⑧5种元素所形成的最高价氧化物的水化物中,属于中强酸的是_______ (填化学式)。
(3)②、⑤、⑥、⑧的简单离子半径由大到小的顺序为_______ (用离子符号和“>”表示)。

(1)元素③单质的化学式为
(2)④-⑧5种元素所形成的最高价氧化物的水化物中,属于中强酸的是
(3)②、⑤、⑥、⑧的简单离子半径由大到小的顺序为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】下表是元素周期表的一部分,根据表中给出的10种元素,用元素符号 或化学式 回答下列问题:
(1)金属性最强的短周期元素是___________ ;化学性质最不活泼的单质是___________ ;
(2)Ca的最外层电子数为___________ ;
(3)表中元素最高价氧化物对应水化物酸性最强的酸是___________ ;
(4)某离子的原子结构示意图为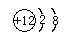 ,其对应的离子符号是
,其对应的离子符号是___________ ;
(5)硫有两种重要氧化物,分别为SO2和___________ (填化学式);
(6)H2S和HCl中,热稳定性较强的是___________ ;
(7)Si是带来人类文明的重要物质之一,晶体硅的主要用途是___________ (写出其中一种),其氧化物的化学式为___________ ;
(8)钠、铝最高价氧化物对应水化物之间反应的化学方程式是___________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)Ca的最外层电子数为
(3)表中元素最高价氧化物对应水化物酸性最强的酸是
(4)某离子的原子结构示意图为
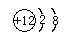 ,其对应的离子符号是
,其对应的离子符号是(5)硫有两种重要氧化物,分别为SO2和
(6)H2S和HCl中,热稳定性较强的是
(7)Si是带来人类文明的重要物质之一,晶体硅的主要用途是
(8)钠、铝最高价氧化物对应水化物之间反应的化学方程式是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
(1)元素②的原子结构示意图为_____ 。
(2)元素③、④、⑤、⑥原子半径由大到小为_____ 。
(3)上述 8 种元素中,非金属性最强的是_____ 。
(4)元素②、③形成的气态氢化物稳定性:_____ >_____ ;元素①、③、⑤可形成既含离子键又含极性共价键的化合物,写出其电子式:_____ 。
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的离子方程式为_____ 。
(6)写出金属铜与②最高价氧化物对应的水化物稀溶液反应的离子方程式_____ 。
(7)从原子结构的角度解释元素③和⑦的非金属性强弱:_____
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素③、④、⑤、⑥原子半径由大到小为
(3)上述 8 种元素中,非金属性最强的是
(4)元素②、③形成的气态氢化物稳定性:
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的离子方程式为
(6)写出金属铜与②最高价氧化物对应的水化物稀溶液反应的离子方程式
(7)从原子结构的角度解释元素③和⑦的非金属性强弱:
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】(1)基态氮原子的价电子排布式为___ 。
(2)Cu原子价电子轨道表示式为___ 。
(2)Cu原子价电子轨道表示式为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态锰的价层电子排布式为___________ 。
您最近一年使用:0次
【推荐1】K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是___________ ,各元素的第一电离能由大到小的顺序为___________ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】元素的第一电离能:Al_________ Si(填“>”或 “<”)
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CulnSe等。
(1)Se在元素周期表中的位置为_______ ,硅的基态原子电子排布式为_______ ,基态Ga原子核外电子占据的最高能级为_______ ,铜的基态原子价电子轨道表达式为_______ 。
(2)P、S、Ga的电负性从大到小的顺序为_______ 。
(3)与A1元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为____ (标出配位键)。
(4)已知[Cu(NH3)4]2+具有对称的空间结构,[Cu(NH3)4]2+中的2个NH3被Cl-取代,能得到2种不同结构的产物,则[Cu(NH3)]2+的空间构型为_______
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是_______ 。
(1)Se在元素周期表中的位置为
(2)P、S、Ga的电负性从大到小的顺序为
(3)与A1元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为
(4)已知[Cu(NH3)4]2+具有对称的空间结构,[Cu(NH3)4]2+中的2个NH3被Cl-取代,能得到2种不同结构的产物,则[Cu(NH3)]2+的空间构型为
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
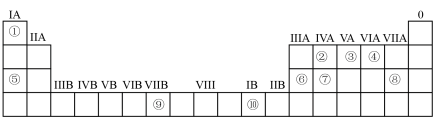
【推荐2】下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,回答下列问题:___________ (用元素符号表示)。
(2)④、⑤、⑥的原子半径由大到小的顺序为___________ (用元素符号表示);
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________ (用化学式表示)。
(4)①、④、⑤、⑧中的某些 元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___________ 。
(5)第一电离能 :
: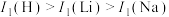 ,原因是
,原因是___________ 。
(6)基态⑧原子占据的最高能级的电子云轮廓图的形状是___________ 形;基态⑨原子的价层电子排布的轨道表示式为___________ ;元素⑩属于___________ 区(填“s”、“d”、“ds”或“p”)。
(7)由④元素形成的常见物质有很多,例如: 、
、 、
、 等,基态④原子的核外电子排布式是
等,基态④原子的核外电子排布式是___________ ,对 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测: 分子中
分子中___________ (填字母序号),确定其结构一定不是甲。
a. 键长 b.
键长 b. 键能 c.
键能 c. 键角
键角
(2)④、⑤、⑥的原子半径由大到小的顺序为
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(4)①、④、⑤、⑧中的
(5)第一电离能
 :
: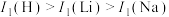 ,原因是
,原因是(6)基态⑧原子占据的最高能级的电子云轮廓图的形状是
(7)由④元素形成的常见物质有很多,例如:
 、
、 、
、 等,基态④原子的核外电子排布式是
等,基态④原子的核外电子排布式是 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测: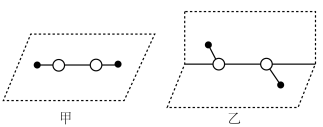
 分子中
分子中a.
 键长 b.
键长 b. 键能 c.
键能 c. 键角
键角
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】(1) 中,电负性最高的元素是
中,电负性最高的元素是______ 。
(2)C、H、O三种元素的电负性由小到大的顺序为______ 。
(3)光催化还原 制备
制备 反应中,带状纳米
反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______ 。
(4)A、B、C、D为原子序数依次增大的四种元素, 和
和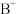 具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。四种元素中电负性最大的是
具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。四种元素中电负性最大的是______ (填元素符号),其中C原子的核外电子排布式为______ 。
 中,电负性最高的元素是
中,电负性最高的元素是(2)C、H、O三种元素的电负性由小到大的顺序为
(3)光催化还原
 制备
制备 反应中,带状纳米
反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是(4)A、B、C、D为原子序数依次增大的四种元素,
 和
和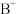 具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。四种元素中电负性最大的是
具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。四种元素中电负性最大的是
您最近一年使用:0次