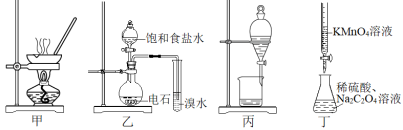
测定CrCl3产品的纯度,实验如下:
①取mg CrCl3产品,在强碱性条件下,加入过量30%H2O2溶液,小火加热使CrCl3完全转化为CrO ,继续加热一段时间;
,继续加热一段时间;
②冷却后,滴入适量的稀硫酸和浓磷酸,使CrO 转化为Cr2O
转化为Cr2O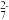 ,加适量的蒸馏水配成250.00mL溶液;
,加适量的蒸馏水配成250.00mL溶液;
③取25.00mL溶液,用新配制的 的NH4)2Fe(SO4)2标准溶液滴定至终点,重复3次,平均消耗NH4)2Fe(SO4)2标准溶液VmL(已知Cr2O
的NH4)2Fe(SO4)2标准溶液滴定至终点,重复3次,平均消耗NH4)2Fe(SO4)2标准溶液VmL(已知Cr2O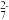 被
被 还原为Cr3+)。
还原为Cr3+)。
则样品中CrCl3 (摩尔质量为M g·molˉ1)的质量分数为___________ %;若步骤③中所用标准溶液已变质,将导致CrCl3质量分数测定值___________ (填“偏高”、“偏低”或“无影响”)。
①取mg CrCl3产品,在强碱性条件下,加入过量30%H2O2溶液,小火加热使CrCl3完全转化为CrO
 ,继续加热一段时间;
,继续加热一段时间;②冷却后,滴入适量的稀硫酸和浓磷酸,使CrO
 转化为Cr2O
转化为Cr2O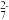 ,加适量的蒸馏水配成250.00mL溶液;
,加适量的蒸馏水配成250.00mL溶液;③取25.00mL溶液,用新配制的
 的NH4)2Fe(SO4)2标准溶液滴定至终点,重复3次,平均消耗NH4)2Fe(SO4)2标准溶液VmL(已知Cr2O
的NH4)2Fe(SO4)2标准溶液滴定至终点,重复3次,平均消耗NH4)2Fe(SO4)2标准溶液VmL(已知Cr2O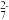 被
被 还原为Cr3+)。
还原为Cr3+)。则样品中CrCl3 (摩尔质量为M g·molˉ1)的质量分数为
2024高三下·全国·专题练习 查看更多[1]
(已下线)题型二 实验中常考滴定计算-备战2024年高考化学答题技巧与模板构建
更新时间:2024-02-29 19:25:59
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】食醋是烹饪美食的调味品,有效成分主要为醋酸. 的应用与其电离平衡密切相关.25℃时,
的应用与其电离平衡密切相关.25℃时, 的
的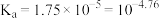 ;
;
(1)用化学用语表示 溶液呈碱性的原因
溶液呈碱性的原因__________________ (用离子方程式表示);
(2)下列方法中,可以使醋酸溶液中 电离程度增大的是___________;
电离程度增大的是___________;
(3)用 溶液分别滴定体积均为20mL、浓度均为
溶液分别滴定体积均为20mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入
的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入 溶液体积而变化的两条滴定曲线;
溶液体积而变化的两条滴定曲线;
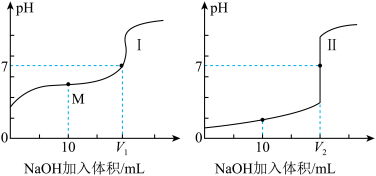
①滴定醋酸的曲线是____________ (填“Ⅰ”或“Ⅱ”);
②在上述滴定过程中,不需要使用的玻璃仪器是___________ (填序号);
A.容量瓶 B.碱式滴定管 C.锥形瓶 D.胶头滴管
③图1中M点,溶液中各离子浓度由大到小的顺序是___________ (用符号“c”及“>”表示),此时溶液中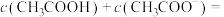
____________ ;(精确到小数点后三位数字)
(4)用 的盐酸滴定20.00mL未知浓度的
的盐酸滴定20.00mL未知浓度的 溶液.下列操作会使测定结果偏低的是___________;
溶液.下列操作会使测定结果偏低的是___________;
 的应用与其电离平衡密切相关.25℃时,
的应用与其电离平衡密切相关.25℃时, 的
的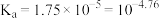 ;
;(1)用化学用语表示
 溶液呈碱性的原因
溶液呈碱性的原因(2)下列方法中,可以使醋酸溶液中
 电离程度增大的是___________;
电离程度增大的是___________;| A.滴加少量浓盐酸 | B.微热溶液 | C.加水稀释 | D.加入少量醋酸钠晶体 |
(3)用
 溶液分别滴定体积均为20mL、浓度均为
溶液分别滴定体积均为20mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入
的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入 溶液体积而变化的两条滴定曲线;
溶液体积而变化的两条滴定曲线;
①滴定醋酸的曲线是
②在上述滴定过程中,不需要使用的玻璃仪器是
A.容量瓶 B.碱式滴定管 C.锥形瓶 D.胶头滴管
③图1中M点,溶液中各离子浓度由大到小的顺序是
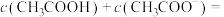
(4)用
 的盐酸滴定20.00mL未知浓度的
的盐酸滴定20.00mL未知浓度的 溶液.下列操作会使测定结果偏低的是___________;
溶液.下列操作会使测定结果偏低的是___________;A.量取 溶液的碱式滴定管未用待测碱液润洗 溶液的碱式滴定管未用待测碱液润洗 |
| B.酸式滴定管未用标准盐酸润洗 |
| C.滴定过程中滴定管内不慎有标准液溅出 |
| D.滴定前俯视读数,滴定后读数正确 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】CH3COONa溶液是常见的强碱弱酸盐溶液,可由醋酸和NaOH溶液反应得到。
(1)用离子方程式解释CH3COONa水溶液呈碱性的原因___________ 。
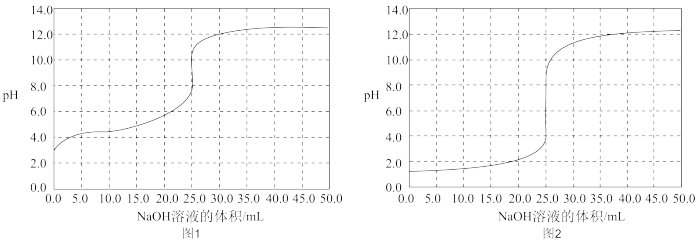
(2)用0.1000mol/L NaOH分别滴定25.00mL 0.1000mol/L盐酸和25.00mL 0.1000mol/L醋酸,滴定过程中pH变化曲线如下图所示。
①在上述滴定过程中,不需要 使用的玻璃仪器是___________ (填序号)。
A.容量瓶 B.碱式滴定管 C.锥形瓶 D.胶头滴管
②由图中数据可判断滴定盐酸的pH变化曲线为图2,判断的理由如下(答出2点):
ⅰ.起始未滴加NaOH溶液时,___________ 。
ⅱ.___________ 。
③滴定CH3COOH溶液的过程中,当滴加12.50mL NaOH溶液时,溶液中各离子浓度由大到小的顺序是___________ (用符号“c”及“>”表示)。
(3)向0.1mol/LCH3COONa溶液中逐滴加入0.1mol/L盐酸至恰好反应。反应过程中,你认为CH3COONa的水解平衡向___________ (填“左”或“右”)移动,分析的过程:当滴入稀盐酸后,___________ 。
(1)用离子方程式解释CH3COONa水溶液呈碱性的原因
(2)用0.1000mol/L NaOH分别滴定25.00mL 0.1000mol/L盐酸和25.00mL 0.1000mol/L醋酸,滴定过程中pH变化曲线如下图所示。

①在上述滴定过程中,
A.容量瓶 B.碱式滴定管 C.锥形瓶 D.胶头滴管
②由图中数据可判断滴定盐酸的pH变化曲线为图2,判断的理由如下(答出2点):
ⅰ.起始未滴加NaOH溶液时,
ⅱ.
③滴定CH3COOH溶液的过程中,当滴加12.50mL NaOH溶液时,溶液中各离子浓度由大到小的顺序是
(3)向0.1mol/LCH3COONa溶液中逐滴加入0.1mol/L盐酸至恰好反应。反应过程中,你认为CH3COONa的水解平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】亚氯酸钠(NaClO2)是重要漂白剂。测定某产品中NaClO2纯度的实验操作如下:准确称取1.00g样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应:ClO +4I-+4H+=2H2O+2I2+Cl-。将所得混合液稀释成100mL待测溶液。用
+4I-+4H+=2H2O+2I2+Cl-。将所得混合液稀释成100mL待测溶液。用_______ (填“酸式”或“碱式”)滴定管量取25.00mL待测溶液置于锥形瓶中,加入淀粉溶液作指示剂,用0.5000mol•L-1Na2S2O3标准液滴定(已知:I2+2S2O =2I-+S4O
=2I-+S4O ),当
),当_______ ,即为滴定终点;平行滴定3次,测得消耗标准溶液体积的平均用量为20.00mL。所称取的样品中NaClO2质量百分含量为_______ 。
 +4I-+4H+=2H2O+2I2+Cl-。将所得混合液稀释成100mL待测溶液。用
+4I-+4H+=2H2O+2I2+Cl-。将所得混合液稀释成100mL待测溶液。用 =2I-+S4O
=2I-+S4O ),当
),当
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。但二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。
(1)欧洲国家主要采用氯酸钠氧化浓盐酸制备ClO2,缺点主要是产率低,产品难以分离,还产生毒副产品。该反应的化学反应方程式为:______________ 。科学家又研究出了一 种新的制备ClO2的方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为___________ ,此法提高了生产及储存、运输的安全性,原因是___________________________ 。
(2)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg∙L−1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
I.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液.(已知:2 +I2=
+I2= +2I-)
+2I-)
III.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示。
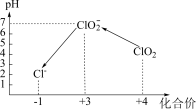
请回答:
①操作I中反应的离子方程式是_____________________________ 。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是_______________ 。
③若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10−3 mol∙L−1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是________________________ mg∙L−1。
(1)欧洲国家主要采用氯酸钠氧化浓盐酸制备ClO2,缺点主要是产率低,产品难以分离,还产生毒副产品。该反应的化学反应方程式为:
(2)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg∙L−1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
I.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液.(已知:2
 +I2=
+I2= +2I-)
+2I-)III.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示。

请回答:
①操作I中反应的离子方程式是
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是
③若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10−3 mol∙L−1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】实验室常以硫酸亚铁和草酸为原料制备草酸亚铁(FeC2O4·2H2O)。通过测定产品中Fe2+和C2O 的含量来判断晶体的纯度,其测定过程示意图如图。
的含量来判断晶体的纯度,其测定过程示意图如图。
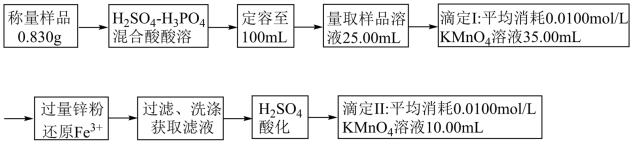
(1)KMnO4标准溶液应盛放在___________ 滴定管(填“酸式”或“碱式”)。
(2)滴定在65~85℃进行,应采取的加热方式为___________ 。
(3)H3PO4可与Fe3+形成无色的[Fe(HPO4)]+,使滴定的终点更容易判断。滴定终点的现象是___________ 。
(4)“滴定Ⅰ”是为了测定n(Fe2+)和n(C2O )的总量,以下操作会导致结果偏高的是___________。
)的总量,以下操作会导致结果偏高的是___________。
(5)为促使Fe3+全部转化成Fe2+,锌粉必须大大过量。
①锌粉加入后,发生的反应有Zn+2H+=Zn2++H2↑、___________ 。
②“过滤”、“洗涤”操作会导致所测得的n(Fe2+)偏低的原因有___________ 。
 的含量来判断晶体的纯度,其测定过程示意图如图。
的含量来判断晶体的纯度,其测定过程示意图如图。
(1)KMnO4标准溶液应盛放在
(2)滴定在65~85℃进行,应采取的加热方式为
(3)H3PO4可与Fe3+形成无色的[Fe(HPO4)]+,使滴定的终点更容易判断。滴定终点的现象是
(4)“滴定Ⅰ”是为了测定n(Fe2+)和n(C2O
 )的总量,以下操作会导致结果偏高的是___________。
)的总量,以下操作会导致结果偏高的是___________。| A.未用KMnO4标准溶液润洗滴定管 | B.滴定终点时,仰视刻度线 |
| C.滴定终点时,发现滴定管中出现气泡 | D.滴定时间过长 |
①锌粉加入后,发生的反应有Zn+2H+=Zn2++H2↑、
②“过滤”、“洗涤”操作会导致所测得的n(Fe2+)偏低的原因有
您最近一年使用:0次