科学家设计了一种以石墨为正极的高容量可充电Li/Cl2电池,原理如图所示。氯化铝(AlCl3)溶解在亚硫酰氯(SOCl2)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
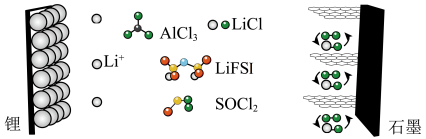
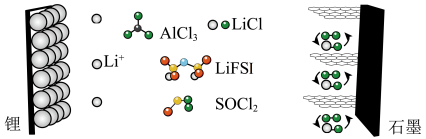
| A.放电时,电解质溶液可以是AlCl3水溶液 |
| B.放电时,石墨极的电极反应式为Cl2+2e-+2Li+=2LiCl |
| C.充电时,石墨极与电源负极连接 |
| D.充电时,转移2NA个电子时锂电极理论上消耗7g锂 |
2024·云南昆明·三模 查看更多[2]
更新时间:2024-03-02 14:24:03
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】NA为阿伏加 德罗常数的值,下列叙述正确的是
| A.1.0L1.0molL—1的H2SO4水溶液中含有的氧原子数为4NA |
| B.273K、101kPa下,22.4L甲烷和氧气的混合气体燃烧后,产物的分子总数一定为NA |
| C.25℃时pH=13的NaOH溶液中含有OH—的数目为0.1NA |
| D.1 mol Na与氧气完全反应得到Na2O与Na2O2的混合物时失去的电子数一定为NA |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列叙述正确的是
| A.Al与足量稀硫酸反应,转移电子数目为3NA |
| B.1 mol KMnO4被还原为Mn2+转移的电子数为5NA |
| C.标准状况下,22.4 L CCl4中含C-Cl键的数目为4NA |
| D.常温下,5.6 g铁与足量浓硫酸反应,转移的电子数目为0.3NA |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1mol的11B中,含有0.6NA个中子 |
| B.pH=1的H3PO4溶液中,含有0.1NA个H+ |
| C.2.24L(标准状况)苯(C6H6)在O2中完全燃烧,得到0.6NA个CO2分子 |
| D.2.4gMg与H2SO4完全反应,转移的电子数为0.1NA |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】如图是NO2和O2形成的原电池装置。下列说法不正确的是
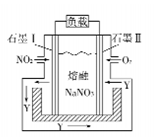

| A.石墨Ⅱ做正极,O2发生还原反应 |
| B.该电池放电时NO3-从右侧向左侧迁移 |
| C.当消耗1mol NO2时,电解质中转移1mol e |
| D.石墨Ⅰ附近发生的反应为NO2+NO3--e-=N2O5 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】碱性电池具有容量、放电电流大的特点。锌锰碱性电池以氢氧化钾溶液为电解质,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。下列说法不正确 的是
| A.该电池属于一次电池,已使用过的电池需放到专门的电池回收箱中 |
| B.原电池工作时,正极的极反应式为:2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电解质氢氧化钾溶液中阳离子迁移到电池的正极 |
| D.电池工作时,Zn为负极,负极区pH变大 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】纤维素乙醇燃料是一种绿色、可再生的新能源,利用地球上广泛存在的纤维素质生物原料生产清洁的乙醇燃料制成燃料电池。下图是绿色电源“乙醇燃料电池”的工作原理示意图(a、b均为多孔性石墨电极)。该电池工作时,下列说法错误的是
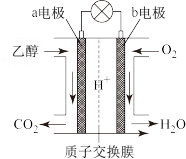

| A.该电池工作时是把化学能转化为电能 | B.H+通过质子交换膜从a极区移向b极区 |
C.a电极反应式为C2H5OH-12e- +16OH-=2CO +11H2O +11H2O | D.电池工作时,消耗标准状况下6.72LO2,外电路中转移电子数为1.2NA |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】2019年诺贝尔化学奖授予在锂离子电池的发展方面作出贡献的三位科学家。国内某科技研究小组首次提出一种新型的Li+电池体系,该体系正极采用含有I-、Li+的水溶液,负极采用固体有机聚合物,电解质溶液为LiNO3溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图所示)。已知I3-在水溶液中量黄色,则下列有关判断正确的是( )
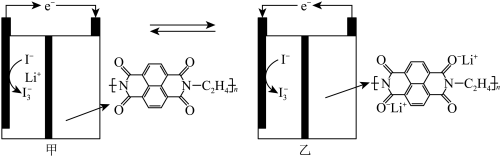

| A.图甲是原电池工作原理图,图乙是电池充电原理图 |
| B.放电时,正极液态电解质溶液的颜色变浅 |
| C.充电时,Li+从右向左通过聚合物离子交换膜 |
D.放电时,负极的电极反应式为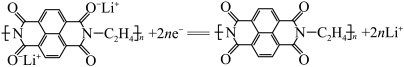 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.铅蓄电池放电时负极质量减轻,充电时阳极质量增加 |
| B.同温下,0.1 mol·L-1醋酸溶液pH=a,0.01 mol·L-1醋酸溶液pH=b,则a+1<b |
| C.钢铁水闸可用牺牲阳极的阴极保护法或外加电流的阴极保护法进行防护 |
D.一定条件下反应N2+3H2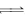 2NH3,当3v正(H2)=2v逆(NH3),则反应达到平衡 2NH3,当3v正(H2)=2v逆(NH3),则反应达到平衡 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列两个装置中,液体体积均为200mL,开始时电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线上都通过了0.02 mol电子,若不考虑溶液体积的变化,下列叙述中正确的是
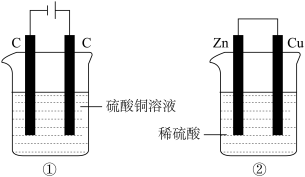

| A.产生气体体积①=② |
| B.溶液的pH变化:①减小②增大 |
| C.电极上析出固体质量①<② |
| D.电极反应式:①中阳极Cu2++2e—=Cu,②中负极Zn—2e—=Zn2+ |
您最近半年使用:0次