已知A是一种常见金属,B的俗称为磁性氧化铁,C溶液呈浅绿色。试根据图中转化关系,回答下列问题。
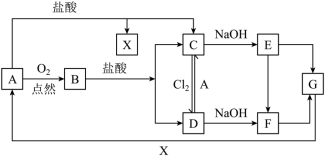
(1)写出B和G的化学式:B___________ 、G___________ 。
(2)检验D中少量阳离子的最佳试剂的化学式是___________ 。
(3)写出下列转化的化学方程式:
①C→D___________ ;
②G→A___________ 。
(4)E在空气中放置容易转化为F,该反应的化学方程式为______ ;产生的现象为________ 。
(5)在有氧条件下,Fe3O4在含Cl-溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:________ 。
4Fe3O4+O2+ ___________+
___________+ H2O=
H2O= FeOCl+
FeOCl+ ___________。
___________。

(1)写出B和G的化学式:B
(2)检验D中少量阳离子的最佳试剂的化学式是
(3)写出下列转化的化学方程式:
①C→D
②G→A
(4)E在空气中放置容易转化为F,该反应的化学方程式为
(5)在有氧条件下,Fe3O4在含Cl-溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:
4Fe3O4+O2+
 ___________+
___________+ H2O=
H2O= FeOCl+
FeOCl+ ___________。
___________。
更新时间:2024-03-02 15:52:35
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】次锰酸根离子 ,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分
,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的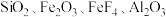 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
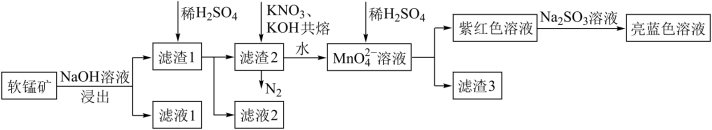
(1)滤渣1的主要成分是____ , 在周期表中的位置
在周期表中的位置___ 。
(2)流程中共熔时发生的主要反应的化学方程式为____ 。
(3)写出 转变为紫红色溶液的离子反应方程式
转变为紫红色溶液的离子反应方程式____ 。
(4)整个流程中的__ (填化学式)能重复利用。
(5) 还原软锰矿制备
还原软锰矿制备 的化学方程式为
的化学方程式为____ 。
(6)往 溶液中加入过量
溶液中加入过量 溶液可以制得
溶液可以制得 ,该反应的离子方程式为
,该反应的离子方程式为__ 。
 ,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分
,水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的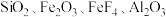 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
(1)滤渣1的主要成分是
 在周期表中的位置
在周期表中的位置(2)流程中共熔时发生的主要反应的化学方程式为
(3)写出
 转变为紫红色溶液的离子反应方程式
转变为紫红色溶液的离子反应方程式(4)整个流程中的
(5)
 还原软锰矿制备
还原软锰矿制备 的化学方程式为
的化学方程式为(6)往
 溶液中加入过量
溶液中加入过量 溶液可以制得
溶液可以制得 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】W、X、Y、Z、Q、R是核电荷数依次增大的六种短周期主族元素。W的一种核素可用于考古,X原子的最外层电子数是其内层电子数的3倍,Y在短周期元素中金属性最强,Z是地壳中含量最多的金属元素,Q与X同主族。
请回答下列问题:
(1)W的元素名称为___________ ,R的元素符号为___________ 。
(2)X、Y、Z、Q的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)W、X、Q的最简单氢化物中,沸点最高的是___________ (用化学式表示),原因是___________ 。
(4)将R的单质通入Y2Q溶液中能够证明R的非金属性强于Q的,请写出该反应的化学方程式:___________ 。
(5)向Y2WX3溶液中滴加少量稀H2SO4,发生反应的离子方程式为___________ 。
(6)Z的氧化物能与R的最高价氧化物对应的水化物反应,该反应的离子方程式为___________ 。
请回答下列问题:
(1)W的元素名称为
(2)X、Y、Z、Q的简单离子半径由大到小的顺序为
(3)W、X、Q的最简单氢化物中,沸点最高的是
(4)将R的单质通入Y2Q溶液中能够证明R的非金属性强于Q的,请写出该反应的化学方程式:
(5)向Y2WX3溶液中滴加少量稀H2SO4,发生反应的离子方程式为
(6)Z的氧化物能与R的最高价氧化物对应的水化物反应,该反应的离子方程式为
您最近一年使用:0次
【推荐3】高纯四氧化三锰是电子工业生产锰锌氧软磁材料的重要原料之一,一种以菱锰矿(主要成分是 ,含有少量Al、Fe、Mg、Ca、Cu、Si的氧化物)为原料制备
,含有少量Al、Fe、Mg、Ca、Cu、Si的氧化物)为原料制备 流程如下图所示。
流程如下图所示。
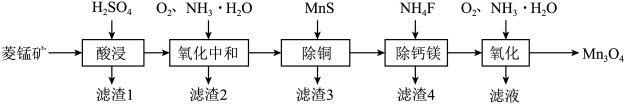
回答下列问题:
(1)“酸浸”过程中需要加热,其目的是___________ 。
(2)“酸浸”过程中发生的主要反应的离子方程式为___________ 。
(3)“滤渣1”的成分是___________ 。
(4)“氧化中和”可除去的主要金属阳离子是___________ 。
(5)已知 ,
,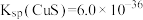 ,请利用计算说明选择MnS能除铜的原因
,请利用计算说明选择MnS能除铜的原因___________ 。
(6)“除钙镁”加入 的用量是理论用量的1.5倍,其目的是
的用量是理论用量的1.5倍,其目的是___________ 。
(7)“氧化”过程发生的总反应的化学方程式为___________ 。
 ,含有少量Al、Fe、Mg、Ca、Cu、Si的氧化物)为原料制备
,含有少量Al、Fe、Mg、Ca、Cu、Si的氧化物)为原料制备 流程如下图所示。
流程如下图所示。
回答下列问题:
(1)“酸浸”过程中需要加热,其目的是
(2)“酸浸”过程中发生的主要反应的离子方程式为
(3)“滤渣1”的成分是
(4)“氧化中和”可除去的主要金属阳离子是
(5)已知
 ,
,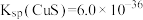 ,请利用计算说明选择MnS能除铜的原因
,请利用计算说明选择MnS能除铜的原因(6)“除钙镁”加入
 的用量是理论用量的1.5倍,其目的是
的用量是理论用量的1.5倍,其目的是(7)“氧化”过程发生的总反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知,A为一种常见的单质,B是一种淡黄色固体;B、C、D、E是含A元素且焰色均为黄色

(1)写出化学式:B___________ ,C___________ ,E___________
(2)写出化学方程式B→C:___________ ;E→D:___________
(3)向NaOH溶液中通入 气体,得到混合的溶液,向反应后溶液中滴入HCl溶液,关系如下图所示,溶液中溶质为
气体,得到混合的溶液,向反应后溶液中滴入HCl溶液,关系如下图所示,溶液中溶质为 和M,M为
和M,M为___________ ;混合溶液中物质的量之比为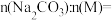
___________
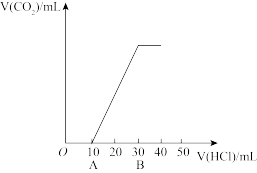
(4)Na、Al元素的单质共6.25g在250mL水中完全反应,生成的溶液中只含有一种溶质,所得溶液的物质的量浓度最大值为___________ mol/L(液体的体积变化忽略不计)

(1)写出化学式:B
(2)写出化学方程式B→C:
(3)向NaOH溶液中通入
 气体,得到混合的溶液,向反应后溶液中滴入HCl溶液,关系如下图所示,溶液中溶质为
气体,得到混合的溶液,向反应后溶液中滴入HCl溶液,关系如下图所示,溶液中溶质为 和M,M为
和M,M为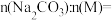

(4)Na、Al元素的单质共6.25g在250mL水中完全反应,生成的溶液中只含有一种溶质,所得溶液的物质的量浓度最大值为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示是某些无机物的转化关系(部分反应物和生成物未列出)。已知F是一种红褐色沉淀;M、K是常见的金属单质;B是一种有刺激性气味的气体;向C溶液中加入BaCl2溶液,生成不溶于稀盐酸的白色沉淀。
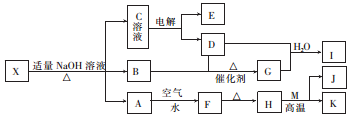
(1)已知盐X不带结晶水,则X的化学式为_________ 。
(2)若不考虑损失,G、D和H2O可恰好完全反应生成I,反应时G和D的物质的量之比为__________ 。
(3)足量K与I的稀溶液反应的离子方程式为____________________ 。
(4)J与NaOH溶液恰好完全反应可生成一种盐。将该盐的水溶液蒸干灼烧可得到_________ (填化学式)。
(5)在0.02 mol·L-1的X溶液中,各种离子的浓度由大到小的顺序为_______________ 。

(1)已知盐X不带结晶水,则X的化学式为
(2)若不考虑损失,G、D和H2O可恰好完全反应生成I,反应时G和D的物质的量之比为
(3)足量K与I的稀溶液反应的离子方程式为
(4)J与NaOH溶液恰好完全反应可生成一种盐。将该盐的水溶液蒸干灼烧可得到
(5)在0.02 mol·L-1的X溶液中,各种离子的浓度由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:

(1)若A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液,E溶于NaOH溶液的离子方程式是____ ;工业上冶炼A的化学反应方程式是____ 。
(2)若C是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式是____ ;1 mol C完全燃烧生成液态水时放热1300 kJ·mol-1,则C完全燃烧的热化学方程式是_____ 。A与B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是_________ 。

(1)若A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液,E溶于NaOH溶液的离子方程式是
(2)若C是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】铁元素是重要的金属元素,含有铁元素的物质在人类的生活中有着重要应用。
(1)小思设计了探究铁与水的反应的实验。虚线框处用来检验生成的气体。
①A装置的作用是_______ ,B中反应的化学方程式为_______ 。
②虚线框C处应该选择装置_______ (填甲或乙),实验现象是_______ 。
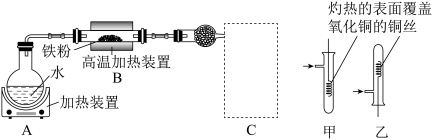
③反应一段时间后,冷却并取出B中固体,与过量的稀盐酸充分反应后_______ (填字母)
A.一定存在 B.一定存在
B.一定存在
C. 和
和 中只存在一种 D.一定存在
中只存在一种 D.一定存在 +和
+和
为了证明你的判断,应选用的检验试剂是_______ 。
(2)小海利用上述反应的产物制取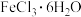 晶体。
晶体。
取③反应后的溶液过滤:
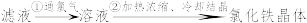 。
。
步骤①通氯气的离子方程式为_______ 。
(3)用氧化沉淀法生产 的工艺流程如图。
的工艺流程如图。

请写出②通一定量空气时发生反应的化学方程式_______ 。
(1)小思设计了探究铁与水的反应的实验。虚线框处用来检验生成的气体。
①A装置的作用是
②虚线框C处应该选择装置

③反应一段时间后,冷却并取出B中固体,与过量的稀盐酸充分反应后
A.一定存在
 B.一定存在
B.一定存在
C.
 和
和 中只存在一种 D.一定存在
中只存在一种 D.一定存在 +和
+和
为了证明你的判断,应选用的检验试剂是
(2)小海利用上述反应的产物制取
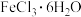 晶体。
晶体。取③反应后的溶液过滤:
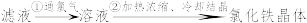 。
。步骤①通氯气的离子方程式为
(3)用氧化沉淀法生产
 的工艺流程如图。
的工艺流程如图。
请写出②通一定量空气时发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:____ 。
Ⅰ.某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
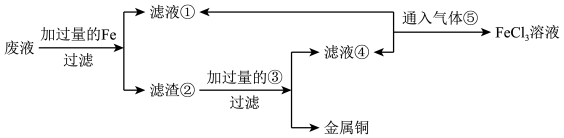
(2)请写出上述实验中有关物质的化学式:③_____ 。
(3)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为_____ 。
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
(4)写出向①④的混合液中通入⑤的离子方程式:_____ 。
Ⅱ.用如图所示装置制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及6mol•L-1的硫酸,其他试剂任选。填写下列空白:
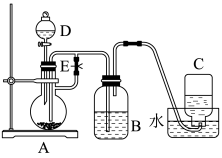
(5)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是____ ,实验开始时先将活塞E打开,再打开分液漏斗D活塞让酸液流下,在C中收集到气体。
(6)简述生成Fe(OH)2的操作过程:____ 。
(7)拔去装置B中的橡皮塞,让空气进入,写出有关反应的化学方程式:____ 。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:
Ⅰ.某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

(2)请写出上述实验中有关物质的化学式:③
(3)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为
①加入足量氯水②加入足量KMnO4溶液③加入少量KSCN溶液
| A.①③ | B.③② | C.③① | D.①②③ |
Ⅱ.用如图所示装置制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及6mol•L-1的硫酸,其他试剂任选。填写下列空白:

(5)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是
(6)简述生成Fe(OH)2的操作过程:
(7)拔去装置B中的橡皮塞,让空气进入,写出有关反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某铁矿石烧渣含 、
、 和
和 ,以该烧渣为原料制取
,以该烧渣为原料制取 的流程如下:
的流程如下:
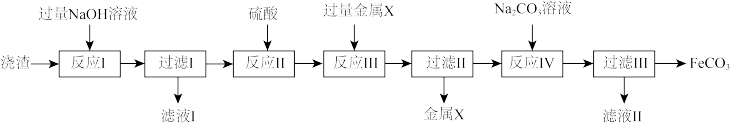
已知 是难溶于水的酸性氧化物,
是难溶于水的酸性氧化物, 是难溶于水的白色固体。
是难溶于水的白色固体。
(1)反应Ⅰ中 所发生反应的离子方程式为
所发生反应的离子方程式为____________ 。
(2)选择最适合的金属 ,写出反应Ⅲ的离子方程式:
,写出反应Ⅲ的离子方程式:____________ 。
(3)检验反应Ⅲ已经完全的方法是____________ 。
(4)反应Ⅳ中当将过滤Ⅱ的滤液缓慢滴加到 溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。
溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。
①白色沉淀中除 外,还含有
外,还含有____________ (填化学式),生成该沉淀是因为 溶液中含有
溶液中含有____________ (填离子符号)。
②写出沉淀变色时所发生反应的化学方程式:____________ 。
 、
、 和
和 ,以该烧渣为原料制取
,以该烧渣为原料制取 的流程如下:
的流程如下:
已知
 是难溶于水的酸性氧化物,
是难溶于水的酸性氧化物, 是难溶于水的白色固体。
是难溶于水的白色固体。(1)反应Ⅰ中
 所发生反应的离子方程式为
所发生反应的离子方程式为(2)选择最适合的金属
 ,写出反应Ⅲ的离子方程式:
,写出反应Ⅲ的离子方程式:(3)检验反应Ⅲ已经完全的方法是
(4)反应Ⅳ中当将过滤Ⅱ的滤液缓慢滴加到
 溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。
溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。①白色沉淀中除
 外,还含有
外,还含有 溶液中含有
溶液中含有②写出沉淀变色时所发生反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】根据下图的化学反应框图回答下列问题。已知:粉状化合物A是红棕色,粉状单质B是金属单质。
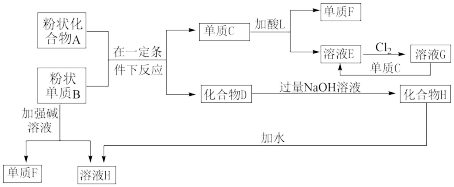
(1)溶液E加入氢氧化钠溶液的现象是_______ 。
(2)写出下列反应的化学方程式:
 →
→ :
:_______ ;
D→H:_______ 。
(3)写出下列反应的离子方程式:
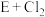 →G:
→G:_______ ;
 →E:
→E:_______ ;
B→ :
:_______ 。

(1)溶液E加入氢氧化钠溶液的现象是
(2)写出下列反应的化学方程式:
 →
→ :
:D→H:
(3)写出下列反应的离子方程式:
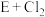 →G:
→G: →E:
→E:B→
 :
:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某化学实验室产生的酸性废液中含有Fe3+、Cu2+、Ag+三种金属离子,甲同学设计了如图所示的方案对废液进行处理,以回收金属,保护环境。请回答:
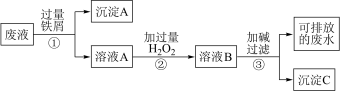
(1)沉淀A中含有的金属单质有Fe、__ 。
(2)写出反应②的离子方程式__ 。
(3)用KSCN来检验溶液B中所含的金属离子,其离子方程式为__ 。
(4)操作①的名称是__ ,操作过程中使用到的玻璃仪器有烧杯、玻璃棒、__ 。

(1)沉淀A中含有的金属单质有Fe、
(2)写出反应②的离子方程式
(3)用KSCN来检验溶液B中所含的金属离子,其离子方程式为
(4)操作①的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
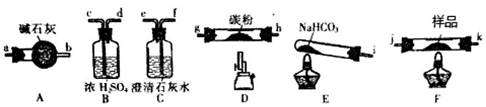
【推荐3】某研究小组利用下图装置探究CO还原Fe2O3所得到的一种黑色粉末的成分(固定装置略去)。(已知:Fe2+遇到K3[Fe(CN)6]溶液生成蓝色沉淀)
请回答问题:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→____________ →____________ →g→h→__________ →__________ →j → k→____________ →___________ 。(填字母编号)
(2)证明Fe2O3已被还原的现象是___________________ 。
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe。
【猜想二】黑色粉末的成分可能是FeO。
【猜想三】黑色粉末的成分可能是__________________ 。
设计并完成实验如下:
①根据实验现象,则猜想_________ 成立。
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去。可能的原因及验证方法为__________________ 。
(4)上述装置还有不妥之处,改进措施为____________________ 。
请回答问题:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→
(2)证明Fe2O3已被还原的现象是
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe。
【猜想二】黑色粉末的成分可能是FeO。
【猜想三】黑色粉末的成分可能是
设计并完成实验如下:
步骤 | 操作 | 现象 |
1 | 加入稀盐酸 | 溶解,无气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 |
3 | 变红 |
①根据实验现象,则猜想
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去。可能的原因及验证方法为
(4)上述装置还有不妥之处,改进措施为
您最近一年使用:0次



