卤族元素包含F(氟)、Cl(氯)、Br(溴)和I(碘)等元素,卤族元素的单质及其化合物在生产生活中有着重要的应用,人们从自然界中获得卤族单质及基化合物的过程,体现了化学科学在利用自然资源创造新物质中的独特作用,根据所学知识及所给信息,回答下列问题:
(1)写出 的离子结构示意图
的离子结构示意图_______ 。
(2)氯元素存在 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有_______ 种。
(3)将氯气通入紫色石蕊溶液中,实验的现象是_______ ,结合离子方程式加上必要的文字解释原因_______ 。
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液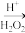 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有_______ 。
①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入 和
和 发生的离子方程式为
发生的离子方程式为_______ ;检验提取的碘水中含有 的试剂是
的试剂是_______ 。
(5)从海水晒盐后的盐卤(主要含 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:

从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是_______ 反应。工业上从盐卤中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是_______ 。写出 与盐酸反应的离子方程式
与盐酸反应的离子方程式_______ 。
(1)写出
 的离子结构示意图
的离子结构示意图(2)氯元素存在
 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有(3)将氯气通入紫色石蕊溶液中,实验的现象是
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是
 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液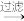 滤液
滤液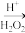 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入
 和
和 发生的离子方程式为
发生的离子方程式为 的试剂是
的试剂是(5)从海水晒盐后的盐卤(主要含
 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:
从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是 与盐酸反应的离子方程式
与盐酸反应的离子方程式
更新时间:2024-03-03 07:32:07
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题:
(1)氯原子的最外层电子数为___________ ;其最高价氧化物的化学式是___________ 。
(2)维生素 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有___________ 性(填“还原”或“氧化”)。
(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式___________ 。
(1)氯原子的最外层电子数为
(2)维生素
 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯化钠是一种重要的化工原料,可用于制备如下图所示的一系列物质。
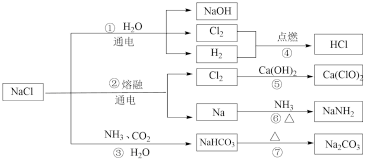
(1)反应①的离子方程式为___________ ,反应中氧化剂为___________ 。
(2)Na+的离子结构示意图为___________ ,NH3的电子式为___________ 。
(3)漂白粉在空气中久置易变质的原因是___________ (用文字表述)。
(4)氨基钠(NaNH2)是生产维生素A的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨,再加热至一定温度生成氨基钠和氢气。NaNH2中氮元素的化合价为___________ ,该反应属于四大基本反应类型中的___________ 。

(1)反应①的离子方程式为
(2)Na+的离子结构示意图为
(3)漂白粉在空气中久置易变质的原因是
(4)氨基钠(NaNH2)是生产维生素A的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨,再加热至一定温度生成氨基钠和氢气。NaNH2中氮元素的化合价为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】结合如图六种微粒的结构示意图,回答下列问题:

(1)粒子④在化学反应中易___ (填“失”或“得”)电子,形成___ (填符号)。
(2)①—⑤五种粒子中化学性质相似的是___ (填序号)。
(3)①—⑥六种粒子中具有相对稳定结构的是___ (填序号)。
(4)若⑥表示某阴离子的结构示意图,则X可能是下列中的___ (填字母序号)。
a.16 b.17 c.18 d.19
(5)若某元素的阳离子X2+核外有28个电子,相对原子质量为65,则X原子核内中子数与质子数之差为___ 。

(1)粒子④在化学反应中易
(2)①—⑤五种粒子中化学性质相似的是
(3)①—⑥六种粒子中具有相对稳定结构的是
(4)若⑥表示某阴离子的结构示意图,则X可能是下列中的
a.16 b.17 c.18 d.19
(5)若某元素的阳离子X2+核外有28个电子,相对原子质量为65,则X原子核内中子数与质子数之差为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(CN)2、(OCN)2、(SCN)2等与X2(X=F、Cl、Br、I)的性质相似,CN—、OCN—、SCN—与X—的性质相似,被称为拟卤素。完成下列反应方程式(一律要配平):
(CN)2+H2O=_____________________ ;
AgSCN+Br2=________________ ;
AgCN=_____________________ ;
BrCl+ H2O=___________________ 。
(CN)2+H2O=
AgSCN+Br2=
AgCN=
BrCl+ H2O=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.已知KMnO4在常温下与浓盐酸反应生成Cl2
2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O
(1)被氧化的HCl的物质的量与实际被消耗的KMnO4的物质的量之比是___________ 。
(2)生成标准状况下3.36 L氯气,转移的电子的物质的量是___________ 。
(3)检验氯气存在可以用湿润的淀粉-KI试纸;若氯气存在,则试纸呈现___________ 色;该过程的离子方程式是___________ 。
Ⅱ.氯水是实验室中常用的液体试剂。
(4)氯气和水反应的化学方程式是___________ 。
(5)氯水中含有一种弱酸,该酸见光分解的化学方程式是___________ 。
2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O
(1)被氧化的HCl的物质的量与实际被消耗的KMnO4的物质的量之比是
(2)生成标准状况下3.36 L氯气,转移的电子的物质的量是
(3)检验氯气存在可以用湿润的淀粉-KI试纸;若氯气存在,则试纸呈现
Ⅱ.氯水是实验室中常用的液体试剂。
(4)氯气和水反应的化学方程式是
(5)氯水中含有一种弱酸,该酸见光分解的化学方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 与
与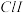 性质相似,
性质相似,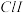 与水反应可能有两种,写出可能的方程式:
与水反应可能有两种,写出可能的方程式:
①___________________________
②___________________________
(要求方程式的物质必须用结构式表示,例:H2+Cl2==2HCl可表示为H—H+Cl—Cl ==2H—Cl)试用实验事实判断是哪一种可能?
___________________ (提示:AgI是黄色沉淀);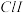 中Cl 显
中Cl 显________ 价,你的依据是______________ ;HIO的电子式________________ 。
 与
与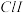 性质相似,
性质相似,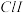 与水反应可能有两种,写出可能的方程式:
与水反应可能有两种,写出可能的方程式:①
②
(要求方程式的物质必须用结构式表示,例:H2+Cl2==2HCl可表示为H—H+Cl—Cl ==2H—Cl)试用实验事实判断是哪一种可能?
 中Cl 显
中Cl 显
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
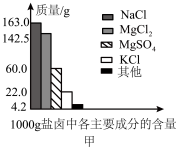
(1)根据图甲所示,写出盐卤中含量最多的盐为___________ (填化学式)其电子式为___________
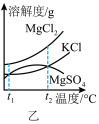
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是___________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
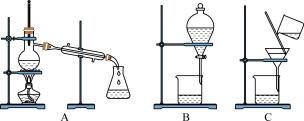
粗盐的提纯应选择图___________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是___________ 。
A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。
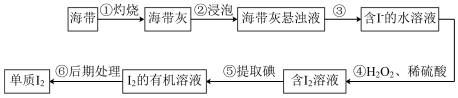
(4)实验步骤①会用到下列仪器中的___________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,___________ 。
(6)“提取碘”存在以下两种方案。
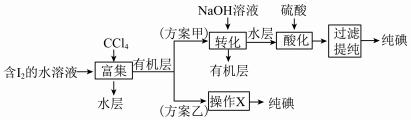
①方案乙中“操作X”的名称是___________ 。
②该流程可循环利用的物质是___________ 。
③采用方案乙得到纯碘的产率较低,原因是___________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是
(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,
(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是___________(填序号)。
(2)海带中含有碘元素。实验室提取碘的步骤如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是___________ 。海带灰中含有硫酸镁、碳酸钠等,在实验步骤___________ (填序号)中实现与碘分离。
②写出步骤④反应的离子方程式___________ 。提取碘的过程中,不能选择乙醇代替 提取碘单质的原因
提取碘单质的原因___________ 。
(3)已知: ,氯气既可以氧化
,氯气既可以氧化 ,也可以氧化
,也可以氧化 。往200mL
。往200mL  溶液中通入8.96L(标准状况)
溶液中通入8.96L(标准状况) ,反应完成后,溶液中有
,反应完成后,溶液中有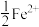 被氧化,则原
被氧化,则原 溶液的物质的量浓度为
溶液的物质的量浓度为___________ 。
(1)无需经过化学变化就能从海水中获得的物质是___________(填序号)。
| A.食盐 | B.溴 | C.烧碱 | D.纯碱 |

①灼烧海带至灰烬时所用的主要仪器名称是
②写出步骤④反应的离子方程式
 提取碘单质的原因
提取碘单质的原因(3)已知:
 ,氯气既可以氧化
,氯气既可以氧化 ,也可以氧化
,也可以氧化 。往200mL
。往200mL  溶液中通入8.96L(标准状况)
溶液中通入8.96L(标准状况) ,反应完成后,溶液中有
,反应完成后,溶液中有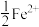 被氧化,则原
被氧化,则原 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】海洋资源的利用具有非常广阔的前景。
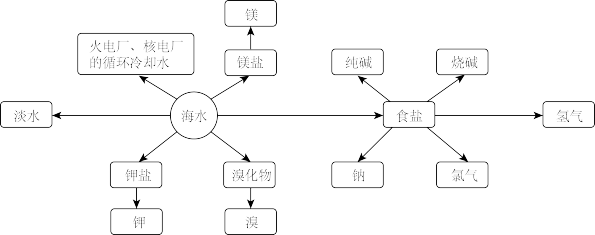
回答下列问题:
Ⅰ.海水制盐
(1)粗盐中可溶性杂质离子包含 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为___________ (填字母)。
a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
(2)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式___________ 。
Ⅱ.海水提溴
(3)工业上常用“吹出法”提溴,请写出用SO2吸收Br2的化学反应方程式___________ 。
(4)含Br2的海水经“空气吹出、SO2吸收、通入氯气”后再蒸馏的目的是___________ 。
Ⅲ.从海带中提取碘的实验过程如下图所示:
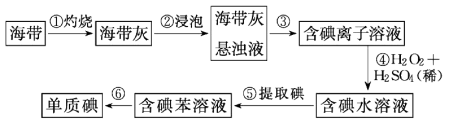
(5)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(6)请写出步骤④反应的离子方程式___________ 。
Ⅳ.海水淡化
(7)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是___________ 。

回答下列问题:
Ⅰ.海水制盐
(1)粗盐中可溶性杂质离子包含
 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
(2)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式
Ⅱ.海水提溴
(3)工业上常用“吹出法”提溴,请写出用SO2吸收Br2的化学反应方程式
(4)含Br2的海水经“空气吹出、SO2吸收、通入氯气”后再蒸馏的目的是
Ⅲ.从海带中提取碘的实验过程如下图所示:

(5)步骤①中灼烧海带时,应将海带放入
(6)请写出步骤④反应的离子方程式
Ⅳ.海水淡化
(7)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】目前世界上60%的镁是从海水中提取的。已知海水提取镁的主要步骤如下:
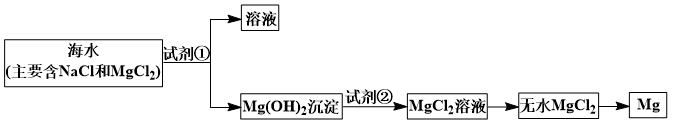
(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
(一)__________________________________________________ ;
(二)__________________________________________________ ;
(三)__________________________________________________ ;
(四)__________________________________________________ 。
(2)框图中加入的试剂①应该是________ (填化学式);加入的试剂②是________ (填化学式);工业上由无水MgCl2制取镁的化学方程式为___________ 。

(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
| 方法 | 是否正确 | 简述理由 |
| 方法1:直接往海水中加入沉淀剂 | 不正确 | (一) |
| 方法2:高温加热蒸发海水后,再加入沉淀剂 | (二) | (三) |
| 你认为最合理的其他方法是: (四) | ||
(一)
(二)
(三)
(四)
(2)框图中加入的试剂①应该是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】海洋是一个巨大的物质资源和能量宝库,世界各国都在研究如何充分利用海洋资源。
Ⅰ. 从海水中可以提取食盐。
Ⅱ.从海水中提取镁。已知MgO、MgCl2的熔点分别为2800℃、604℃,从海水中提
取镁,最合理的方法是_____ 。
Ⅲ.从海水中提溴。其工业方法有:空气吹出纯碱吸收法、空气吹出SO2吸收法、溶
剂萃取法等。
(1)空气吹出纯碱吸收法。将氯气通入富含溴离子的海水中,再用空气将溴吹出,
用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及的反应有:
①______________________________ (写出离子方程式);
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3CO2↑;
③BrO3﹣+5Br﹣+6H+═3Br2+3H2O
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,
然后再用氯气氧化即得单质溴。
写出溴与二氧化硫反应的化学方程式:_____________________________ 。
Ⅰ. 从海水中可以提取食盐。
Ⅱ.从海水中提取镁。已知MgO、MgCl2的熔点分别为2800℃、604℃,从海水中提
取镁,最合理的方法是
A.海水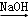 Mg(OH)2 Mg(OH)2 Mg Mg |
B.海水 MgCl2溶液→MgCl2熔融 MgCl2溶液→MgCl2熔融 Mg Mg |
C.海水 Mg(OH)2 Mg(OH)2 MgO MgO Mg Mg |
D.海水 Mg(OH)2 Mg(OH)2 MgCl2溶液→MgCl2熔融 MgCl2溶液→MgCl2熔融 Mg Mg |
Ⅲ.从海水中提溴。其工业方法有:空气吹出纯碱吸收法、空气吹出SO2吸收法、溶
剂萃取法等。
(1)空气吹出纯碱吸收法。将氯气通入富含溴离子的海水中,再用空气将溴吹出,
用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及的反应有:
①
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3CO2↑;
③BrO3﹣+5Br﹣+6H+═3Br2+3H2O
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,
然后再用氯气氧化即得单质溴。
写出溴与二氧化硫反应的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】海水资源的利用具有非常广阔的前景,从海水中可提取多种化工原料。
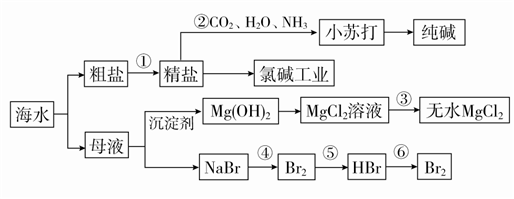
(1)海水淡化处理的方法有__________________________ (写出两种即可)。
(2)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制时所用试剂为:
等杂质,精制时所用试剂为:
A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Na2CO3溶液
加入试剂的顺序是__________________ 。
(3)步骤②中,向精盐溶液中应先通入________ ,再通入________ 。
(4)氯碱工业中,与电源负极相连的电极附近溶液pH值________ (填“变大”“变小”或“不变”)。用玻璃棒蘸浓氨水检验阳极产生的气体,发现产生大量白烟,白烟的主要成分是________________________ 。
(5)实际生产中,常选用________ 作为沉淀剂,从氯化镁溶液中得到无水晶体的操作为_____________________________________ 。
(6)步骤⑤用SO2水溶液吸收溴单质,吸收率可达93%,反应的离子方程式为______________________________________ 。

(1)海水淡化处理的方法有
(2)粗盐中含有Ca2+、Mg2+、SO
 等杂质,精制时所用试剂为:
等杂质,精制时所用试剂为:A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Na2CO3溶液
加入试剂的顺序是
(3)步骤②中,向精盐溶液中应先通入
(4)氯碱工业中,与电源负极相连的电极附近溶液pH值
(5)实际生产中,常选用
(6)步骤⑤用SO2水溶液吸收溴单质,吸收率可达93%,反应的离子方程式为
您最近半年使用:0次



