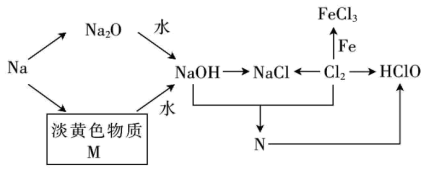
氯化钠是一种重要的化工原料,可用于制备如下图所示的一系列物质。
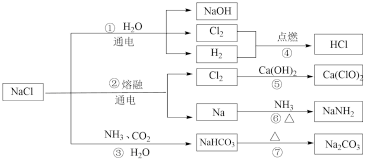
(1)反应①的离子方程式为___________ ,反应中氧化剂为___________ 。
(2)Na+的离子结构示意图为___________ ,NH3的电子式为___________ 。
(3)漂白粉在空气中久置易变质的原因是___________ (用文字表述)。
(4)氨基钠(NaNH2)是生产维生素A的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨,再加热至一定温度生成氨基钠和氢气。NaNH2中氮元素的化合价为___________ ,该反应属于四大基本反应类型中的___________ 。

(1)反应①的离子方程式为
(2)Na+的离子结构示意图为
(3)漂白粉在空气中久置易变质的原因是
(4)氨基钠(NaNH2)是生产维生素A的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨,再加热至一定温度生成氨基钠和氢气。NaNH2中氮元素的化合价为
更新时间:2022-01-23 17:11:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】M元素的单质可用于原子反应堆的到导热剂,其原子结构示意图,则:

(1)该原子有___________ 个电子层,X的值是:___________ ,M元素属于___________ (填“金属”或“非金属”)元素;
(2)M元素的化学性质与下列___________(填序号)元素的化学性质相似。
(3)M元素的与第八号元素组成的化学式是___________ 。
(4)第(2)小题的D元素与氢元素形成化合物的化学式是___________ 。

(1)该原子有
(2)M元素的化学性质与下列___________(填序号)元素的化学性质相似。
A. | B. | C. | D. |
(4)第(2)小题的D元素与氢元素形成化合物的化学式是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,进行作答
(1)2023年第19届杭州亚运会场馆实现 覆盖,制作
覆盖,制作 芯片的材料为
芯片的材料为 (氮化镓),镓原子结构示意图为
(氮化镓),镓原子结构示意图为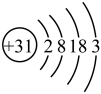 ,镓元素在元素周期表中的位置
,镓元素在元素周期表中的位置___________ 。
(2)2023年10月26日神舟十七号飞船成功对接太空站,为使宇航员有良好的生存环境,飞船中装有盛 颗粒的供氧装置。
颗粒的供氧装置。
① 中的氧元素的化合价为
中的氧元素的化合价为___________ 价。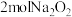 与水完全反应时,生成的氧气在标准状况下体积为
与水完全反应时,生成的氧气在标准状况下体积为___________ L。
②如用 (超氧化钾)代替
(超氧化钾)代替 ,也能达到同样的目的。写出
,也能达到同样的目的。写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
(3)2023年12月18日甘肃省发生地震灾害,受灾废墟需喷洒大量84消毒液的稀溶液进行消毒。84消毒液可由 与
与 溶液反应制得,其主要成分为
溶液反应制得,其主要成分为 。
。
①资料(3)涉及的物质中,属于碱的是___________ (填化学式,下同);属于盐的是___________ 。
②“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是___________ (用离子方程式表示),但“84消毒液”却不能与“洁厕灵”(浓盐酸)混合使用,原因是___________ (用离子方程式表示)。
(1)2023年第19届杭州亚运会场馆实现
 覆盖,制作
覆盖,制作 芯片的材料为
芯片的材料为 (氮化镓),镓原子结构示意图为
(氮化镓),镓原子结构示意图为 ,镓元素在元素周期表中的位置
,镓元素在元素周期表中的位置(2)2023年10月26日神舟十七号飞船成功对接太空站,为使宇航员有良好的生存环境,飞船中装有盛
 颗粒的供氧装置。
颗粒的供氧装置。①
 中的氧元素的化合价为
中的氧元素的化合价为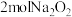 与水完全反应时,生成的氧气在标准状况下体积为
与水完全反应时,生成的氧气在标准状况下体积为②如用
 (超氧化钾)代替
(超氧化钾)代替 ,也能达到同样的目的。写出
,也能达到同样的目的。写出 与
与 反应的化学方程式
反应的化学方程式(3)2023年12月18日甘肃省发生地震灾害,受灾废墟需喷洒大量84消毒液的稀溶液进行消毒。84消毒液可由
 与
与 溶液反应制得,其主要成分为
溶液反应制得,其主要成分为 。
。①资料(3)涉及的物质中,属于碱的是
②“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是
您最近半年使用:0次
【推荐1】回答下列问题:
(1)下列微粒:①S②SO ③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是
③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是___ (填序号),只能表现出氧化性的是___ (填序号)。
(2)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为___ 。
(3)自来水中的NO 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平
,产物是N2。发生的反应可表示如下,请完成方程式的配平___ 。
Al+ NO + OH-→ AlO
+ OH-→ AlO + N2↑+ H2O
+ N2↑+ H2O
(4)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:___ 。
②反应中发生电子转移的Cl2与NH3的分子数之比为:___ 。
(1)下列微粒:①S②SO
 ③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是
③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是(2)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为
(3)自来水中的NO
 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平
,产物是N2。发生的反应可表示如下,请完成方程式的配平Al+ NO
 + OH-→ AlO
+ OH-→ AlO + N2↑+ H2O
+ N2↑+ H2O(4)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:
②反应中发生电子转移的Cl2与NH3的分子数之比为:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】水体中的含氮化合物(以 、
、 、
、 等形式存在)是主要的污染物之一,需对其进行无害化处理。
等形式存在)是主要的污染物之一,需对其进行无害化处理。
(1)酸性废水中的氨氮(主要是以 形式存在)可以通过沉淀法或是氧化还原法除去。
形式存在)可以通过沉淀法或是氧化还原法除去。
①向该酸性废水中加入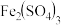 溶液,反应后生成
溶液,反应后生成 沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为
沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为___________ 价,除去氨氮的过程中生成 沉淀的反应的离子方程式为
沉淀的反应的离子方程式为___________ 。
②向该酸性废水中加入NaClO溶液可将 转化成无害气体放出,发生反应的离子方程式为
转化成无害气体放出,发生反应的离子方程式为___________ ;NaCl可以通过 与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为
与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)利用厌氧氨氧化菌细胞中的三种酶处理废水中含氮粒子的反应机理如图所示。

①从图中可以看出该废水中含氮粒子主要以___________ 形式存在,图中1mol  中存在的共价键数目为
中存在的共价键数目为___________  。
。
②在NR酶的作用下, 发生了
发生了___________ (填“氧化反应”或“还原反应”), 在HH酶的催化下与
在HH酶的催化下与 发生反应,生成两种产物的化学方程式为
发生反应,生成两种产物的化学方程式为___________ 。
 、
、 、
、 等形式存在)是主要的污染物之一,需对其进行无害化处理。
等形式存在)是主要的污染物之一,需对其进行无害化处理。(1)酸性废水中的氨氮(主要是以
 形式存在)可以通过沉淀法或是氧化还原法除去。
形式存在)可以通过沉淀法或是氧化还原法除去。①向该酸性废水中加入
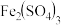 溶液,反应后生成
溶液,反应后生成 沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为
沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为 沉淀的反应的离子方程式为
沉淀的反应的离子方程式为②向该酸性废水中加入NaClO溶液可将
 转化成无害气体放出,发生反应的离子方程式为
转化成无害气体放出,发生反应的离子方程式为 与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为
与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为(2)利用厌氧氨氧化菌细胞中的三种酶处理废水中含氮粒子的反应机理如图所示。

①从图中可以看出该废水中含氮粒子主要以
 中存在的共价键数目为
中存在的共价键数目为 。
。②在NR酶的作用下,
 发生了
发生了 在HH酶的催化下与
在HH酶的催化下与 发生反应,生成两种产物的化学方程式为
发生反应,生成两种产物的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】阅读下列材料后,回答相应问题。
铁在人体中以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(FeSO4)。
(1)人体中经常进行转化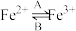 ,A反应中Fe2+作
,A反应中Fe2+作________ 剂,B反应中Fe3+作________ 剂,服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。这说明维生素C具有________ 性。
(2)新配制的FeCl2溶液应加入________ 以防止FeCl2转化为FeCl3,要除去FeCl3溶液中少量的FeCl2杂质,可向其中通入适量的_____ 。
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为______ 。
(4)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为_______ , ________ ;处理过程中需定期添加的原料是______ 。
(5)某同学为检验某未知溶液中是否为FeCl2溶液,采取如下实验方案加以验证:
取少许未知试液于试管中 溶液呈红色(证明含有FeCl2),你认为此方案
溶液呈红色(证明含有FeCl2),你认为此方案______ (填“合理”或“不合理”),若不合理,如何改进:______ 。
铁在人体中以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(FeSO4)。
(1)人体中经常进行转化
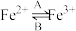 ,A反应中Fe2+作
,A反应中Fe2+作(2)新配制的FeCl2溶液应加入
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为
(4)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为
(5)某同学为检验某未知溶液中是否为FeCl2溶液,采取如下实验方案加以验证:
取少许未知试液于试管中
 溶液呈红色(证明含有FeCl2),你认为此方案
溶液呈红色(证明含有FeCl2),你认为此方案
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是__________ (填“CaCl2”或“Ca(ClO)2”)。
(2)漂白粉露置在空气中容易失效,请用化学方程式表示其失效原理______________________________________________ 、_____________________________ 。
(3)氯水具有漂白作用,是由于其中含有___________ (填“HCl”或“HClO”)。
(2)漂白粉露置在空气中容易失效,请用化学方程式表示其失效原理
(3)氯水具有漂白作用,是由于其中含有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯及其化合物在生产、生活中有着广泛的用途
(1)次氯酸钠是最普通的家庭洗涤中的“氯”漂白剂和消毒剂。已知“84消毒液”的主要成分是次氯酸钠,在清洗卫生间时,若将“洁厕灵”与“84消毒液”混合使用会发生氯气中毒事件。请从氧化还原反应的角度分析原因:_______________________ 。
(2)漂白粉的有效成分是:______________ (填化学式),老师新买的漂白粉没有保存说明书,请你为漂白粉设计一份保存注意事项(不超过20个字):_____________ ,漂白粉久置后其成分除CaCl2外还含有______________ (填化学式),请你设计实验方案证明该固体粉末含Cl-离子:____________________________ 。
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下述离子方程式Fe(OH)3+ClO-+OH-→ +□:
+□:_____________________________ 。
(4)ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O
①请用双线桥表示反应中电子转移的方向和数目: 2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O:______________________ 。
②上述反应中,当生成1 mol ClO2分子时,转移电子的物质的量为:___________ mol。
③Cl2和ClO2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-,则ClO2和Cl2相同质量时,ClO2的消毒能力是Cl2的___________ 倍。
(5)ClO2在工业上的一种生产工艺如图所示:
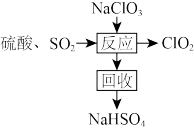
请写出“反应”步骤中生成CO2的化学方程式:________________ 。
(1)次氯酸钠是最普通的家庭洗涤中的“氯”漂白剂和消毒剂。已知“84消毒液”的主要成分是次氯酸钠,在清洗卫生间时,若将“洁厕灵”与“84消毒液”混合使用会发生氯气中毒事件。请从氧化还原反应的角度分析原因:
(2)漂白粉的有效成分是:
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下述离子方程式Fe(OH)3+ClO-+OH-→
 +□:
+□:(4)ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O
①请用双线桥表示反应中电子转移的方向和数目: 2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O:
②上述反应中,当生成1 mol ClO2分子时,转移电子的物质的量为:
③Cl2和ClO2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-,则ClO2和Cl2相同质量时,ClO2的消毒能力是Cl2的
(5)ClO2在工业上的一种生产工艺如图所示:

请写出“反应”步骤中生成CO2的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】“化学一我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是____ ,胶体和溶液的本质区别是____ 。
(2)钠的焰色试验的焰色为____ 色,该色的光射程远,透雾力强,据此原理制作的高压钠灯广泛应用于道路和广场的照明。焰色试验属于____ (填“物理”或“化学”)变化。
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是____ ,原因是____ 。
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有____ (填化学式)。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)钠的焰色试验的焰色为
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)等物质的量的钠、镁、铝分别与足量盐酸反应,产生的氢气在相同条件下的体积比为______________ 。
(2)等质量的钠、镁、铝分别与足量盐酸反应,产生的氢气在相同条件下的体积比为________________ 。
(3)分别将0.2mol的钠、镁、铝分别投入100ml 1mol·L-1的盐酸溶液中,三者产生的氢气在相同条件下的体积比为____________________ 。
(2)等质量的钠、镁、铝分别与足量盐酸反应,产生的氢气在相同条件下的体积比为
(3)分别将0.2mol的钠、镁、铝分别投入100ml 1mol·L-1的盐酸溶液中,三者产生的氢气在相同条件下的体积比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
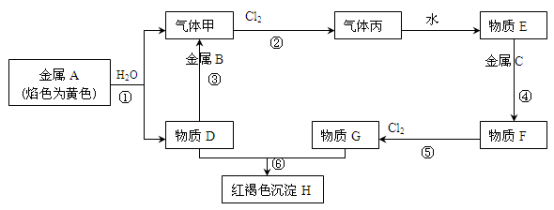
请回答下列问题:
(1)写出下列物质的化学式:B________ 、丙________
(2)写出下列反应的化学方程式:
反应①________________________________________________________________ ;
反应③________________________________________________________________ ;
反应⑥_______________________________________________________________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑥
您最近半年使用:0次

 Cl-微粒,回答下列问题:
Cl-微粒,回答下列问题: Cl、
Cl、