阅读下列材料后,回答相应问题。
铁在人体中以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(FeSO4)。
(1)人体中经常进行转化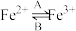 ,A反应中Fe2+作
,A反应中Fe2+作________ 剂,B反应中Fe3+作________ 剂,服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。这说明维生素C具有________ 性。
(2)新配制的FeCl2溶液应加入________ 以防止FeCl2转化为FeCl3,要除去FeCl3溶液中少量的FeCl2杂质,可向其中通入适量的_____ 。
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为______ 。
(4)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为_______ , ________ ;处理过程中需定期添加的原料是______ 。
(5)某同学为检验某未知溶液中是否为FeCl2溶液,采取如下实验方案加以验证:
取少许未知试液于试管中 溶液呈红色(证明含有FeCl2),你认为此方案
溶液呈红色(证明含有FeCl2),你认为此方案______ (填“合理”或“不合理”),若不合理,如何改进:______ 。
铁在人体中以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(FeSO4)。
(1)人体中经常进行转化
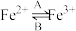 ,A反应中Fe2+作
,A反应中Fe2+作(2)新配制的FeCl2溶液应加入
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为
(4)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为
(5)某同学为检验某未知溶液中是否为FeCl2溶液,采取如下实验方案加以验证:
取少许未知试液于试管中
 溶液呈红色(证明含有FeCl2),你认为此方案
溶液呈红色(证明含有FeCl2),你认为此方案
21-22高一·全国·课前预习 查看更多[2]
更新时间:2022-08-15 21:48:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】写出下列反应的离子方程式:
(1)铜与硝酸银溶液反应_______________ 。
(2)醋酸与氢氧化钾溶液反应_________________ 。
(3)铁锈(主要成分氧化铁)与稀盐酸反应___________________ 。
(4)足量二氧化碳通入氢氧化钠溶液反应__________________ 。
(5)少量的NaHCO3溶液与Ba(OH) 2溶液反应______________ 。
(6)向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至溶液呈中性______________ 。
(1)铜与硝酸银溶液反应
(2)醋酸与氢氧化钾溶液反应
(3)铁锈(主要成分氧化铁)与稀盐酸反应
(4)足量二氧化碳通入氢氧化钠溶液反应
(5)少量的NaHCO3溶液与Ba(OH) 2溶液反应
(6)向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至溶液呈中性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O),其实验方案如下:
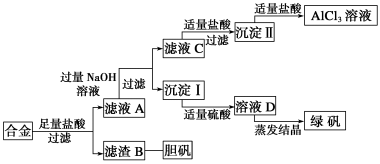
(1)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:___________ 。写出由沉淀Ⅱ转化为AlCl3溶液的离子方程式:___________ 。
(2)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为___________ 。

(1)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:
(2)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)下列物质 ①烧碱、②Fe(OH)3 胶体、③NaCl、④CO2、⑤铁片、⑥石墨、⑦甲烷、⑧HNO3、⑨CaCO3,其中属于混合物的是(填序号) ___________ ;属于酸的是 ___________ ;属于盐的是 ___________ ;属于非电解质的是 ___________ 。
(2)写出下列反应的离子方程式:
①AgNO3 溶液与 KCl 溶液混合:___________
②硫酸和氢氧化钡溶液混合:___________
③氢氧化钠溶液与盐酸溶液混合:___________
④锌投入硫酸铜溶液中:___________ 。
(2)写出下列反应的离子方程式:
①AgNO3 溶液与 KCl 溶液混合:
②硫酸和氢氧化钡溶液混合:
③氢氧化钠溶液与盐酸溶液混合:
④锌投入硫酸铜溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1).2Na+2H2O=2NaOH+H2↑为氧化还原反应
氧化剂是_________ 还原剂是________
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮直至溶液呈____________ 色,即可制得Fe(OH)3胶体。
(3)Fe(OH)3胶体,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫________ ;胶体中加入电解质,胶体变得浑浊,这是发生了__________ 。
氧化剂是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮直至溶液呈
(3)Fe(OH)3胶体,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2019年是“国际化学元素周期表年”。元素周期表中的成员数不断增加,ⅤA族元素是元素周期表中的重要组成元素。
(1)2016年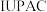 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,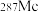 与
与 互为
互为______ 。
(2) 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: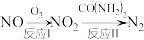
① 的电子式为
的电子式为______ ;反应Ⅰ为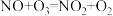 ,其中还原产物为
,其中还原产物为______ ;每消除 ,转移电子
,转移电子______  。
。
②反应Ⅱ中氧化产物与还原产物的质量比为______ 。
(3)①三碘化磷( )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为______ 。制备时常在溶剂中加入 ,其作用是
,其作用是______ 。
②亚磷酸( )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于______ 元酸(填“一”“二”或“三”), 属于
属于______ (填“正盐”或“酸式盐”)。亚磷酸具有强还原性,能与 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式______ 。
(1)2016年
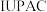 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,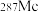 与
与 互为
互为(2)
 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: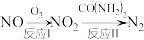
①
 的电子式为
的电子式为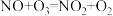 ,其中还原产物为
,其中还原产物为 ,转移电子
,转移电子 。
。②反应Ⅱ中氧化产物与还原产物的质量比为
(3)①三碘化磷(
 )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为 ,其作用是
,其作用是②亚磷酸(
 )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于 属于
属于 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
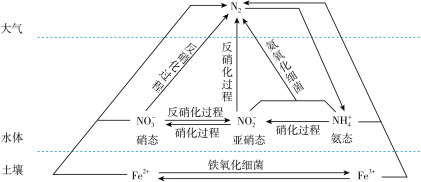
(1)如图所示氮循环中,属于氮的固定的有_______ (填字母序号)。
a. N2转化为氨态氮 b. 硝化过程 c. 反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去,用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:_______ ,
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将v L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为
。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为 的离子方程式是
的离子方程式是_______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O;  + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为_______ g /L。

(1)如图所示氮循环中,属于氮的固定的有
a. N2转化为氨态氮 b. 硝化过程 c. 反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)硝化过程中,含氮物质发生
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去,用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:将v L气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为
。向上述反应后溶液中加入v1 mL c1 mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2 mol·L−1 K2Cr2O7恰好反应。 NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O;  + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NO的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室中为了存放氯化亚铁溶液,经常在其中放入表面除锈的铁钉,防止Fe2+的氧化,以离子方程表示_______________ ;为了存放氯化铁溶液,经常在其中滴入一定量的盐酸,防止Fe3+的水解,以离子方程表示Fe3+的水解__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在生产生活中有极其重要的用途,请回答下列问题:
(1) 溶液可用于刻蚀铜制电路板,该反应的离子方程式为
溶液可用于刻蚀铜制电路板,该反应的离子方程式为________ 。
(2)要实现 转化为
转化为 ,可选用足量的
,可选用足量的________ (填字母)。
①亚硫酸钠溶液 ②稀盐酸 ③酸性 溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液
溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液
(3)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加________ ,若溶液变为_____ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,利用了维生素C的_____ 性。
(4)激光打印机的墨粉中含有 。
。 溶于过量的稀盐酸,反应的离子方程式为
溶于过量的稀盐酸,反应的离子方程式为___________ 。往反应后的溶液中滴加少量酸性 溶液,酸性
溶液,酸性 溶液褪色,
溶液褪色,_____ (填“能或不能”)说明反应后的溶液中含 。若不能,请说明原因:
。若不能,请说明原因:___________ 。
(5)高铁酸盐可作为饮用水的消毒剂和净水剂,工业上以 、
、 、
、 为原料制备高铁酸钾。
为原料制备高铁酸钾。
①高铁酸钠 中Fe的化合价为
中Fe的化合价为_____ 。
②配平制备 的离子方程式:
的离子方程式:______
__ +__
+__ +__=__
+__=__ +__
+__ +__
+__
每生成39.6g ,转移电子的数目为
,转移电子的数目为_____ 。
③已知 ,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因
,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因___________ 。
(1)
 溶液可用于刻蚀铜制电路板,该反应的离子方程式为
溶液可用于刻蚀铜制电路板,该反应的离子方程式为(2)要实现
 转化为
转化为 ,可选用足量的
,可选用足量的①亚硫酸钠溶液 ②稀盐酸 ③酸性
 溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液
溶液 ④铁粉 ⑤碘化钾溶液 ⑥过氧化氢溶液(3)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加(4)激光打印机的墨粉中含有
 。
。 溶于过量的稀盐酸,反应的离子方程式为
溶于过量的稀盐酸,反应的离子方程式为 溶液,酸性
溶液,酸性 溶液褪色,
溶液褪色, 。若不能,请说明原因:
。若不能,请说明原因:(5)高铁酸盐可作为饮用水的消毒剂和净水剂,工业上以
 、
、 、
、 为原料制备高铁酸钾。
为原料制备高铁酸钾。①高铁酸钠
 中Fe的化合价为
中Fe的化合价为②配平制备
 的离子方程式:
的离子方程式:__
 +__
+__ +__=__
+__=__ +__
+__ +__
+__
每生成39.6g
 ,转移电子的数目为
,转移电子的数目为③已知
 ,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因
,说明高铁酸盐既可作饮用水的消毒剂又可作净水剂的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】阅读下面两条科普信息,回答问题:
①一个体重50kg的健康人含铁2g,这2g铁在人体中不是以单质金属的形式存在,而是以Fe2+和Fe3+的形式存在.亚铁离子易被吸收,给贫血者补充铁时,应给予含亚离子的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的铁离子还原成亚铁离子,有于人体吸收。
②在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿;该反应的另一种反应物是CO2,反应后CO2转变成有机物甲醛:(用CH2O表示)。
问题:
这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径
(1)能在人体进行Fe2+和Fe3+的转化,这说明亚铁离子具有_________ 性,铁离子具有_________ 性;
(2)服用维生素C,可以使食物中的Fe3+还原成Fe2+,这句话指出维生素C是_______ 剂,具有_______ 性;
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为_________ ;离子方程式为:__________ 。
(4)第②条信息中的CO2做__________ 剂,写出②中的离子方程式_________ 。
①一个体重50kg的健康人含铁2g,这2g铁在人体中不是以单质金属的形式存在,而是以Fe2+和Fe3+的形式存在.亚铁离子易被吸收,给贫血者补充铁时,应给予含亚离子的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的铁离子还原成亚铁离子,有于人体吸收。
②在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿;该反应的另一种反应物是CO2,反应后CO2转变成有机物甲醛:(用CH2O表示)。
问题:
这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径
(1)能在人体进行Fe2+和Fe3+的转化,这说明亚铁离子具有
(2)服用维生素C,可以使食物中的Fe3+还原成Fe2+,这句话指出维生素C是
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为
(4)第②条信息中的CO2做
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠、铝、铁是三种非常重要的常见金属。根据所学知识完成下列填空。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为_______ 。
(2)足量的Fe在Cl2中点燃,所得产物的化学式是_______ 。将该产物溶于水配成溶液,分装在两支试管中。
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,现象为_______ 。
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为_______ 。若2.7g纯铝片投入足量盐酸中产生氢气的物质的量为_______ mol。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为
(2)足量的Fe在Cl2中点燃,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题。
(1)写出重晶石主要成分的化学式_______ 。
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式_______ 。
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是_______ 。
(1)写出重晶石主要成分的化学式
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据硫元素及其化合物有关知识填空:
(1)往纯净的 溶液中加入
溶液中加入 溶液,溶液
溶液,溶液___________ (填“变”或“不变”)色,再往其中通入氯气,溶液变___________ (填“红”或“黄”)色。
(2)浓硫酸与碳共热时发生反应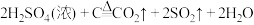 ,在该反应中,浓硫酸表现出
,在该反应中,浓硫酸表现出___________ (填“酸性”或“强氧化性”)。
(3)蓝矾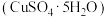 的摩尔质量是
的摩尔质量是___________ (填“160”或“250”) ,把浓硫酸滴在蓝矾固体上,固体表面变
,把浓硫酸滴在蓝矾固体上,固体表面变___________ (填“白”或“黑”),则浓硫酸表现___________ (填“吸水性”或“脱水性”);此反应是___________ (填“物理”或“化学”)变化。
(1)往纯净的
 溶液中加入
溶液中加入 溶液,溶液
溶液,溶液(2)浓硫酸与碳共热时发生反应
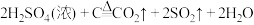 ,在该反应中,浓硫酸表现出
,在该反应中,浓硫酸表现出(3)蓝矾
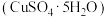 的摩尔质量是
的摩尔质量是 ,把浓硫酸滴在蓝矾固体上,固体表面变
,把浓硫酸滴在蓝矾固体上,固体表面变
您最近一年使用:0次



