根据所学知识,进行作答
(1)2023年第19届杭州亚运会场馆实现 覆盖,制作
覆盖,制作 芯片的材料为
芯片的材料为 (氮化镓),镓原子结构示意图为
(氮化镓),镓原子结构示意图为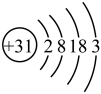 ,镓元素在元素周期表中的位置
,镓元素在元素周期表中的位置___________ 。
(2)2023年10月26日神舟十七号飞船成功对接太空站,为使宇航员有良好的生存环境,飞船中装有盛 颗粒的供氧装置。
颗粒的供氧装置。
① 中的氧元素的化合价为
中的氧元素的化合价为___________ 价。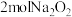 与水完全反应时,生成的氧气在标准状况下体积为
与水完全反应时,生成的氧气在标准状况下体积为___________ L。
②如用 (超氧化钾)代替
(超氧化钾)代替 ,也能达到同样的目的。写出
,也能达到同样的目的。写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
(3)2023年12月18日甘肃省发生地震灾害,受灾废墟需喷洒大量84消毒液的稀溶液进行消毒。84消毒液可由 与
与 溶液反应制得,其主要成分为
溶液反应制得,其主要成分为 。
。
①资料(3)涉及的物质中,属于碱的是___________ (填化学式,下同);属于盐的是___________ 。
②“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是___________ (用离子方程式表示),但“84消毒液”却不能与“洁厕灵”(浓盐酸)混合使用,原因是___________ (用离子方程式表示)。
(1)2023年第19届杭州亚运会场馆实现
 覆盖,制作
覆盖,制作 芯片的材料为
芯片的材料为 (氮化镓),镓原子结构示意图为
(氮化镓),镓原子结构示意图为 ,镓元素在元素周期表中的位置
,镓元素在元素周期表中的位置(2)2023年10月26日神舟十七号飞船成功对接太空站,为使宇航员有良好的生存环境,飞船中装有盛
 颗粒的供氧装置。
颗粒的供氧装置。①
 中的氧元素的化合价为
中的氧元素的化合价为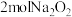 与水完全反应时,生成的氧气在标准状况下体积为
与水完全反应时,生成的氧气在标准状况下体积为②如用
 (超氧化钾)代替
(超氧化钾)代替 ,也能达到同样的目的。写出
,也能达到同样的目的。写出 与
与 反应的化学方程式
反应的化学方程式(3)2023年12月18日甘肃省发生地震灾害,受灾废墟需喷洒大量84消毒液的稀溶液进行消毒。84消毒液可由
 与
与 溶液反应制得,其主要成分为
溶液反应制得,其主要成分为 。
。①资料(3)涉及的物质中,属于碱的是
②“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是
更新时间:2024-01-30 10:12:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】磷的单质及其化合物用途非常广泛。完成下列填空:
(1)画出磷的原子结构示意图________ 。
(2)磷酸钙真空制磷的反应为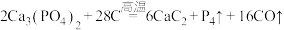 。该反应的氧化产物是
。该反应的氧化产物是________ (填化学式); 中的共价键的类型为
中的共价键的类型为________ 。
(3)次磷酸钠的结构为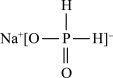 。
。
①次磷酸钠的化学式为________ ,磷的化合价为________ 。
②次磷酸钠为________ 盐(填“正”“酸式”)。
(1)画出磷的原子结构示意图
(2)磷酸钙真空制磷的反应为
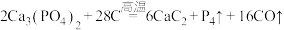 。该反应的氧化产物是
。该反应的氧化产物是 中的共价键的类型为
中的共价键的类型为(3)次磷酸钠的结构为
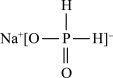 。
。①次磷酸钠的化学式为
②次磷酸钠为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列粒子(分子或离子)均含有18个电子:
请回答下列问题:
(1)A的元素符号是____________ ,B2-的结构示意图是________ 。
(2)C与D混合,发生反应的化学方程式为_____________________________________ 。
(3)E的电子式是________ ;F的水溶液常用于消毒剂,F的化学式是________ 。
| 粒子 | A+ | B2- | C | D | E | F |
| 组成特点 | 单核离子 | 化合物,双核分子 | 单质,双核分子 | 化合物,三核分子 | 化合物,四核分子 | |
请回答下列问题:
(1)A的元素符号是
(2)C与D混合,发生反应的化学方程式为
(3)E的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】中国青铜文化历史悠久、内容丰富,是世界文化宝库中的精华。古代青铜中含有铜、锡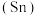 和铅
和铅 。回答下列问题:
。回答下列问题:
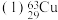 和
和 互称为
互称为________ ,其中 中的中子数与质子数之差为
中的中子数与质子数之差为________ 。
 锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为
锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为________ 。
 吕氏春秋
吕氏春秋 中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是
中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是________ 。
 天工开物
天工开物 中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化
中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化 ”
” 砂的主要成分为
砂的主要成分为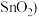 ,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为
,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为________ ,除去Sn中Pb的化学方程式为________ ,提纯除铅是利用了铅、锡的________ 的化学性质差异。
 现代工业中可用黄铜矿火法冶炼铜,反应之一为
现代工业中可用黄铜矿火法冶炼铜,反应之一为

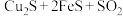 ,该反应每生成
,该反应每生成 转移电子的物质的量为
转移电子的物质的量为________ 。
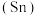 和铅
和铅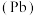 。回答下列问题:
。回答下列问题: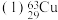 和
和 互称为
互称为 中的中子数与质子数之差为
中的中子数与质子数之差为 锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为
锡与碳同主族,比碳多三个电子层,锡的原子结构示意图为 吕氏春秋
吕氏春秋 中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是
中的“金柔锡柔,合两柔则为刚”,说明合金的一种性能是 天工开物
天工开物 中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化
中关于锡的冶炼及提纯有如下叙述“凡炼煎亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞲熔化 ”
” 砂的主要成分为
砂的主要成分为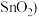 ,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为
,“售者杂铅太多,欲取净则熔化,入醋淬八九度,铅尽化灰而去”。生成Sn的化学方程式为 现代工业中可用黄铜矿火法冶炼铜,反应之一为
现代工业中可用黄铜矿火法冶炼铜,反应之一为

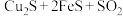 ,该反应每生成
,该反应每生成 转移电子的物质的量为
转移电子的物质的量为
您最近一年使用:0次
【推荐1】K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
(1)该反应中的还原剂是________________ 。
(2)若司机酒后开车,检测仪器内物质显示出____________ 色。
(3)在反应中,铬元素的化合价从_______ 价变为________ 价。
(4)写出并配平该反应的化学方程式________________ 。
(5)如果在反应中生成1mol氧化产物,转移的电子总数为_____________ 。
(1)该反应中的还原剂是
(2)若司机酒后开车,检测仪器内物质显示出
(3)在反应中,铬元素的化合价从
(4)写出并配平该反应的化学方程式
(5)如果在反应中生成1mol氧化产物,转移的电子总数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】全球气候变化对全球人类社会构成重大威胁。政府气候变化专门委员会(IPCC)报告认为,为了避免极端危害,世界必须将全球变暖幅度控制在1.5℃以内。只有全球都在21世纪中叶实现温室气体净零排放,才能有可能实现这一目标。请根据二氧化碳的利用回答下列问题:
(1)CO2催化氢化制甲烷的研究过程如图1:
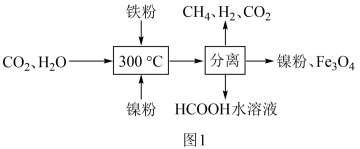
①上述过程中,加入铁粉的作用是__ 。
②HCOOH是CO2转化为CH4的中间体:CO2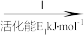 HCOOH
HCOOH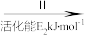 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是__ 。
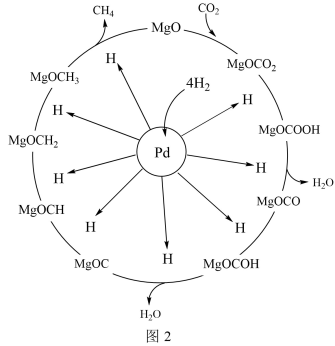
(2)一定条件下,Pd—Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为__ 。
(3)CO2加氢还可制备甲酸(HCOOH)。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=__ k正。
②温度为T2℃时,k正=1.1k逆,则T2℃时平衡压强__ (填“>”“<”或“=”)T1℃时平衡压强。
(4)N—甲基二乙醇胺(用MDEA表示)水溶液具有吸收能力强、对设备腐蚀小等特点,MDEA吸收CO2的反应可以表示为:MDEA(aq)+CO2(g)+H2O(l) MDEAH+(aq)+HCO
MDEAH+(aq)+HCO (aq) △H。
(aq) △H。
①已知MDEA中的氮具有一元碱(类似于NH3)的性质,Kb=5.2×10-4,已知H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,推测溶液MDEAHHCO3显__ 性(填酸,碱,中)。
②标准平衡常数Kθ可以表示平衡时各物质的浓度关系:如反应A(aq)+2B(g) C(g)+D(aq)的Kθ=
C(g)+D(aq)的Kθ=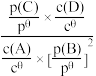 ,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=
,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=__ (计算结果保留两位小数)。
(5)设计二氧化碳熔盐捕获及电化学转化装置示意图如图:
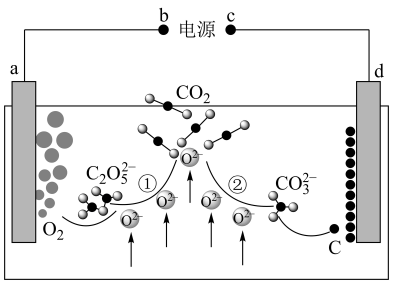
a极的电极反应式为__ 。
(1)CO2催化氢化制甲烷的研究过程如图1:

①上述过程中,加入铁粉的作用是
②HCOOH是CO2转化为CH4的中间体:CO2
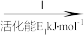 HCOOH
HCOOH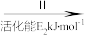 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是(2)一定条件下,Pd—Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为

(3)CO2加氢还可制备甲酸(HCOOH)。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=②温度为T2℃时,k正=1.1k逆,则T2℃时平衡压强
(4)N—甲基二乙醇胺(用MDEA表示)水溶液具有吸收能力强、对设备腐蚀小等特点,MDEA吸收CO2的反应可以表示为:MDEA(aq)+CO2(g)+H2O(l)
 MDEAH+(aq)+HCO
MDEAH+(aq)+HCO (aq) △H。
(aq) △H。①已知MDEA中的氮具有一元碱(类似于NH3)的性质,Kb=5.2×10-4,已知H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,推测溶液MDEAHHCO3显
②标准平衡常数Kθ可以表示平衡时各物质的浓度关系:如反应A(aq)+2B(g)
 C(g)+D(aq)的Kθ=
C(g)+D(aq)的Kθ=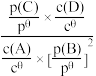 ,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=
,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=(5)设计二氧化碳熔盐捕获及电化学转化装置示意图如图:

a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】近年来,我国研究储氢碳管获得重大进展,用电弧法合成碳纳米管,常伴有大量碳纳米颗粒生成,这种碳纳米颗粒可用氧化气化法除去,其反应的化学方程式为:
C +K2Cr2O7 +H2SO4(稀) → CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)此反应的氧化剂________ ,还原剂___________ ;
(2)硫酸在上述反应中表现出的性质是__________ (填选项编号);
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目__________ 。
C +K2Cr2O7 +H2SO4(稀) → CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)此反应的氧化剂
(2)硫酸在上述反应中表现出的性质是
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】脱硫脱硝技术是指通过一系列的化学反应,将“三废”中有害的 、氮氧化物等转化为无害物质。
、氮氧化物等转化为无害物质。
(1)一种处理 废气的工艺流程如图所示。
废气的工艺流程如图所示。

①若 吸收塔内盛装的是
吸收塔内盛装的是 溶液,则气体
溶液,则气体 为
为___________ 。
②若 吸收塔内盛装的是
吸收塔内盛装的是 溶液,气体
溶液,气体 为空气,则
为空气,则 气体吸收塔内发生反应的离子方程式为
气体吸收塔内发生反应的离子方程式为___________ 。
(2)船舶柴油机废气中含有大量的氮氧化物 ,对大气环境和人类健康造成了不利影响。使用惰性电极,采用无隔膜电解槽电解海水,产生有效氯(主要包括
,对大气环境和人类健康造成了不利影响。使用惰性电极,采用无隔膜电解槽电解海水,产生有效氯(主要包括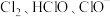 ),再利用循环喷淋模式对船舶废气进行处理。如图甲所示。电解海水溶液的初始
),再利用循环喷淋模式对船舶废气进行处理。如图甲所示。电解海水溶液的初始 对
对 和
和 (
( 与
与 总和)脱硝的影响如图乙所示。
总和)脱硝的影响如图乙所示。
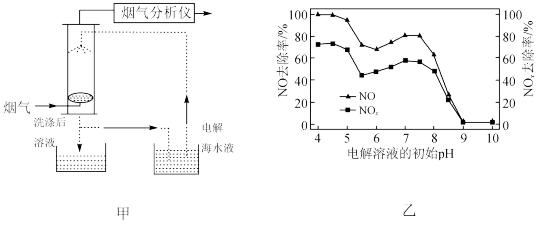
① 约为7.5时,有效氯成分中起主要作用的是
约为7.5时,有效氯成分中起主要作用的是___________ 。
② 时,
时, 去除率明显低于
去除率明显低于 去除率的原因是
去除率的原因是___________ 。
③当电解液的 从5.5下降到4.5时
从5.5下降到4.5时 和
和 的脱除率快速上升的主要原因是
的脱除率快速上升的主要原因是___________ 。
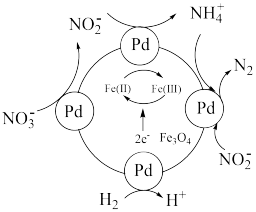
(3) 催化剂可将酸性废水中的
催化剂可将酸性废水中的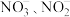 转化为
转化为 ,机理如图所示。
,机理如图所示。 中含有
中含有 价和
价和 价的铁,分别用
价的铁,分别用 (II)和
(II)和 (III))表示。
(III))表示。
① (II)中基态
(II)中基态 的核外电子排布式为
的核外电子排布式为___________ 。
②H2还原 的过程可描述为
的过程可描述为___________ 。
③每处理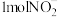 ,理论需要消耗标准状况下的H2
,理论需要消耗标准状况下的H2___________ L。
 、氮氧化物等转化为无害物质。
、氮氧化物等转化为无害物质。(1)一种处理
 废气的工艺流程如图所示。
废气的工艺流程如图所示。
①若
 吸收塔内盛装的是
吸收塔内盛装的是 溶液,则气体
溶液,则气体 为
为②若
 吸收塔内盛装的是
吸收塔内盛装的是 溶液,气体
溶液,气体 为空气,则
为空气,则 气体吸收塔内发生反应的离子方程式为
气体吸收塔内发生反应的离子方程式为(2)船舶柴油机废气中含有大量的氮氧化物
 ,对大气环境和人类健康造成了不利影响。使用惰性电极,采用无隔膜电解槽电解海水,产生有效氯(主要包括
,对大气环境和人类健康造成了不利影响。使用惰性电极,采用无隔膜电解槽电解海水,产生有效氯(主要包括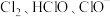 ),再利用循环喷淋模式对船舶废气进行处理。如图甲所示。电解海水溶液的初始
),再利用循环喷淋模式对船舶废气进行处理。如图甲所示。电解海水溶液的初始 对
对 和
和 (
( 与
与 总和)脱硝的影响如图乙所示。
总和)脱硝的影响如图乙所示。
①
 约为7.5时,有效氯成分中起主要作用的是
约为7.5时,有效氯成分中起主要作用的是②
 时,
时, 去除率明显低于
去除率明显低于 去除率的原因是
去除率的原因是③当电解液的
 从5.5下降到4.5时
从5.5下降到4.5时 和
和 的脱除率快速上升的主要原因是
的脱除率快速上升的主要原因是(3)
 催化剂可将酸性废水中的
催化剂可将酸性废水中的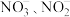 转化为
转化为 ,机理如图所示。
,机理如图所示。 中含有
中含有 价和
价和 价的铁,分别用
价的铁,分别用 (II)和
(II)和 (III))表示。
(III))表示。
①
 (II)中基态
(II)中基态 的核外电子排布式为
的核外电子排布式为②H2还原
 的过程可描述为
的过程可描述为③每处理
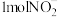 ,理论需要消耗标准状况下的H2
,理论需要消耗标准状况下的H2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某兴趣小组探究氯的单质及其化合物的性质。
Ⅰ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。
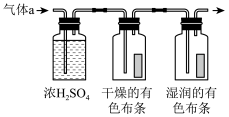
(1)浓硫酸的作用是___________ 。
(2)证明氯气和水反应的实验现象为___________ 。
(3)Cl2溶于水可制得氯水,检验氯水中的Cl-,可选择___________(填字母序号)试剂。
Ⅱ.回答下列问题
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。向“84消毒液”中滴入盐酸,可能发生反应: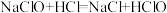 ,其属于
,其属于___________ (填四大基本反应类型)反应。乙同学认为上述过程中还发生了氧化还原反应并生成Cl2,反应的离子方程式为___________ 。
Ⅰ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。

(1)浓硫酸的作用是
(2)证明氯气和水反应的实验现象为
(3)Cl2溶于水可制得氯水,检验氯水中的Cl-,可选择___________(填字母序号)试剂。
| A.硝酸银溶液 | B.酚酞溶液 | C.碳酸钠溶液 | D.品红溶液 |
Ⅱ.回答下列问题
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。向“84消毒液”中滴入盐酸,可能发生反应:
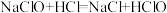 ,其属于
,其属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】图中,A是单质,B的焰色反应呈黄色。判断A、B、C、D的化学式:
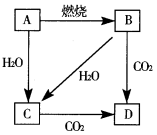
A_____ B______ C______ D______
下列转化的化学方程式为:
(1)A→B__________
(2)B→D________
(3)A→C__________

A
下列转化的化学方程式为:
(1)A→B
(2)B→D
(3)A→C
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求用化学用语表示下列过程
(1)Na元素相关的物质有很多且具有广泛的用途。NaOH可用于制造许多日用化工用品。某同学用含钠元素的不同类别 物质制备NaOH.写出符合要求的4个化学方程式:
①___________ ;
②___________ ;
③___________ ;
④___________ 。
(2) 溶液中逐滴滴加
溶液中逐滴滴加 溶液至
溶液至 恰好完全沉淀的离子方程式:
恰好完全沉淀的离子方程式:______ 。
(1)Na元素相关的物质有很多且具有广泛的用途。NaOH可用于制造许多日用化工用品。某同学用
①
②
③
④
(2)
 溶液中逐滴滴加
溶液中逐滴滴加 溶液至
溶液至 恰好完全沉淀的离子方程式:
恰好完全沉淀的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】1807年通过电解氢氧化钠制得金属钠,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是 。回答下列有关单质钠的问题:
。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是______ (填序号)。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
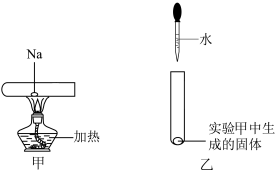
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应,如图甲所示,生成物的颜色为______ ,请写出该反应的化学方程式:__________________ 。将该试管冷却后直立,滴加几滴水,如图乙所示,发生反应的离子方程式为__________________ 。
 。回答下列有关单质钠的问题:
。回答下列有关单质钠的问题:(1)下列各项中属于保存金属钠的正确方法是
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应,如图甲所示,生成物的颜色为

您最近一年使用:0次



