按要求用化学用语表示下列过程
(1)Na元素相关的物质有很多且具有广泛的用途。NaOH可用于制造许多日用化工用品。某同学用含钠元素的不同类别 物质制备NaOH.写出符合要求的4个化学方程式:
①___________ ;
②___________ ;
③___________ ;
④___________ 。
(2) 溶液中逐滴滴加
溶液中逐滴滴加 溶液至
溶液至 恰好完全沉淀的离子方程式:
恰好完全沉淀的离子方程式:______ 。
(1)Na元素相关的物质有很多且具有广泛的用途。NaOH可用于制造许多日用化工用品。某同学用
①
②
③
④
(2)
 溶液中逐滴滴加
溶液中逐滴滴加 溶液至
溶液至 恰好完全沉淀的离子方程式:
恰好完全沉淀的离子方程式:
更新时间:2023-11-12 08:50:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D为四种可溶性的盐(离子不重复),它们的阳离子分别是Ba2+、Ag+、K+、Cu2+中的一种,阴离子分别是NO 、SO
、SO 、Cl-、CO
、Cl-、CO 的中的一种。
的中的一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有B盐的溶液呈蓝色。
②若向①的四支试管中分别加入盐酸,A盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断它们的化学式为:
(1)A_______ ,C_______
(2)C、D溶液混合后的现象是_______ 。
(3)写出足量盐酸与D反应的离子方程式:_______ ;写出B与Ba(OH)2溶液反应的离子方程式:_______
 、SO
、SO 、Cl-、CO
、Cl-、CO 的中的一种。
的中的一种。①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有B盐的溶液呈蓝色。
②若向①的四支试管中分别加入盐酸,A盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断它们的化学式为:
(1)A
(2)C、D溶液混合后的现象是
(3)写出足量盐酸与D反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求写出下列方程式:
(1)制备Fe(OH)3胶体的化学方程式:__________
(2)硫酸镁溶液与氢氧化钡溶液反应的离子方程式:___________
(3)氢氧化铜与盐酸反应的离子方程式:______________
(4)少量硫酸氢钠溶液与澄清石灰水反应的离子方程式:____________
(1)制备Fe(OH)3胶体的化学方程式:
(2)硫酸镁溶液与氢氧化钡溶液反应的离子方程式:
(3)氢氧化铜与盐酸反应的离子方程式:
(4)少量硫酸氢钠溶液与澄清石灰水反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列九种物质:①H2②铜③CO2④H2SO4⑤Ba(OH)2⑥熔融的NaHSO4⑦氨水⑧稀硝酸⑨Al2(SO4)3
(1)上述九种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为___________ 。
(2)⑨在水中的电离方程式为___________ 。
(3)以上属于电解质的共有___________ 种。
(4)将少量的③通入⑤的溶液中反应的离子方程式为___________ 。
(5)写出⑥的电离方程式___________ 。
(6)对于②与⑧的反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,当有1mol 发生反应时,转移电子的个数为
发生反应时,转移电子的个数为___________ ;当有3molCu发生反应时被还原的HNO3的物质的量为___________ 。
(1)上述九种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
(2)⑨在水中的电离方程式为
(3)以上属于电解质的共有
(4)将少量的③通入⑤的溶液中反应的离子方程式为
(5)写出⑥的电离方程式
(6)对于②与⑧的反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,当有1mol
 发生反应时,转移电子的个数为
发生反应时,转移电子的个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将固体钠溶于水配成体积为500ml 的溶液,收集到的气体在标况下的体积为44.8L 回答下列问题:
(1)写出反应的化学反应方程式_______________________________________ 。
(2)若要再配制80mL0.5mol·L-1 的稀氢氧化钠溶液,需用量筒量取上述原氢氧化钠溶液的体积为_____ mL。
(3)现有某浓度的浓氢氧化钠溶液,该氢氧化钠溶液的密度为1.3g/cm3,质量分数为27.4%,计算该氢氧化钠溶液的物质的量浓度是_____ mol/L。
(1)写出反应的化学反应方程式
(2)若要再配制80mL0.5mol·L-1 的稀氢氧化钠溶液,需用量筒量取上述原氢氧化钠溶液的体积为
(3)现有某浓度的浓氢氧化钠溶液,该氢氧化钠溶液的密度为1.3g/cm3,质量分数为27.4%,计算该氢氧化钠溶液的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钠、铝和铁是三种重要的金属。请回答:
(1)三种金属中,___________________ 既能与盐酸又能与氢氧化钠溶液反应,且生成物均为盐和氢气。写出该物质与氢氧化钠溶液反应的化学方程式__________________________
(2)三种金属在一定条件下均能与水发生反应。其中,铁与水蒸气反应的化学方程式为:____________________ 。
(3)钠与水反应时可观察到的实验现象有__________ (填序号);钠与水反应的化学方程式为:_________________
a.钠沉入水底 b.钠熔成小球 c.钠四处游动 d.溶液变为红色
(1)三种金属中,
(2)三种金属在一定条件下均能与水发生反应。其中,铁与水蒸气反应的化学方程式为:
(3)钠与水反应时可观察到的实验现象有
a.钠沉入水底 b.钠熔成小球 c.钠四处游动 d.溶液变为红色
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】以食盐为钠源制备纯碱的一种工艺流程如图。
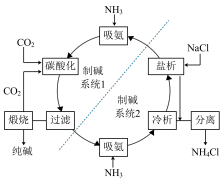
(1)熔融氯化钠可以导电是因为___________ (用化学用语解释)。
(2)电解熔融NaCl可制得单质钠,钠与水反应的化学方程式为___________ 。
(3)需要100mL0.1mol/L的NaCl溶液,配制时需用托盘天平称取NaCl固体___________ g。
(4)制碱系统1中,饱和食盐水吸氨后通入过量CO2碳酸化,过滤。
①滤渣的成分是___________ (填化学式),煅烧滤渣制取纯碱的化学方程式为___________ 。
②滤渣成分可作膨松剂,制馒头时与食醋(CH3COOH)共用效果更佳,相关的离子方程式为______ 。
(5)该流程中,可以循环利用的物质有CO2和___________ 。

(1)熔融氯化钠可以导电是因为
(2)电解熔融NaCl可制得单质钠,钠与水反应的化学方程式为
(3)需要100mL0.1mol/L的NaCl溶液,配制时需用托盘天平称取NaCl固体
(4)制碱系统1中,饱和食盐水吸氨后通入过量CO2碳酸化,过滤。
①滤渣的成分是
②滤渣成分可作膨松剂,制馒头时与食醋(CH3COOH)共用效果更佳,相关的离子方程式为
(5)该流程中,可以循环利用的物质有CO2和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钠及其化合物是重要的化学物质。回答下列问题:
(1) 、
、 、
、 、
、 久置空气中最终都变为
久置空气中最终都变为_________ (填化学式)。
(2)小块金属钠投入水中发生反应的离子方程式为_________ 。
(3) 、
、 都属于
都属于_________ (“碱性氧化物”或“氧化物”),可用蒸馏水检验 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:_________ 。
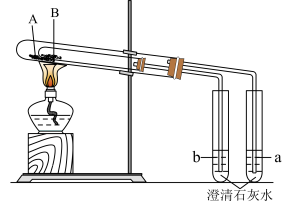
(4)如图装置可用于鉴别 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的_________ 性质加以鉴别。实验中可观察到b中澄清石灰水变浑浊,则物质A为_________ (填名称)。
(5) 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、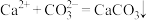 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
(1)
 、
、 、
、 、
、 久置空气中最终都变为
久置空气中最终都变为(2)小块金属钠投入水中发生反应的离子方程式为
(3)
 、
、 都属于
都属于 中混有少量
中混有少量 ,试用化学方程式解释含有
,试用化学方程式解释含有 的现象:
的现象:(4)如图装置可用于鉴别
 和
和 ,这是根据它们具有不同的
,这是根据它们具有不同的
(5)
 溶液与
溶液与 溶液混合产生
溶液混合产生 白色沉淀。生成
白色沉淀。生成 的反应过程:
的反应过程: 、
、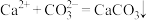 。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:
。某同学设计了如下实验方案,验证上述反应过程,请将方案补充完整:| 实验步骤 | 实验现象 |
ⅰ.取少量 溶液,向其中加入适量 溶液,向其中加入适量 溶液 溶液 | 无明显现象 |
| ⅱ.向上述溶液中滴加 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一块表面已被氧化为氧化钠的钠块17.0 g,投入50 g水中,最多能产生0.2 g气体,则:
(1)涉及的化学方程式为_______ ,_______ 。
(2)钠块中钠的质量是_______ g。
(3)钠块中氧化钠的质量是_______ g。
(4)原来钠块中被氧化的钠的质量是_______ g。
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是_______ 。
(1)涉及的化学方程式为
(2)钠块中钠的质量是
(3)钠块中氧化钠的质量是
(4)原来钠块中被氧化的钠的质量是
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】A是一种常见的金属单质,B、C、D、E是含有A元素的常见化合物,转化关系如图所示:
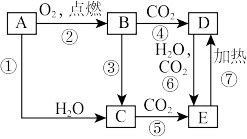
回答下列问题:
(1)上述①~⑦反应中,A元素化合价发生变化的有____ (填标号)。
(2)E的化学式为_____ ,写出该物质的一种用途____ 。
(3)反应③的离子方程式为_____ ;反应⑥的化学方程式为_____ 。

回答下列问题:
(1)上述①~⑦反应中,A元素化合价发生变化的有
(2)E的化学式为
(3)反应③的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知钠、氯及其化合物间有如下转化关系,请按要求填空。
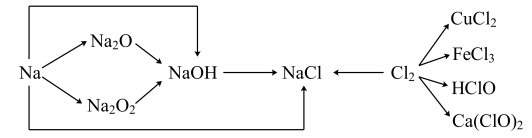
(1)一小块金属钠投入水中反应的化学方程式是___________ 。若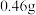 金属钠完全与水反应,可产生标准状况下H2的体积是
金属钠完全与水反应,可产生标准状况下H2的体积是___________ L,若反应后所得溶液为 ,则
,则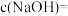
___________  。
。
(2) 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为___________ 、___________ 。
(3)新制的氯水中加入打磨过的镁条,观察到的现象是___________ ;请写出氯气与水反应的化学方程式:___________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为___________ 。

(1)一小块金属钠投入水中反应的化学方程式是
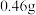 金属钠完全与水反应,可产生标准状况下H2的体积是
金属钠完全与水反应,可产生标准状况下H2的体积是 ,则
,则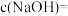
 。
。(2)
 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为(3)新制的氯水中加入打磨过的镁条,观察到的现象是
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精、含氯消毒剂、过氧乙酸等可有效灭活病毒。回答下列问题:
(1)Cl2是最早用于饮用水消毒的物质,主要是利用Cl2溶于水生成的次氯酸灭活病毒。
①Cl2与水反应的化学方程式为_______ 。
②氯水经光照后酸性增强,用化学方程表示其原因:_______ 。
(2)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。
①漂白液的有效成分为_______ 。
②它的消毒原理是_______ (用化学方程式表示)。
③由以上反应证明 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸_______ 。
④工业生产漂白粉的化学方程式为_______ 。
(3)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8gNa2O2中阴离子的物质的量为_______ 。
(4)将 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为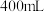 。试计算:
。试计算:
①原混合物中 的质量为
的质量为_______  。
。
②所得溶液的物质的量浓度为_______  。
。
(1)Cl2是最早用于饮用水消毒的物质,主要是利用Cl2溶于水生成的次氯酸灭活病毒。
①Cl2与水反应的化学方程式为
②氯水经光照后酸性增强,用化学方程表示其原因:
(2)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。
①漂白液的有效成分为
②它的消毒原理是
③由以上反应证明
 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸④工业生产漂白粉的化学方程式为
(3)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8gNa2O2中阴离子的物质的量为
(4)将
 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为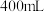 。试计算:
。试计算:①原混合物中
 的质量为
的质量为 。
。②所得溶液的物质的量浓度为
 。
。
您最近一年使用:0次



