全球气候变化对全球人类社会构成重大威胁。政府气候变化专门委员会(IPCC)报告认为,为了避免极端危害,世界必须将全球变暖幅度控制在1.5℃以内。只有全球都在21世纪中叶实现温室气体净零排放,才能有可能实现这一目标。请根据二氧化碳的利用回答下列问题:
(1)CO2催化氢化制甲烷的研究过程如图1:
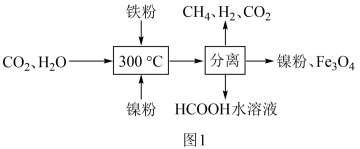
①上述过程中,加入铁粉的作用是__ 。
②HCOOH是CO2转化为CH4的中间体:CO2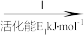 HCOOH
HCOOH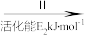 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是__ 。
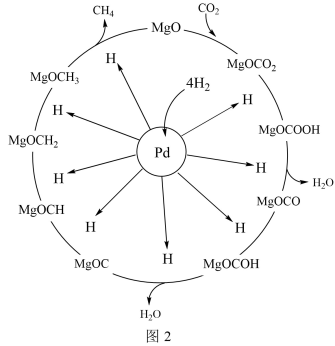
(2)一定条件下,Pd—Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为__ 。
(3)CO2加氢还可制备甲酸(HCOOH)。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=__ k正。
②温度为T2℃时,k正=1.1k逆,则T2℃时平衡压强__ (填“>”“<”或“=”)T1℃时平衡压强。
(4)N—甲基二乙醇胺(用MDEA表示)水溶液具有吸收能力强、对设备腐蚀小等特点,MDEA吸收CO2的反应可以表示为:MDEA(aq)+CO2(g)+H2O(l) MDEAH+(aq)+HCO
MDEAH+(aq)+HCO (aq) △H。
(aq) △H。
①已知MDEA中的氮具有一元碱(类似于NH3)的性质,Kb=5.2×10-4,已知H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,推测溶液MDEAHHCO3显__ 性(填酸,碱,中)。
②标准平衡常数Kθ可以表示平衡时各物质的浓度关系:如反应A(aq)+2B(g) C(g)+D(aq)的Kθ=
C(g)+D(aq)的Kθ=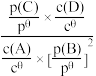 ,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=
,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=__ (计算结果保留两位小数)。
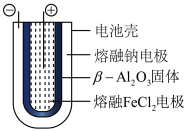
(5)设计二氧化碳熔盐捕获及电化学转化装置示意图如图:
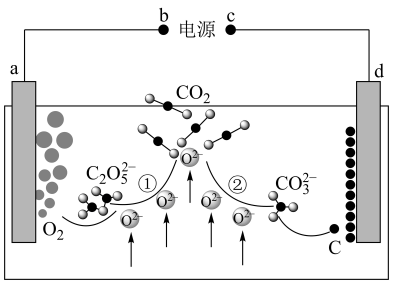
a极的电极反应式为__ 。
(1)CO2催化氢化制甲烷的研究过程如图1:

①上述过程中,加入铁粉的作用是
②HCOOH是CO2转化为CH4的中间体:CO2
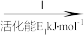 HCOOH
HCOOH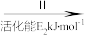 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是(2)一定条件下,Pd—Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为

(3)CO2加氢还可制备甲酸(HCOOH)。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=②温度为T2℃时,k正=1.1k逆,则T2℃时平衡压强
(4)N—甲基二乙醇胺(用MDEA表示)水溶液具有吸收能力强、对设备腐蚀小等特点,MDEA吸收CO2的反应可以表示为:MDEA(aq)+CO2(g)+H2O(l)
 MDEAH+(aq)+HCO
MDEAH+(aq)+HCO (aq) △H。
(aq) △H。①已知MDEA中的氮具有一元碱(类似于NH3)的性质,Kb=5.2×10-4,已知H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,推测溶液MDEAHHCO3显
②标准平衡常数Kθ可以表示平衡时各物质的浓度关系:如反应A(aq)+2B(g)
 C(g)+D(aq)的Kθ=
C(g)+D(aq)的Kθ=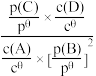 ,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=
,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=(5)设计二氧化碳熔盐捕获及电化学转化装置示意图如图:

a极的电极反应式为
21-22高三上·辽宁铁岭·阶段练习 查看更多[2]
更新时间:2021-12-16 09:36:37
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题:
Ⅱ.NOx含量的测定
将V L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3−,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3−的离子方程式是___________ 。
(2)滴定过程中发生下列反应:
3Fe2++NO3−+4H+=NO↑+3Fe3++2H2O
Cr2O72− + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为_________ mg·m−3。
Ⅱ.NOx含量的测定
将V L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3−,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。
(1)NO被H2O2氧化为NO3−的离子方程式是
(2)滴定过程中发生下列反应:
3Fe2++NO3−+4H+=NO↑+3Fe3++2H2O
Cr2O72− + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O
则气样中NOx折合成NO2的含量为
您最近一年使用:0次
【推荐2】高锰酸钾是一种典型的强氧化剂。完成下列填空:
Ⅰ:在用 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:
①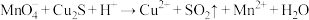 (未配平)
(未配平)
②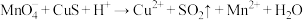 (未配平)
(未配平)
(1)下列关于反应①的说法中错误的是___________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下) ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mol
d.还原性的强弱关系是: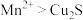
Ⅱ:在稀硫酸中, 与也能发生氧化还原反应。
与也能发生氧化还原反应。
(2)配平 与
与 反应的离子方程式:
反应的离子方程式:___________

(3)欲配制480mL0.1mol/L 溶液,需称取
溶液,需称取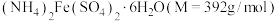 的质量为
的质量为___________ g,需要的玻璃仪器有___________ 。
Ⅲ:实验室可由软锰矿(主要成分为 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和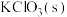 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:
(4)用软锰矿制备 的化学方程式是:
的化学方程式是:___________ 。
(5) 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为___________ 。
Ⅰ:在用
 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:①
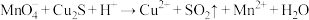 (未配平)
(未配平)②
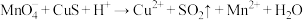 (未配平)
(未配平)(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下)
 ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mold.还原性的强弱关系是:
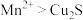
Ⅱ:在稀硫酸中,
 与也能发生氧化还原反应。
与也能发生氧化还原反应。(2)配平
 与
与 反应的离子方程式:
反应的离子方程式:
(3)欲配制480mL0.1mol/L
 溶液,需称取
溶液,需称取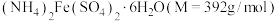 的质量为
的质量为Ⅲ:实验室可由软锰矿(主要成分为
 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和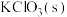 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:(4)用软锰矿制备
 的化学方程式是:
的化学方程式是:(5)
 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)意大利罗马大学的FulvioCacsce 等人获得了极具理论研究意义的N4 分子。N4与N2是氮元素的______________ ,它们的性质_____________ 。(填“相同”或“不同”)
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C= K2S+N2↑ +3CO2↑,反应中被还原的物质是______________ (填化学式)
(3)过氧化钠与CO2反应的化学方程式:_______________________________________ ;其中氧化剂是________________ ,还原剂是___________________ 。
(4)在常温下,将氯气通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式___________________________________ 。该漂白液的有效成分是___________ (填名称)。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C= K2S+N2↑ +3CO2↑,反应中被还原的物质是
(3)过氧化钠与CO2反应的化学方程式:
(4)在常温下,将氯气通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
(1)上述反应符合“原子经济”原则的是_______ (填“Ⅰ”或“Ⅱ”),反应I的化学平衡常数表达式K=_______ 。
(2)下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
①由表中数据判断ΔH2 _______ 0(填“>”、“<”或“=”);
②若容器容积不变,下列措施可增加甲醇产率的是_______ ;
A、升高温度 B、将CH3OH(g)从体系中分离 C、使用合适的催化剂 D、充入He,使体系总压强增大 E、按原比例再充入CO和H2
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为_______ ,此时的温度为_______ (从上表中选择)。
反应I:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1反应II:CO(g)+2H2(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2(1)上述反应符合“原子经济”原则的是
(2)下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②若容器容积不变,下列措施可增加甲醇产率的是
A、升高温度 B、将CH3OH(g)从体系中分离 C、使用合适的催化剂 D、充入He,使体系总压强增大 E、按原比例再充入CO和H2
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】300℃时,将气体X和气体Y各0.18mol充入10L恒容密闭容器中,发生反应: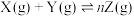 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:
回答下列问题:
(1)n=___________ ;0~2min内的平均反应速率v(Z)=___________ ;4min时,v正___________ (填“>”“<”或“=”)v逆。
(2)能判断该反应已经达到平衡状态的是___________ (填字母)。
a.生成X的速率是生成Z的速率的2倍 b.容器内压强保持不变
c.容器内气体的密度保持不变 d.容器内各气体的浓度保持不变
(3)反应达到平衡时Z的物质的量为___________ ;平衡时X的转化率为___________ (保留1位小数)。
(4)若起始时向该容器中充入X、Y、Z各0.12mol,则反应将向___________ (填“正”或“逆”)反应方向进行。
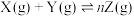 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| n(Z)/mol | 0.12 |
(1)n=
(2)能判断该反应已经达到平衡状态的是
a.生成X的速率是生成Z的速率的2倍 b.容器内压强保持不变
c.容器内气体的密度保持不变 d.容器内各气体的浓度保持不变
(3)反应达到平衡时Z的物质的量为
(4)若起始时向该容器中充入X、Y、Z各0.12mol,则反应将向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有电解质溶液:①Na2CO3②NaHCO3③CH3COONa ④ NaOH
(1)当四种溶液的pH相同时,其物质的量浓度由大到小的顺序是_________________ (填编号,以下相同)
(2)在上述四种电解质溶液中,分别加入AlCl3溶液,无气体产生的是_____________
(1)当四种溶液的pH相同时,其物质的量浓度由大到小的顺序是
(2)在上述四种电解质溶液中,分别加入AlCl3溶液,无气体产生的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】碳酸氢钠俗称“小苏打”,在生活、生产中用途广泛。
(1)泡沫灭火器中主要成分是NaHCO3溶液和Al2(SO4)3溶液,两者混合后发生双水解反应生成Al(OH)3和CO2进行灭火,写出该反应的化学方程式_______________ 。
(2)Na2O2和NaHCO3属于钠的化合物,它具有很强的氧化性。少量Na2O2与FeCl2溶液能发生如下反应:__ Na2O2+__ FeCl2+__ H2O→__ Fe(OH)3+__ FeCl3+__ NaCl,已知FeCl2前面系数为6,配平上述化学方程式,并用单线桥法标出电子转移方向和数目______ 。
(3)向NaHCO3溶液中加入少许Ba(OH)2固体,忽略溶液体积变化,溶液中的c(CO )的变化是
)的变化是_________ (选填“增大”、“减小”或“不变”)。
(4)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤 ②不通入氨,冷却、加食盐,过滤对两种方法的评价正确的是______ (选填编号)。
A.①析出的氯化铵纯度更高
B.②析出的氯化铵纯度更高
C.①②析出的氯化铵纯度一样
D.无法判断纯度高低
(5)已知HCO 在水中既能水解也能电离。NaHCO3溶液呈碱性,溶液中c(H2CO3)
在水中既能水解也能电离。NaHCO3溶液呈碱性,溶液中c(H2CO3) _____ c(CO )(选填“>”、“<”、“=”)。
)(选填“>”、“<”、“=”)。
(1)泡沫灭火器中主要成分是NaHCO3溶液和Al2(SO4)3溶液,两者混合后发生双水解反应生成Al(OH)3和CO2进行灭火,写出该反应的化学方程式
(2)Na2O2和NaHCO3属于钠的化合物,它具有很强的氧化性。少量Na2O2与FeCl2溶液能发生如下反应:
(3)向NaHCO3溶液中加入少许Ba(OH)2固体,忽略溶液体积变化,溶液中的c(CO
 )的变化是
)的变化是(4)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤 ②不通入氨,冷却、加食盐,过滤对两种方法的评价正确的是
A.①析出的氯化铵纯度更高
B.②析出的氯化铵纯度更高
C.①②析出的氯化铵纯度一样
D.无法判断纯度高低
(5)已知HCO
 在水中既能水解也能电离。NaHCO3溶液呈碱性,溶液中c(H2CO3)
在水中既能水解也能电离。NaHCO3溶液呈碱性,溶液中c(H2CO3)  )(选填“>”、“<”、“=”)。
)(选填“>”、“<”、“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
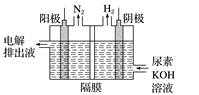
【推荐1】电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图所示(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阴极的电极反应式为_____________________ 。阳极的电极反应式为_________________________ 。

您最近一年使用:0次
【推荐2】根据要求,回答下列问题:
Ⅰ.原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池的工作原理示意图。
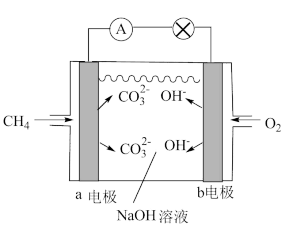
①电池的负极是__ 电极(填“a”或“b”),该极的电极反应为__ 。
②电池工作一段时间后,电解质溶液的pH__ (填“增大”“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应为CO+CO -2e-=2CO2。
-2e-=2CO2。
①正极反应是__ 。
②总反应是__ 。
Ⅱ.防止或减少钢铁的腐蚀有多种方法,如制成耐腐蚀合金,表面“烤蓝”,电镀另一种金属以及电化学保护等方法。
(3)钢铁的腐蚀主要是吸氧腐蚀。钢铁发生吸氧腐蚀时,负极反应为___ ,正极反应为___ 。
(4)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的___ 极(填“正”或“负”)相连,把镀层金属铬作___ 极(填“阳”或“阴”)。电镀铬时,不能用含有CrO 或Cr2O
或Cr2O 的溶液作电镀液,原因是
的溶液作电镀液,原因是___ 。
(5)利用如图装置,可以模拟铁的电化学保护。
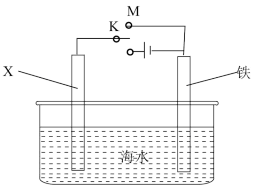
若X为碳棒,为减缓铁的腐蚀,开关K应置于___ 处(填“M”或“N”)。若X为锌,开关K置于M处,该电化学保护法称为__ 。
Ⅰ.原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池的工作原理示意图。

①电池的负极是
②电池工作一段时间后,电解质溶液的pH
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应为CO+CO
 -2e-=2CO2。
-2e-=2CO2。①正极反应是
②总反应是
Ⅱ.防止或减少钢铁的腐蚀有多种方法,如制成耐腐蚀合金,表面“烤蓝”,电镀另一种金属以及电化学保护等方法。
(3)钢铁的腐蚀主要是吸氧腐蚀。钢铁发生吸氧腐蚀时,负极反应为
(4)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的
 或Cr2O
或Cr2O 的溶液作电镀液,原因是
的溶液作电镀液,原因是(5)利用如图装置,可以模拟铁的电化学保护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图。
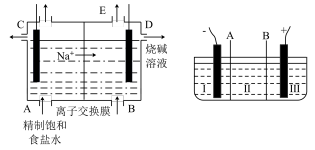
(1)下列说法不正确的是__________
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加 Na2CO3溶液
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),在这种电解池中电解Na2SO4溶液可制得氢氧化钠、硫酸等物质。A为_______ 离子交换膜、B为_______ 离子交换膜(填“阴”或“阳”),电极均为惰性电极。Na2SO4溶液应该在_______ 区(填“I”、“II”、“III”)加入。通电电解时阴极的电极反应式为_______ ,在III区得到_______ 。当外电路总共通过30 mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为:_______

(1)下列说法不正确的是
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加 Na2CO3溶液
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),在这种电解池中电解Na2SO4溶液可制得氢氧化钠、硫酸等物质。A为
您最近一年使用:0次

 、压强
、压强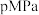 下发生反应:
下发生反应: 。平衡时,若
。平衡时,若 的分压为
的分压为 (列式即可,下同),平衡常数
(列式即可,下同),平衡常数
 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
 、
、 ,HB的
,HB的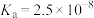 。
。 NaB溶液的
NaB溶液的
 。
。