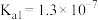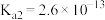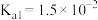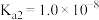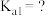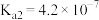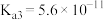水体中的含氮化合物(以 、
、 、
、 等形式存在)是主要的污染物之一,需对其进行无害化处理。
等形式存在)是主要的污染物之一,需对其进行无害化处理。
(1)酸性废水中的氨氮(主要是以 形式存在)可以通过沉淀法或是氧化还原法除去。
形式存在)可以通过沉淀法或是氧化还原法除去。
①向该酸性废水中加入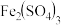 溶液,反应后生成
溶液,反应后生成 沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为
沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为___________ 价,除去氨氮的过程中生成 沉淀的反应的离子方程式为
沉淀的反应的离子方程式为___________ 。
②向该酸性废水中加入NaClO溶液可将 转化成无害气体放出,发生反应的离子方程式为
转化成无害气体放出,发生反应的离子方程式为___________ ;NaCl可以通过 与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为
与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)利用厌氧氨氧化菌细胞中的三种酶处理废水中含氮粒子的反应机理如图所示。

①从图中可以看出该废水中含氮粒子主要以___________ 形式存在,图中1mol  中存在的共价键数目为
中存在的共价键数目为___________  。
。
②在NR酶的作用下, 发生了
发生了___________ (填“氧化反应”或“还原反应”), 在HH酶的催化下与
在HH酶的催化下与 发生反应,生成两种产物的化学方程式为
发生反应,生成两种产物的化学方程式为___________ 。
 、
、 、
、 等形式存在)是主要的污染物之一,需对其进行无害化处理。
等形式存在)是主要的污染物之一,需对其进行无害化处理。(1)酸性废水中的氨氮(主要是以
 形式存在)可以通过沉淀法或是氧化还原法除去。
形式存在)可以通过沉淀法或是氧化还原法除去。①向该酸性废水中加入
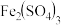 溶液,反应后生成
溶液,反应后生成 沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为
沉淀,达到除去氨氮的目的。该沉淀中铁元素的化合价为 沉淀的反应的离子方程式为
沉淀的反应的离子方程式为②向该酸性废水中加入NaClO溶液可将
 转化成无害气体放出,发生反应的离子方程式为
转化成无害气体放出,发生反应的离子方程式为 与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为
与NaOH溶液反应制得,该反应中氧化剂与还原剂的物质的量之比为(2)利用厌氧氨氧化菌细胞中的三种酶处理废水中含氮粒子的反应机理如图所示。

①从图中可以看出该废水中含氮粒子主要以
 中存在的共价键数目为
中存在的共价键数目为 。
。②在NR酶的作用下,
 发生了
发生了 在HH酶的催化下与
在HH酶的催化下与 发生反应,生成两种产物的化学方程式为
发生反应,生成两种产物的化学方程式为
更新时间:2022-03-17 07:20:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知25℃时有关弱酸的电离平衡常数如表。
(1)已知常温下,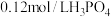 溶液pH=1.7,则磷酸的
溶液pH=1.7,则磷酸的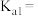
_______ (已知 )
)
(2)等体积等浓度的 和NaCN溶液中的离子总数大小关系为:
和NaCN溶液中的离子总数大小关系为:
_______ NaCN(填“大于”,“小于”或“等于”)
(3)向 溶液中通入过量
溶液中通入过量 的离子反应方程式为
的离子反应方程式为_____________________
(4)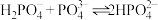 的平衡常数K=
的平衡常数K=______________ (填数值)
(5)将 通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:
通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:_____________________
弱酸 | HCN |
|
|
|
|
电离平衡常数 |
|
|
|
|
|
(1)已知常温下,
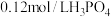 溶液pH=1.7,则磷酸的
溶液pH=1.7,则磷酸的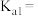
 )
)(2)等体积等浓度的
 和NaCN溶液中的离子总数大小关系为:
和NaCN溶液中的离子总数大小关系为:
(3)向
 溶液中通入过量
溶液中通入过量 的离子反应方程式为
的离子反应方程式为(4)
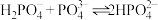 的平衡常数K=
的平衡常数K=(5)将
 通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:
通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:
您最近一年使用:0次
【推荐2】(1)按要求写出电子式:CO2_________ COCl2_________ NaCN______ N2H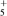
_______
(2)元素周期表中“对角线规则”是指处于周期表中对角线位置(左上和右下方)的两元素,其性质具有相似性,例如:Be和Al处于对角线位置。写出Be与氢氧化钠溶液反应的化学方程式:_________________________________ 。
(3)写出氢,氧,钠,硫四种元素组成的两种酸式盐发生复分解反应的离子方程式:___________________ 。
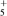
(2)元素周期表中“对角线规则”是指处于周期表中对角线位置(左上和右下方)的两元素,其性质具有相似性,例如:Be和Al处于对角线位置。写出Be与氢氧化钠溶液反应的化学方程式:
(3)写出氢,氧,钠,硫四种元素组成的两种酸式盐发生复分解反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:_______ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾)。取补铁剂少许溶于水配成溶液,_______ (填写实验操作、现象和结论)
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(3)镁铝合金的硬度比金属铝的硬度_______ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为_______ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3,合金中镁铝的物质的量之比为_______ 。
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾)。取补铁剂少许溶于水配成溶液,
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(3)镁铝合金的硬度比金属铝的硬度
您最近一年使用:0次
【推荐1】过氧化氢被称为绿色氧化剂,在实验、医疗、化工、生产工艺等方面有广泛的应用,请回答下列有关H2O2的问题:
(1)H2O2中O的化合价为_______ 价,具有_______ (填“氧化性”或“还原性”或“氧化性和还原性”)。
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是:_______H2O2 +_______KMnO4 +_______H2SO4= _______+_______MnSO4 +_______O2↑ +_______H2O
已知:稀 溶液几乎无色。
溶液几乎无色。
①请将上述化学方程式配平;___________
②上述反应中的还原剂为_______ (填化学式),被还原的元素是_______ (填元素符号)。
③向酸性 溶液中滴入双氧水,观察到的现象是
溶液中滴入双氧水,观察到的现象是_______ ,反应后溶液的pH_______ (填“增大”“减小”或“不变”)。
④0.3mol 参加上述反应,转移电子
参加上述反应,转移电子_______ mol。
(3)酸性条件下,在FeCl3和FeCl2的混合溶液中加入H2O2以除去Fe2+,反应的离子方程式_______ 。
(4)H2O2可用于SO2的尾气处理,请写出反应的化学方程式_______ 。
(1)H2O2中O的化合价为
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是:_______H2O2 +_______KMnO4 +_______H2SO4= _______+_______MnSO4 +_______O2↑ +_______H2O
已知:稀
 溶液几乎无色。
溶液几乎无色。①请将上述化学方程式配平;
②上述反应中的还原剂为
③向酸性
 溶液中滴入双氧水,观察到的现象是
溶液中滴入双氧水,观察到的现象是④0.3mol
 参加上述反应,转移电子
参加上述反应,转移电子(3)酸性条件下,在FeCl3和FeCl2的混合溶液中加入H2O2以除去Fe2+,反应的离子方程式
(4)H2O2可用于SO2的尾气处理,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题。
(1)有下列反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④CO2+2NaOH=Na2CO3+H2O
上述反应中不属于氧化还原反应的是_______ (填序号,下同);H2O只作还原剂的是_______ ;属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是_______ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目_______ 。
②若消耗30 g的NO得到还原产物的质量为_______ g。
(1)有下列反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④CO2+2NaOH=Na2CO3+H2O
上述反应中不属于氧化还原反应的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②若消耗30 g的NO得到还原产物的质量为
您最近一年使用:0次
【推荐3】黑火药是我国古代科技四大发明之一,在化学史上占有重要地位,黑火药主要是硝酸钾、硫磺、木炭三者粉末的混合物,在点燃条件下,其化学反应式主要为:KNO3+S+C →N2↑+CO2↑+K2S
试填下列空白.
(1)在黑火药燃烧的反应中,氧化剂为____ ,被氧化的物质为_____ 。
(2)根据化学反应式分析,一个硫原子参与反应时____ (得到或失去)____ 个电子。
(3)黑火药燃烧后的固体残留物中,除了K2S外,还有少许K2CO3、K2SO4和未燃烧的炭末,请设计一个简单的实验证明,黑火药燃烧的固体产物中存在K2CO3。
[实验方案]
①取黑火药燃烧后的固体残留物于烧杯中,加适量水溶解,过滤,得无色澄清溶液;
②用洁净的铂丝蘸取滤液,将铂丝放在酒精灯火焰上灼烧,透过蓝色钴玻璃片观察火焰,若火焰呈紫色,则证明含K+;
③___________ 。
试填下列空白.
(1)在黑火药燃烧的反应中,氧化剂为
(2)根据化学反应式分析,一个硫原子参与反应时
(3)黑火药燃烧后的固体残留物中,除了K2S外,还有少许K2CO3、K2SO4和未燃烧的炭末,请设计一个简单的实验证明,黑火药燃烧的固体产物中存在K2CO3。
[实验方案]
①取黑火药燃烧后的固体残留物于烧杯中,加适量水溶解,过滤,得无色澄清溶液;
②用洁净的铂丝蘸取滤液,将铂丝放在酒精灯火焰上灼烧,透过蓝色钴玻璃片观察火焰,若火焰呈紫色,则证明含K+;
③
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有①Na2S、②金刚石、③NH4Cl、④Na2SO4、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是____________ ,熔化时需要破坏共价键的是____________ ,熔点最高的是____________ ,熔点最低的是_____________ (填序号)。
(2)属于离子化合物的是_______________________ ,只有离子键的物质是____________ ,晶体以分子间作用力结合的是____________________ (填序号)。
(3)用电子式表示①的形成过程是______________________ ,用电子式表示⑥的形成过程是_______________________ ,⑤的电子式是__________________ 。
(1)熔化时不需要破坏化学键的是
(2)属于离子化合物的是
(3)用电子式表示①的形成过程是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在HF、H2S、PH3、CS2、CCl4、H2O2、N2分子中:(将所选的物质化学式填入空白)
(1)以非极性键结合的非极性分子是_______
(2)以极性键相结合,具有直线型结构的非极性分子是_______
(3)以极性键相结合,具有正四面体结构的非极性分子是_______
(4)以极性键相结合,具有三角锥型结构的极性分子是______
(5)以极性键相结合,具有V型结构的极性分子是_______
(6)以极性键相结合,而且分子极性最大的是_______
(7)与N2O互为等电子体的是_________
(8)含有非极性键的极性分子是________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,具有三角锥型结构的极性分子是
(5)以极性键相结合,具有V型结构的极性分子是
(6)以极性键相结合,而且分子极性最大的是
(7)与N2O互为等电子体的是
(8)含有非极性键的极性分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)现有以下物质:①NaOH固体②盐酸③CaCO3固体④熔融 KCl⑤蔗糖⑥铜⑦NH3⑧液态的HCl,以上物质中能导电的是___________ ;(填序号,下同);以上物质中属于非电解质的是___________ 。
(2)现有以下物质:
①氩气 ②NaOH③AlCl3④BaCl2 ⑤硫酸 ⑥NH3 ⑦CCl4 ⑧H2O2,
a.以上物质中只含离子键的物质是___________ (填序号,下同);含非极性键的物质是___________ ;含有共价键的离子化合物是___________ ;
b.用电子式表示⑧的形成过程___________ 。
(1)现有以下物质:①NaOH固体②盐酸③CaCO3固体④熔融 KCl⑤蔗糖⑥铜⑦NH3⑧液态的HCl,以上物质中能导电的是
(2)现有以下物质:
①氩气 ②NaOH③AlCl3④BaCl2 ⑤硫酸 ⑥NH3 ⑦CCl4 ⑧H2O2,
a.以上物质中只含离子键的物质是
b.用电子式表示⑧的形成过程
您最近一年使用:0次