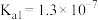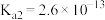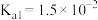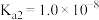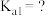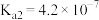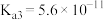已知25℃时有关弱酸的电离平衡常数如表。
(1)已知常温下,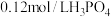 溶液pH=1.7,则磷酸的
溶液pH=1.7,则磷酸的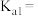
_______ (已知 )
)
(2)等体积等浓度的 和NaCN溶液中的离子总数大小关系为:
和NaCN溶液中的离子总数大小关系为:
_______ NaCN(填“大于”,“小于”或“等于”)
(3)向 溶液中通入过量
溶液中通入过量 的离子反应方程式为
的离子反应方程式为_____________________
(4)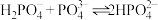 的平衡常数K=
的平衡常数K=______________ (填数值)
(5)将 通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:
通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:_____________________
弱酸 | HCN |
|
|
|
|
电离平衡常数 |
|
|
|
|
|
(1)已知常温下,
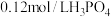 溶液pH=1.7,则磷酸的
溶液pH=1.7,则磷酸的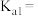
 )
)(2)等体积等浓度的
 和NaCN溶液中的离子总数大小关系为:
和NaCN溶液中的离子总数大小关系为:
(3)向
 溶液中通入过量
溶液中通入过量 的离子反应方程式为
的离子反应方程式为(4)
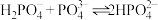 的平衡常数K=
的平衡常数K=(5)将
 通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:
通入1L1.5mol/LNaOH溶液中充分反应,所得溶液离子浓度大小的关系为:
更新时间:2022-11-27 12:12:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如何除去氯化亚铁中的氯化铁,写出其化学方程式____________ ,其反应的离子方程式是_____________ .
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。下图为氯元素的单质及其化合物的“价~类”二维图。请回答下列问题:

(1)二维图中X的化学式(分子式)为_______ 。
(2)“84”消毒液(有效成分为NaClO)进行环境消毒时,会与空气中的CO2发生反应生成NaHCO3与次氯酸。写出该反应的离子方程式_______ 。
(3)舍勒是最早制取Cl2的化学家,请你写出舍勒制取Cl2的离子方程式_______ ,实验室对Cl2进行尾气处理的离子方程式为_______ 。
(4)二氧化氯(ClO2)是一种新型自来水消毒剂。工业上一种制备ClO2的反应原理为2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O,该反应中H2O2作_______ (填“氧化剂”或“还原剂”)。

(1)二维图中X的化学式(分子式)为
(2)“84”消毒液(有效成分为NaClO)进行环境消毒时,会与空气中的CO2发生反应生成NaHCO3与次氯酸。写出该反应的离子方程式
(3)舍勒是最早制取Cl2的化学家,请你写出舍勒制取Cl2的离子方程式
(4)二氧化氯(ClO2)是一种新型自来水消毒剂。工业上一种制备ClO2的反应原理为2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O,该反应中H2O2作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有以下物质:①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥亚硫酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩氯化氢气体。
(1)其中能导电的是____________ ;属于电解质的是______________
(2)写出物质⑥溶于水的电离方程式:_____________ 。
(3)将物质⑥配制成溶液,逐滴加入⑦溶液至沉淀量最大,写出该反应的离子方程式:_________ 。
(1)其中能导电的是
(2)写出物质⑥溶于水的电离方程式:
(3)将物质⑥配制成溶液,逐滴加入⑦溶液至沉淀量最大,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】常温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
(1)HA为___________ (填“强酸”、“弱酸”或“无法确定”)
(2)x___________ 0.2(填:“<”、“=”、“>”)
(3)实验②反应后的溶液中离子浓度由大到小的顺序为___________
(4)实验①反应后的溶液中c(K+)___________ c(A-)+c(HA) (填:“<”、“=”、“>”)
(5)0.2 mol∙L−1的HA和0.1 mol∙L−1的KOH等体积混合充分反应后所得的溶液中c(HA)___________ c(A-) (填:“<”、“=”、“>”)
| 实验编号 | 起始浓度/ mol∙L−1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
(1)HA为
(2)x
(3)实验②反应后的溶液中离子浓度由大到小的顺序为
(4)实验①反应后的溶液中c(K+)
(5)0.2 mol∙L−1的HA和0.1 mol∙L−1的KOH等体积混合充分反应后所得的溶液中c(HA)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
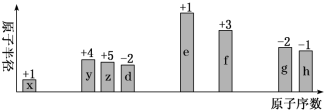
根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
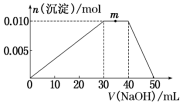
(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________ 。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是
(2)写出m点反应的离子方程式:
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在常温下,下列五种溶液:①0.1mol/LNH4Cl②0.l mol/L CH3COONH4 ③0.1mol/L NH4HSO4 ④0.1mol/L NH3·H2O和0.1mol/L NH4Cl混合液 ⑤0.lmol/L NH3·H2O。请根据要求填写下列空白:
(1)溶液①呈酸性,其原因是_______ (用离子方程式表示)。
(2)在上述五种溶液中,pH最小的是_______ ;c )最小的是
)最小的是_______ (填序号)。
(3)比较溶液②、③中c( )的大小关系是②
)的大小关系是②_______ ③(填“>”、“<”或“=”)。
(4)已知,常温下,0.1mol/LCH3COOH溶液的Ka与0.1mol/L NH3·H2O溶液的Kb相等,请写出②中离子浓度由大到小的顺序:_______ 。
(1)溶液①呈酸性,其原因是
(2)在上述五种溶液中,pH最小的是
 )最小的是
)最小的是(3)比较溶液②、③中c(
 )的大小关系是②
)的大小关系是②(4)已知,常温下,0.1mol/LCH3COOH溶液的Ka与0.1mol/L NH3·H2O溶液的Kb相等,请写出②中离子浓度由大到小的顺序:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知醋酸、盐酸和碳酸钠是生活中常见的物质。
(1)碳酸钠水溶液显碱性的原因是(用离子方程式表示)______________________________
(2)25 ℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是_________________ ;
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(3)25 ℃时,有pH 均等于4的醋酸溶液和氯化铵溶液,醋酸中水电离出的H+浓度与氯化铵溶液中水电离出的H+浓度之比是________________
(4)25 ℃时,向体积为Va mLpH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与的Vb关系是Va__________ Vb(填“>”、“<”或“=”)。
(5)醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,下列叙述不正确的是
CH3COO-+H+,下列叙述不正确的是_____
a.CH3COOH溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO‾)
b.0.1 mol / L 的CH3COOH 溶液加水稀释,溶液中c(OHˉ)减小
c.CH3COOH溶液中加入少量CH3COONa固体.平衡逆向移动
d.常温下,pH=2的CH3COOH溶液与pH=12的NaOH 溶液等体积混合后溶液的pH <7
e.室温下向pH=3的醋酸溶液中加水稀释,溶液中 不变
不变
(1)碳酸钠水溶液显碱性的原因是(用离子方程式表示)
(2)25 ℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(3)25 ℃时,有pH 均等于4的醋酸溶液和氯化铵溶液,醋酸中水电离出的H+浓度与氯化铵溶液中水电离出的H+浓度之比是
(4)25 ℃时,向体积为Va mLpH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与的Vb关系是Va
(5)醋酸溶液中存在电离平衡:CH3COOH
 CH3COO-+H+,下列叙述不正确的是
CH3COO-+H+,下列叙述不正确的是a.CH3COOH溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO‾)
b.0.1 mol / L 的CH3COOH 溶液加水稀释,溶液中c(OHˉ)减小
c.CH3COOH溶液中加入少量CH3COONa固体.平衡逆向移动
d.常温下,pH=2的CH3COOH溶液与pH=12的NaOH 溶液等体积混合后溶液的pH <7
e.室温下向pH=3的醋酸溶液中加水稀释,溶液中
 不变
不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
①0.1 mol/L Na2CO3溶液的pH____________ 0.1 mol/L Na2C2O4溶液的pH。(选填“大于”“小于”或“等于”)
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____ 。(选填编号)
A.[H+]>[ ]>[
]>[ ]>[
]>[ ] B.[
] B.[ ]>[
]>[ ]>[
]>[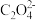 ]>[
]>[ ]
]
C.[H+]>[ ]>[
]>[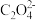 ]>[
]>[ ] D.[H2CO3] >[
] D.[H2CO3] >[ ]>[
]>[ ]>[
]>[ ]
]
(2)白磷与氧气可发生如下反应:P4+5O2= P4O10。已知断裂下列化学键需要吸收的能量分别为: P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH=___________ 。

(3)25 ℃,某浓度的盐酸、氯化铵溶液中由水电离出的氢离子浓度分别为1.0×10-amol·L-1、1.0×10-b mol·L-1,这两种溶液的pH之和=___________ 。
(4)在t ℃时,某Ba(OH)2的稀溶液中c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示:
假设溶液混合前后的体积变化忽略不计,则c=___________ 。
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
①0.1 mol/L Na2CO3溶液的pH
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是
A.[H+]>[
 ]>[
]>[ ]>[
]>[ ] B.[
] B.[ ]>[
]>[ ]>[
]>[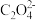 ]>[
]>[ ]
]C.[H+]>[
 ]>[
]>[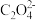 ]>[
]>[ ] D.[H2CO3] >[
] D.[H2CO3] >[ ]>[
]>[ ]>[
]>[ ]
] (2)白磷与氧气可发生如下反应:P4+5O2= P4O10。已知断裂下列化学键需要吸收的能量分别为: P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH=

(3)25 ℃,某浓度的盐酸、氯化铵溶液中由水电离出的氢离子浓度分别为1.0×10-amol·L-1、1.0×10-b mol·L-1,这两种溶液的pH之和=
(4)在t ℃时,某Ba(OH)2的稀溶液中c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 | 氢氧化钡溶液 的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在含有弱电解质的溶液中,往往有多个平衡共存。
(1)常温下,将 的某一元酸
的某一元酸 溶液和
溶液和 的
的 溶液等体积混合后溶液的
溶液等体积混合后溶液的 大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是
大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是___________ (填字母)。
A.
B.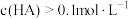
C.
(2)常温下,向 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳元素的各种微粒(
溶液,溶液中含碳元素的各种微粒( 因逸出未画出)的物质的量分数(纵轴)随溶液的
因逸出未画出)的物质的量分数(纵轴)随溶液的 变化的部分情况如图所示。
变化的部分情况如图所示。

①在同一溶液中,
___________ (填“能”或“不能”)大量共存。
②当 时,溶液中
时,溶液中
___________ (填“>”、“<”或“=”)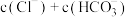 。
。
③ 时,
时, 水解反应的平衡常数
水解反应的平衡常数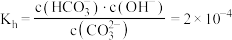 ,当溶液中
,当溶液中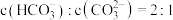 时,溶液的
时,溶液的
___________ 。
(3) 虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比
虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。
① 在溶液中分三步水解:
在溶液中分三步水解:


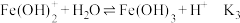
上述水解反应的平衡常数 由大到小的顺序是
由大到小的顺序是___________ 。
②通过控制条件,上述水獬产物聚合,生成聚合氯化铁,其离子方程式为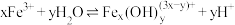 ,欲使平衡正向移动可采用的措施是
,欲使平衡正向移动可采用的措施是___________ (填字母)。
a.加水稀释 b.降温 c.加入
(1)常温下,将
 的某一元酸
的某一元酸 溶液和
溶液和 的
的 溶液等体积混合后溶液的
溶液等体积混合后溶液的 大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是
大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是A.

B.
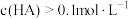
C.

(2)常温下,向
 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳元素的各种微粒(
溶液,溶液中含碳元素的各种微粒( 因逸出未画出)的物质的量分数(纵轴)随溶液的
因逸出未画出)的物质的量分数(纵轴)随溶液的 变化的部分情况如图所示。
变化的部分情况如图所示。
①在同一溶液中,

②当
 时,溶液中
时,溶液中
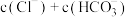 。
。③
 时,
时, 水解反应的平衡常数
水解反应的平衡常数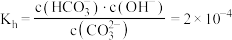 ,当溶液中
,当溶液中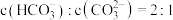 时,溶液的
时,溶液的
(3)
 虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比
虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。①
 在溶液中分三步水解:
在溶液中分三步水解:

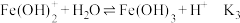
上述水解反应的平衡常数
 由大到小的顺序是
由大到小的顺序是②通过控制条件,上述水獬产物聚合,生成聚合氯化铁,其离子方程式为
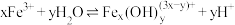 ,欲使平衡正向移动可采用的措施是
,欲使平衡正向移动可采用的措施是a.加水稀释 b.降温 c.加入

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】研究弱电解质的电离,有重要的实际意义。
下表是不同温度下水的离子积常数:
试回答以下问题:
(1)若25℃<t1<t2,则KW_______ 1×10﹣14(填“>”、“<”或“=”),判断的理由是_______ 。
(2)若25℃时,pH=3的盐酸和pH=11的氢氧化钠溶液等体积混合后溶液呈_______ 性(填“酸”、“中”或“碱”),溶液中c(Na+)_______ c(Cl﹣)(填“>”、“=”或“<”)。
(3)醋酸是一种常见的有机酸。醋酸的电离方程式为_______ 。
保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是_______ 。
A.c(CH3COO-) B.c(H+)
C.c(OH-) D.CH3COOH电离平衡常数
(4)向0.1 mol·L-1CH3COOH溶液中加水稀释,c(CH3COO-) / c(CH3COOH)的比值将_______ (填“变大”、“不变”或“变小”)。
(5)下列事实一定能说明CH3COOH是弱电解质的是_______ (填字母)。
A.相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B.1 mol·L-1 CH3COOH溶液能使紫色石蕊试液变红
C.25℃时,1 mol·L-1 CH3COOH溶液的pH约为2
D.10 mL 1mol·L-1的CH3COOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
E.相同物质的量浓度的CH3COOH和HCl溶液中,水的电离程度的大小关系为a大于b
(6)某些弱酸的电离常数如下:
下列反应可以发生的是_______(填字母)。
下表是不同温度下水的离子积常数:
温度/℃ | 25 | t1 | t2 |
水的离子积常数 | 1×10﹣14 | KW | 1×10﹣12 |
(1)若25℃<t1<t2,则KW
(2)若25℃时,pH=3的盐酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)醋酸是一种常见的有机酸。醋酸的电离方程式为
保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是
A.c(CH3COO-) B.c(H+)
C.c(OH-) D.CH3COOH电离平衡常数
(4)向0.1 mol·L-1CH3COOH溶液中加水稀释,c(CH3COO-) / c(CH3COOH)的比值将
(5)下列事实一定能说明CH3COOH是弱电解质的是
A.相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B.1 mol·L-1 CH3COOH溶液能使紫色石蕊试液变红
C.25℃时,1 mol·L-1 CH3COOH溶液的pH约为2
D.10 mL 1mol·L-1的CH3COOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
E.相同物质的量浓度的CH3COOH和HCl溶液中,水的电离程度的大小关系为a大于b
(6)某些弱酸的电离常数如下:
| 化学式 | CH3COOH | HSCN | HCN | HClO | H2CO3 |
| 电 离 常 数 | 1.8×10-5 | 1.3×10-1 | 4.9×10-10 | 3.0×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
| A.CH3COOH+Na2CO3=NaHCO3+CH3COONa |
| B.CH3COOH+NaCN=CH3COONa+HCN |
| C.CO2+H2O+2NaClO=Na2CO3+2HClO |
| D.NaHCO3+HCN=NaCN+H2O+CO2↑ |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是25℃时某些弱酸的电离常数,其中多元弱酸分步电离。
(1)根据表中数据判断下述反应可以发生的是__ (填编号)。
①NaF+CH3COOH=CH3COONa+HF
②HF+NaHCO3=NaF+H2O+CO2↑
③CH3COOH+K2C2O4=CH3COOK+KHC2O4
(2)少量CO2通入NaClO溶液中发生反应的离子方程式为__ 。
(3)常温下在20mL0.1mol/LNa2CO3溶液中逐滴滴加40mL0.1mol/L盐酸溶液,溶液中含碳元素的三种微粒H2CO3、HCO 、CO
、CO (CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。

问答下列问题:
①各字母代表的粒子为b__ ,c___ 。
②在同一溶液中,H2CO3、HCO 、CO
、CO (填“能“或“不能”)
(填“能“或“不能”)___ 大量共存。
| 弱酸 | K | 弱酸 | K |
| HF | 3.52×10-4 | H2CO3 | K1=4.4×10-7 |
| HClO | 2.95×10-8 | K2=4.7×10-11 | |
| HCOOH | 1.765×10-4 | H2C2O4 | K1=5.4×10-2 |
| CH3COOH | 1.753×10-5 | K2=5.4×10-5 |
①NaF+CH3COOH=CH3COONa+HF
②HF+NaHCO3=NaF+H2O+CO2↑
③CH3COOH+K2C2O4=CH3COOK+KHC2O4
(2)少量CO2通入NaClO溶液中发生反应的离子方程式为
(3)常温下在20mL0.1mol/LNa2CO3溶液中逐滴滴加40mL0.1mol/L盐酸溶液,溶液中含碳元素的三种微粒H2CO3、HCO
 、CO
、CO (CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
问答下列问题:
①各字母代表的粒子为b
②在同一溶液中,H2CO3、HCO
 、CO
、CO (填“能“或“不能”)
(填“能“或“不能”)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如表是几种常见弱酸的电离平衡常数(25℃),回答下列各题:
结合表中给出的电离常数回答下列问题:
(1)上述四种酸中,酸性最弱的是___________。
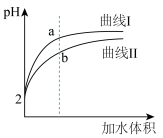
(2)将pH和体积均相同的 溶液和
溶液和 溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是
溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是___________ 的pH变化情况,
(3)下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的操作是
的电离程度增大,而电离平衡常数不变的操作是___________ (填序号)。
A.升高温度 B.加水稀释 C.加少量的 固体 D.加少量冰醋酸 E.加氢氧化钠固体
固体 D.加少量冰醋酸 E.加氢氧化钠固体
(4)依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式___________ 。
(5)室温下,测得10mL 醋酸(
醋酸( )溶液的电离度约为1%。完成下列填空:
)溶液的电离度约为1%。完成下列填空:
①上述醋酸溶液的pH=___________ 。
②加水稀释上述醋酸溶液,相对于原溶液,此时
___________ 。
A.不断减小 B.不断增大 C.无明显变化
(6)已知醋酸的酸性强于碳酸,请问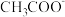 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是___________ 。
(7)某些共价化合物(如 、
、 、
、 等)在液态时会发生微弱的电离,如:
等)在液态时会发生微弱的电离,如: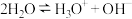 ,则液态
,则液态 的电离方程式为
的电离方程式为___________ 。
(8)现有浓度均为 的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的
的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是___________ (用序号表示)。
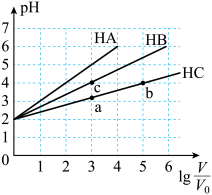
(9)常温下,pH均为2、体积均为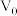 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随
的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随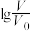 的变化关系如图所示,下列叙述错误的是___________。
的变化关系如图所示,下列叙述错误的是___________。
| 酸 |  |  | HCN | HClO |
| 电离平衡常数 |  |  | 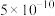 |  |
(1)上述四种酸中,酸性最弱的是___________。
A. | B. | C.HCN | D.HClO |
(2)将pH和体积均相同的
 溶液和
溶液和 溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是
溶液分别稀释,其pH随加水体积的变化如图所示,曲线Ⅰ是
(3)下列能使醋酸溶液中
 的电离程度增大,而电离平衡常数不变的操作是
的电离程度增大,而电离平衡常数不变的操作是A.升高温度 B.加水稀释 C.加少量的
 固体 D.加少量冰醋酸 E.加氢氧化钠固体
固体 D.加少量冰醋酸 E.加氢氧化钠固体(4)依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式
(5)室温下,测得10mL
 醋酸(
醋酸( )溶液的电离度约为1%。完成下列填空:
)溶液的电离度约为1%。完成下列填空:①上述醋酸溶液的pH=
②加水稀释上述醋酸溶液,相对于原溶液,此时

A.不断减小 B.不断增大 C.无明显变化
(6)已知醋酸的酸性强于碳酸,请问
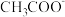 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是(7)某些共价化合物(如
 、
、 、
、 等)在液态时会发生微弱的电离,如:
等)在液态时会发生微弱的电离,如: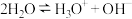 ,则液态
,则液态 的电离方程式为
的电离方程式为(8)现有浓度均为
 的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的
的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是(9)常温下,pH均为2、体积均为
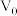 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随
的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随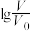 的变化关系如图所示,下列叙述错误的是___________。
的变化关系如图所示,下列叙述错误的是___________。
A.常温下: |
| B.HC的电离程度,a点<b点 |
C.当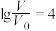 时,三种溶液同时升高温度, 时,三种溶液同时升高温度,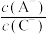 减小 减小 |
| D.a点酸的总浓度小于b点酸的总浓度 |
您最近一年使用:0次