(1)等物质的量的钠、镁、铝分别与足量盐酸反应,产生的氢气在相同条件下的体积比为______________ 。
(2)等质量的钠、镁、铝分别与足量盐酸反应,产生的氢气在相同条件下的体积比为________________ 。
(3)分别将0.2mol的钠、镁、铝分别投入100ml 1mol·L-1的盐酸溶液中,三者产生的氢气在相同条件下的体积比为____________________ 。
(2)等质量的钠、镁、铝分别与足量盐酸反应,产生的氢气在相同条件下的体积比为
(3)分别将0.2mol的钠、镁、铝分别投入100ml 1mol·L-1的盐酸溶液中,三者产生的氢气在相同条件下的体积比为
更新时间:2017-08-24 19:46:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】通过计算,回答下列问题:
(1)标况下 分子中所含原子数与
分子中所含原子数与______ 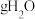 分子中所含原子数相等。
分子中所含原子数相等。
(2)一定条件下, 和
和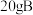 恰好完全反应生成
恰好完全反应生成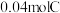 和
和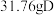 ,则C的摩尔质量为
,则C的摩尔质量为______ 。
(3)等质量的 和
和 中所含有的电子数之比为
中所含有的电子数之比为______ 。
(4)标准状况下, 与足量
与足量 反应转移的电子数为
反应转移的电子数为______ 。
(1)标况下
 分子中所含原子数与
分子中所含原子数与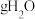 分子中所含原子数相等。
分子中所含原子数相等。(2)一定条件下,
 和
和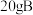 恰好完全反应生成
恰好完全反应生成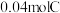 和
和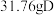 ,则C的摩尔质量为
,则C的摩尔质量为(3)等质量的
 和
和 中所含有的电子数之比为
中所含有的电子数之比为(4)标准状况下,
 与足量
与足量 反应转移的电子数为
反应转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】以NO和NO2为主的氮氧化物是造成光化学烟雾、雾霾和酸雨的一个重要原因。
I.为防止氮的氧化物(NO、NO2)污染空气,可用活性炭或一氧化碳还原氮氧化物。
(1)在一定条件下,CO与NO反应生成CO2和N2,反应的化学方程式: 。为提高此反应的速率,下列措施不可行的是___________(填标号)。
。为提高此反应的速率,下列措施不可行的是___________(填标号)。
(2)恒温条件下,向2L恒容密闭容器中加入活性炭(足量)和1.0molNO,发生反应: 。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=
。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=___________ mol·L-1·min-1。
II.氨气在一定条件下也可以还原氮氧化物,其反应为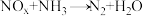 (未配平)。
(未配平)。
(3)下列有关NH3的说法中,错误的是___________ (填标号)。
A.工业合成NH3需要在高温、高压、催化剂下进行
B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥
(4)硝酸工业排放的废气中常含有NO、NO2等,为消除它们对环境的破坏作用,工业上可采用氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ ;若用通式NOx表示氮氧化物,则每摩尔氨可将___________ mol的NOx转化为N2。
III.工业上也常用Na2CO3溶液吸收法处理氮氧化物(NOX)。
已知:①NO不能与Na2CO3溶液反应。
② ;
;
(5)①当NOx被Na2CO3溶液完全吸收时,x的值不可能是___________ (填标号)。
A.1.3 B.1.6 C.1.8 D.2.0
②若用溶质质量分数为21.2%的Na2CO3溶液完全吸收1molNOx,则需要Na2CO3溶液至少______ g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液的质量就增加44g,则NOx中的x值为___________ 。
(6)氨转化法和Na2CO3溶液吸收法处理NOx尾气共同的优点是___________ 。
I.为防止氮的氧化物(NO、NO2)污染空气,可用活性炭或一氧化碳还原氮氧化物。
(1)在一定条件下,CO与NO反应生成CO2和N2,反应的化学方程式:
 。为提高此反应的速率,下列措施不可行的是___________(填标号)。
。为提高此反应的速率,下列措施不可行的是___________(填标号)。| A.及时转移出CO2 |
| B.使用合适的催化剂 |
| C.升高温度 |
| D.恒温恒容条件下,通入稀有气体增大压强 |
 。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=
。反应至5min时,实验测得CO2的物质的量为0.21mol,则0~5min内,以NO表示的反应速率υ(NO)=II.氨气在一定条件下也可以还原氮氧化物,其反应为
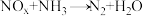 (未配平)。
(未配平)。(3)下列有关NH3的说法中,错误的是
A.工业合成NH3需要在高温、高压、催化剂下进行
B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥
(4)硝酸工业排放的废气中常含有NO、NO2等,为消除它们对环境的破坏作用,工业上可采用氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
III.工业上也常用Na2CO3溶液吸收法处理氮氧化物(NOX)。
已知:①NO不能与Na2CO3溶液反应。
②
 ;
;
(5)①当NOx被Na2CO3溶液完全吸收时,x的值不可能是
A.1.3 B.1.6 C.1.8 D.2.0
②若用溶质质量分数为21.2%的Na2CO3溶液完全吸收1molNOx,则需要Na2CO3溶液至少
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液的质量就增加44g,则NOx中的x值为
(6)氨转化法和Na2CO3溶液吸收法处理NOx尾气共同的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空
(1)写出下列物质的电子式:
①KCl___________ ②MgCl2 ___________ ③Cl2___________
④N2___________ ⑤H2O___________ ⑥CH4___________
(2)写出下列反应的化学方程式。
①锂在空气中燃烧:___________ ;
②钾与水反应:___________ ;
③溴与碘化钾反应:___________ ;
④氯化亚铁与氯气反应:___________ ;
(1)写出下列物质的电子式:
①KCl
④N2
(2)写出下列反应的化学方程式。
①锂在空气中燃烧:
②钾与水反应:
③溴与碘化钾反应:
④氯化亚铁与氯气反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成溶液C,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D.
⑴写出下列物质的化学式:B______ E______ D______
⑵写出A→C的化学方程式,并标出电子转移的方向和数目:__________ 。
⑶写出C→D的离子方程式:_______________
⑷写出化学方程式:E+B D+C+O2↑:
D+C+O2↑:_____________ .
⑴写出下列物质的化学式:B
⑵写出A→C的化学方程式,并标出电子转移的方向和数目:
⑶写出C→D的离子方程式:
⑷写出化学方程式:E+B
 D+C+O2↑:
D+C+O2↑:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是2NaCl(熔融) 2Na+Cl2↑。回答下列问题:
2Na+Cl2↑。回答下列问题:
(1)保存金属钠的正确方法是___________(填字母)。
(2)Na、NaOH久置在空气中最终都是变为___________ (填化学式)。
(3)将一小块金属钠投入CuCl2溶液中,发生反应的化学方程式为_______________ 。
Ⅱ. 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。
(4) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与CO2反应的化学方程式
与CO2反应的化学方程式___________ 。
(5)将一定量的 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有___________ (填离子符号)。
(6)查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
①已知 能发生如下反应:
能发生如下反应: ,上述反应中氧化产物是
,上述反应中氧化产物是___________ ;HI在反应中体现了什么性质___________ 。
②根据上述反应鉴别 和NaCl,可选择以下物质中的
和NaCl,可选择以下物质中的___________ 进行实验(填序号)。
A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.白酒
 2Na+Cl2↑。回答下列问题:
2Na+Cl2↑。回答下列问题:(1)保存金属钠的正确方法是___________(填字母)。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
(3)将一小块金属钠投入CuCl2溶液中,发生反应的化学方程式为
Ⅱ.
 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。(4)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与CO2反应的化学方程式
与CO2反应的化学方程式(5)将一定量的
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有(6)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:①已知
 能发生如下反应:
能发生如下反应: ,上述反应中氧化产物是
,上述反应中氧化产物是②根据上述反应鉴别
 和NaCl,可选择以下物质中的
和NaCl,可选择以下物质中的A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.白酒
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1) 绿矾的化学式是________ 。
(2) 热稳定性H2O大于H2S的主要原因是________ 。
(3) 写出镁在二氧化碳中燃烧的化学反应方程式:_______ 。
(2) 热稳定性H2O大于H2S的主要原因是
(3) 写出镁在二氧化碳中燃烧的化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铈、钛、锌、锰虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,反应中CeO2作______ 剂。在加热条件下,CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是______ 。
(2)钛(Ti)被誉为“二十一世纪的金属”。
①在高温下,向金红石(主要成分TiO2)与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体。该反应的化学方程式是______ 。
②加热条件下,镁与TiCl4反应可得到钛,下列气体可以作为保护气的是______
A.O2 B. N2 C. CO2 D.Ar
(3)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。写出锌和氢氧化钠溶液反应的化学方程式______ 。
(4)锰及其化合物应用越来越广泛,MnO2是一种重要的无机功能材料。
①已知A~G各物质间的关系如图,其中B、D为气态单质。
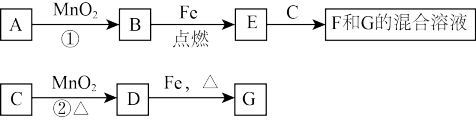
则反应②的离子方程式为______ 。
②E和C反应的化学方程式______ 。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,反应中CeO2作
(2)钛(Ti)被誉为“二十一世纪的金属”。
①在高温下,向金红石(主要成分TiO2)与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体。该反应的化学方程式是
②加热条件下,镁与TiCl4反应可得到钛,下列气体可以作为保护气的是
A.O2 B. N2 C. CO2 D.Ar
(3)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。写出锌和氢氧化钠溶液反应的化学方程式
(4)锰及其化合物应用越来越广泛,MnO2是一种重要的无机功能材料。
①已知A~G各物质间的关系如图,其中B、D为气态单质。

则反应②的离子方程式为
②E和C反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2013年H7N9禽流感肆虐期间为了保证卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。钠、镁及其化合物在工业中具有广泛的应用。回答下列问题:
(1)写出钠与水反应的化学方程式____________________
(2)写出镁与二氧化碳反应的化学方程式___________________
(3)漂白粉溶于水后,与空气中CO2发生反应,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________
(4)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质_________ (填序号)。
(1)写出钠与水反应的化学方程式
(2)写出镁与二氧化碳反应的化学方程式
(3)漂白粉溶于水后,与空气中CO2发生反应,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(4)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质
| A.酸性 | B.碱性 | C.漂白性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】阅读下列材料并填空。
2021年10月16日,搭载神舟十三号载人飞船的长征二号F遥十三运载火箭精准点火。神舟十三号载人飞船的成功发射离不开化学燃料。火箭分级推进中使用的燃料主要有①煤油、②液氢、③肼 和④固态铝粉,氧化剂主要有⑤液氧、⑥
和④固态铝粉,氧化剂主要有⑤液氧、⑥ 和⑦高氯酸铵
和⑦高氯酸铵 。
。
(1)上述材料涉及到的物质中,属于混合物的是_______ (填标号,下同);属于氧化物的是_______ ;属于单质的是_______ 。
(2)下列物质能与铝反应的是_______ (填标号)。
A.硝酸铜溶液B.稀硫酸C.氯气
(3)天宫课堂展示的泡腾片实验让我们感受到太空的奇妙。泡腾片含碳酸氢钠和固体酸,实验中将泡腾片放入蓝色水球,水球中产生许多气泡,气泡的主要成分是____ ,你推断的理由是____ 。
2021年10月16日,搭载神舟十三号载人飞船的长征二号F遥十三运载火箭精准点火。神舟十三号载人飞船的成功发射离不开化学燃料。火箭分级推进中使用的燃料主要有①煤油、②液氢、③肼
 和④固态铝粉,氧化剂主要有⑤液氧、⑥
和④固态铝粉,氧化剂主要有⑤液氧、⑥ 和⑦高氯酸铵
和⑦高氯酸铵 。
。(1)上述材料涉及到的物质中,属于混合物的是
(2)下列物质能与铝反应的是
A.硝酸铜溶液B.稀硫酸C.氯气
(3)天宫课堂展示的泡腾片实验让我们感受到太空的奇妙。泡腾片含碳酸氢钠和固体酸,实验中将泡腾片放入蓝色水球,水球中产生许多气泡,气泡的主要成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在标准状况下进行甲、乙、丙三组实验。三组实验均各取30mL同浓度的盐酸,加入同一种镁铝合金粉末,加入合金质量与产生气体有关数据见下表:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?______ (填“甲”或“乙”),理由是______________ 。
(2)要算出盐酸的物质的量浓度,题中可作为计算依据的数据是________ ,求得的盐酸的物质的量浓度为________ 。
(3)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是________ ,求得的Mg、Al物质的量之比为_____ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?
(2)要算出盐酸的物质的量浓度,题中可作为计算依据的数据是
(3)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求完成下列各小题:
(1)实验室中用铝和盐酸在常温条件下制备AlCl3其化学方程式为___________ 。工业上在高温条件下用碳氯化法制备AlCl3,其化学方程式Al2O3+xC+3Cl2 2AlCl3+3M,则M为
2AlCl3+3M,则M为___________ 。
(2)已知每100g葡萄糖中含碳元素40.00g、氢元素6.67g,其余为氧元素,试求葡萄糖中碳、氢、氧3种元素的原子个数之比___________ 。
(3)已知乙醇(C2H5OH)能与K2C2O4和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O, 和Cr3+和在溶液中分别显橙色和绿色,该反应
和Cr3+和在溶液中分别显橙色和绿色,该反应___________ (填“是”或“不是”)离子反应,写出Cr2(SO4)3的电离方程式___________ 。你认为能否用这一反应来检测司机是否酒驾___________ (填“能”或“不能“),简述其原理:___________ 。
(1)实验室中用铝和盐酸在常温条件下制备AlCl3其化学方程式为
 2AlCl3+3M,则M为
2AlCl3+3M,则M为(2)已知每100g葡萄糖中含碳元素40.00g、氢元素6.67g,其余为氧元素,试求葡萄糖中碳、氢、氧3种元素的原子个数之比
(3)已知乙醇(C2H5OH)能与K2C2O4和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,
 和Cr3+和在溶液中分别显橙色和绿色,该反应
和Cr3+和在溶液中分别显橙色和绿色,该反应
您最近一年使用:0次

 ,在一定量的氧气中恰好完全燃烧,反应的方程式为:
,在一定量的氧气中恰好完全燃烧,反应的方程式为: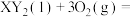
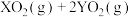 ,冷却后,在标准状况下测的生成物的体积是
,冷却后,在标准状况下测的生成物的体积是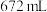 ,密度是
,密度是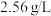 。求:
。求: 、
、 两种元素的质量比为
两种元素的质量比为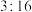 ,则
,则

