“化学一我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是____ ,胶体和溶液的本质区别是____ 。
(2)钠的焰色试验的焰色为____ 色,该色的光射程远,透雾力强,据此原理制作的高压钠灯广泛应用于道路和广场的照明。焰色试验属于____ (填“物理”或“化学”)变化。
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是____ ,原因是____ 。
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有____ (填化学式)。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)钠的焰色试验的焰色为
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有
更新时间:2022-03-23 19:27:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表
每组分类均有错误,其错误的物质分别是_______ 、_______ 、_______ (填化学式)。
(2)胶体和溶液的本质区别是_______ 。
(3)下列3个反应,按要求填写相关量。
①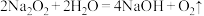 反应中,每生成1分子
反应中,每生成1分子 转移
转移_______ 个电子。
②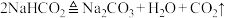 反应中,每消耗
反应中,每消耗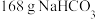 ,生成
,生成_______ 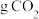 ;
;
③ 反应中,每消耗10分子
反应中,每消耗10分子 ,转移
,转移_______ 个电子。
(1)下列是某同学对有关物质进行分类的列表
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 |  |  |  |  |  |
| 第二组 |  |  |  |  |  |
| 第三组 |  |  |  |  |  |
每组分类均有错误,其错误的物质分别是
(2)胶体和溶液的本质区别是
(3)下列3个反应,按要求填写相关量。
①
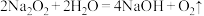 反应中,每生成1分子
反应中,每生成1分子 转移
转移②
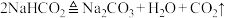 反应中,每消耗
反应中,每消耗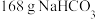 ,生成
,生成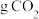 ;
;③
 反应中,每消耗10分子
反应中,每消耗10分子 ,转移
,转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】常用的干燥剂有:①生石灰;②氢氧化钠固体;③变色硅胶(主要成分是二氧化硅,在其中掺入少量的无水氯化钴作指示剂);④五氧化二磷;⑤无水氯化钙;⑥浓硫酸。
(1)上述物质中,属于纯净物的是_______(填字母,下同)。
(2)上述干燥剂中①,其主要化学成分所属的类别为_______ 。
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
(3)硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于_______ (填“物理变化”或“化学变化”)。
(4)为了能观察到丁达尔效应,某兴趣小组同学在实验室制备Fe(OH)3胶体。
①制备时,将5~6滴_______ 溶液逐滴加入到40mL煮沸的蒸馏水中,待液体呈_______ 色后停止加热。
②Fe(OH)3胶体与FeCl3溶液相比较,其本质区别是_______
A.颜色不同 B.Fe(OH)3胶体能产生丁达尔现象而FeCl3溶液不能
C.分散质粒子大小不同 D.Fe(OH)3胶体不透明而FeCl3溶液透明
(1)上述物质中,属于纯净物的是_______(填字母,下同)。
| A.①②④ | B.②④⑥ | C.①②④⑤ | D.全部 |
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
(3)硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于
(4)为了能观察到丁达尔效应,某兴趣小组同学在实验室制备Fe(OH)3胶体。
①制备时,将5~6滴
②Fe(OH)3胶体与FeCl3溶液相比较,其本质区别是
A.颜色不同 B.Fe(OH)3胶体能产生丁达尔现象而FeCl3溶液不能
C.分散质粒子大小不同 D.Fe(OH)3胶体不透明而FeCl3溶液透明
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断正误:
1.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂。_______
2.漂白粉可用于生活用水的消毒。_______
3.标准状况下,11.2LCl2与水充分反应转移电子数为0.5NA。_______
4.“84”消毒液的消毒原理与H2O2的相同,都是利用强氧化性。_______
5.漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3。_______
6.NaClO和Ca(ClO)2的溶液能杀菌消毒的原理是二者水解均呈碱性。_______
7.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合产生的HClO易分解。_______
1.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂。
2.漂白粉可用于生活用水的消毒。
3.标准状况下,11.2LCl2与水充分反应转移电子数为0.5NA。
4.“84”消毒液的消毒原理与H2O2的相同,都是利用强氧化性。
5.漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3。
6.NaClO和Ca(ClO)2的溶液能杀菌消毒的原理是二者水解均呈碱性。
7.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合产生的HClO易分解。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碱式次氯酸镁[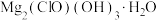 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
(1)工业上利用 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式_______ 。
(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是_______ ,阴极电极反应方程式为_______ 。
(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是_______ (用离子方程式表示)。
(4)碱式次氯酸镁( )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量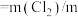 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为_______ 。
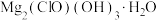 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:(1)工业上利用
 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、
 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是
(4)碱式次氯酸镁(
 )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量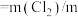 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:_________________________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:__________________________ 。
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:__________________________ 。
(2)海水开发利用的部分过程如图所示:
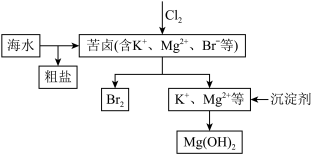
④向苦卤中通入氯气,发生反应的离子方程式是_____________________________________
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是______________________
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是_______ 。
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:
(2)海水开发利用的部分过程如图所示:

④向苦卤中通入氯气,发生反应的离子方程式是
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用
 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】前一段时间,各地报刊纷纷转载了不要将不同品牌洁污剂混合使用的警告。据报道,在全国各地发生了多起混合洁污剂发生氯气中毒的事件。发生反应的离子方程式是:ClO+Cl+2H+=Cl2↑+H2O。根据你所掌握的化学知识作出如下判断:当事人使用的液态洁污剂之一必定含氯,其中氯最可能的存在形式是_________ 和_______ (填离子),当另一种具有_______ (性质)的液态洁污剂与之混合,可能发生上述反应而产生氯气。举例说明这两种洁污剂的名称(家用洁污剂的商品名称)___________ 、____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】漂白粉的有效成分是______ ,制取漂白粉的反应方程式为______ ,漂白粉漂白和消毒的主要原因是:_______ (文字表述),漂白粉在空气中长时间放置失效的原因是:__________ (用化学方程式表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠具有很活泼的化学性质,易与很多物质反应。钠与水的反应(水中滴有酚酞溶液)实验现象和结论如下表,请同学们完成填空。
(5)钠与水反应方程式是__________________ 。实验室中金属钠通常保存在_______ 。
(6)实验室常用氢氧化钠溶液来吸收多余的氯气以防止污染空气,请写出发生反应的方程式_______________ 。漂白粉长时期露置在空气中会失效,用方程式表示其失效的原因_________________________ ;______________________ 。
| 实验现象 | 解释与结论 |
| (1) | 密度比水小 |
| (2)熔化成闪亮的小球 | |
| (3)四处游动、嘶嘶作响 | |
| (4)反应后溶液呈红色 |
(5)钠与水反应方程式是
(6)实验室常用氢氧化钠溶液来吸收多余的氯气以防止污染空气,请写出发生反应的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)生石灰可作食品干燥剂,它属于___________ (填“碱”、“盐”或“氧化物”)。
(2)将食品袋中的抗氧化剂还原铁粉投入食醋中,发现产生大量气泡,溶液变为浅绿色。请写出发生反应的离子方程式___________ 。
(3)洪涝灾害后,加入KAl(SO4)2·12H2O可使浑浊的水变澄清,该物质俗名为___________ ,因其溶于水生成___________ (化学式)而具有净水作用。
(4)铝粉和氢氧化钠混合物可用作下水道疏通剂,其主要原因为___________ (用化学方程式表示)。
(5)炒菜时,食盐不慎撒落在天然气火焰上,可能看到的现象为:___________ 。
(1)生石灰可作食品干燥剂,它属于
(2)将食品袋中的抗氧化剂还原铁粉投入食醋中,发现产生大量气泡,溶液变为浅绿色。请写出发生反应的离子方程式
(3)洪涝灾害后,加入KAl(SO4)2·12H2O可使浑浊的水变澄清,该物质俗名为
(4)铝粉和氢氧化钠混合物可用作下水道疏通剂,其主要原因为
(5)炒菜时,食盐不慎撒落在天然气火焰上,可能看到的现象为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】判断下列说法的正误,并说明原因:
| 说法 | 正误及解释或改正 | |
| 1 | 根据化合物的水溶液能否导电,将化合物分为电解质和非电解质 | |
| 2 | 硫酸电离:H2SO4=H +SO +SO | |
| 3 | 醋酸电离:CH3COOH=CH3COO-+H+ | |
| 4 | 碳酸氢钠电离:NaHCO3=Na++H++CO | |
| 5 | Cl2溶于水可以导电,所以Cl2是电解质 | |
| 6 | CaCO3难溶于水,所以CaCO3是非电解质 | |
| 7 | 硫酸是强酸,醋酸是弱酸,所以硫酸溶液的导电能力大于醋酸溶液 | |
| 8 | Na2O熔融状态可导电,所以Na2O为电解质 | |
| 9 | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| 10 | 用铂丝蘸取溶液进行焰色反应,火焰呈黄色,该溶液中可能含有K+ |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,
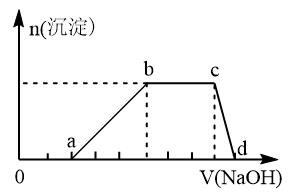
⑴该溶液中肯定含有的离子是_________________ ,且各离子的物质的量之比为____________ ;肯定不含的离子是_____________ 。
⑵还有一种离子可能存在,写出检验这种离子的实验方法及现象:_______________ 。

⑴该溶液中肯定含有的离子是
⑵还有一种离子可能存在,写出检验这种离子的实验方法及现象:
您最近一年使用:0次



