判断下列说法的正误,并说明原因:
| 说法 | 正误及解释或改正 | |
| 1 | 根据化合物的水溶液能否导电,将化合物分为电解质和非电解质 | |
| 2 | 硫酸电离:H2SO4=H +SO +SO | |
| 3 | 醋酸电离:CH3COOH=CH3COO-+H+ | |
| 4 | 碳酸氢钠电离:NaHCO3=Na++H++CO | |
| 5 | Cl2溶于水可以导电,所以Cl2是电解质 | |
| 6 | CaCO3难溶于水,所以CaCO3是非电解质 | |
| 7 | 硫酸是强酸,醋酸是弱酸,所以硫酸溶液的导电能力大于醋酸溶液 | |
| 8 | Na2O熔融状态可导电,所以Na2O为电解质 | |
| 9 | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| 10 | 用铂丝蘸取溶液进行焰色反应,火焰呈黄色,该溶液中可能含有K+ |
23-24高一上·全国·期中 查看更多[1]
(已下线)专题02 离子反应【考点清单】(讲+练)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)
更新时间:2023-10-16 15:17:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有以下几种物质:A.硝酸钾固体;B.稀盐酸;C.胆矾(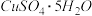 )晶体;D.熔融的
)晶体;D.熔融的 ;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:
;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:
(1)①以上物质中能导电的是_______ (填字母,下同)。
②以上物质中属于电解质的是_______ 。
③以上物质中属于氧化物的是_______ 。
④以上物质中属于混合物的是_______ 。
⑤以上物质中属于有机化合物的是_______ 。
(2)A溶于水的电离方程式为_______ ;
(3)B的水溶液与H反应的离子方程式为_______ 。
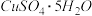 )晶体;D.熔融的
)晶体;D.熔融的 ;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:
;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:(1)①以上物质中能导电的是
②以上物质中属于电解质的是
③以上物质中属于氧化物的是
④以上物质中属于混合物的是
⑤以上物质中属于有机化合物的是
(2)A溶于水的电离方程式为
(3)B的水溶液与H反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈_________ 色,停止加热,可制得Fe(OH)3胶体。若向制得的胶体中加入过量稀硫酸,反应的离子方程式为____________________ 。
(2)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦蔗糖 ⑧熔化的NaCl,其中能导电的物质有________________ (填序号),属于电解质的有____________ (填序号)。
(3)①标准状况下,11.2L NH3中含_____________ 个氨分子。
②12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为_____________ g/mol。
③10mL 3mol/L稀硫酸加水稀释到200mL,稀释后c(H+)=_____________ 。
(2)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦蔗糖 ⑧熔化的NaCl,其中能导电的物质有
(3)①标准状况下,11.2L NH3中含
②12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为
③10mL 3mol/L稀硫酸加水稀释到200mL,稀释后c(H+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列十种物质:①熔融的氢氧化钠、②Al、③液态氯化氢、④稀硫酸、⑤ 、⑥
、⑥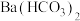 溶液、⑦
溶液、⑦ 固体、⑧乙醇、⑨
固体、⑧乙醇、⑨ 、⑩
、⑩ 胶体。
胶体。
(1)按物质的分类方法回答下列问题(填序号):属于非电解质的是___________ ,属于电解质的是___________ ,上述状态下的电解质不能导电的是___________ 。
(2)写出⑦在水溶液中的电离方程式___________ ,向 溶液中加入
溶液中加入 溶液,写出发生反应的离子方程式:
溶液,写出发生反应的离子方程式:___________ 。
(3)⑥与少量①的溶液反应的离子方程式___________ 。
(4)补全离子方程式:________
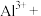 ___________
___________ ___________。
___________。
 、⑥
、⑥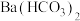 溶液、⑦
溶液、⑦ 固体、⑧乙醇、⑨
固体、⑧乙醇、⑨ 、⑩
、⑩ 胶体。
胶体。(1)按物质的分类方法回答下列问题(填序号):属于非电解质的是
(2)写出⑦在水溶液中的电离方程式
 溶液中加入
溶液中加入 溶液,写出发生反应的离子方程式:
溶液,写出发生反应的离子方程式:(3)⑥与少量①的溶液反应的离子方程式
(4)补全离子方程式:
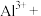 ___________
___________ ___________。
___________。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4∙5H2O晶体。请用序号填空:
(1)上述状态下可导电的是___________ 。
(2)属于电解质的是___________ 。
(3)属于非电解质的是___________ 。
(4)②在水溶液中的电离方程式为___________ ,①与②在溶液中反应呈中性的离子方程式为___________ 。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
Ⅰ.还原产物是___________ 。
Ⅱ.用单线桥法标出反应中电子转移的方向和数目___________ 。
(6)用双线桥法来表示电子的转移方向与数目:____________
Fe2O3+3CO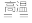 2Fe+3CO2。
2Fe+3CO2。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)②在水溶液中的电离方程式为
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
Ⅰ.还原产物是
Ⅱ.用单线桥法标出反应中电子转移的方向和数目
(6)用双线桥法来表示电子的转移方向与数目:
Fe2O3+3CO
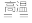 2Fe+3CO2。
2Fe+3CO2。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤Ba(OH)2,⑥氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4,⑨碳酸钙,⑩乙醇。
(1)上述物质中能导电的是___ ,属于电解质的有___ ,属于非电解质的有___ (填序号)。
(2)向⑥中逐滴滴加④的溶液,观察到的现象是___ ,发生反应的离子方程式为__ 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为___ 。
(4)⑧在水中的电离方程式为___ 。
(5)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O。用双线桥法标明上述反应方程式中电子转移的方向和数目___ 。
(1)上述物质中能导电的是
(2)向⑥中逐滴滴加④的溶液,观察到的现象是
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为
(4)⑧在水中的电离方程式为
(5)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O。用双线桥法标明上述反应方程式中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用2FeCl3+Cu=CuCl2+2X表示。
(1)上式中X的化学式为___________ 。
(2)在上述反应中,氧化剂为___________ ,氧化产物为 ___________ ,将两者的氧化性相比较,___________ 的氧化性更强。
(3)若有32g铜被氧化,则参与反应的FeCl3的质量为___________ g。
(4)该反应的离子方程式为___________ 。
(5)请写出反应物氯化铁的电离方程式___________ 。
(1)上式中X的化学式为
(2)在上述反应中,氧化剂为
(3)若有32g铜被氧化,则参与反应的FeCl3的质量为
(4)该反应的离子方程式为
(5)请写出反应物氯化铁的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D、的化学式:C_______ ,D______ 。
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:_______________ 。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为_____________________ 。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理______________________ 。
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为__________ g。
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 |    OH- OH- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D、的化学式:C
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:
(3)在A溶液中加入少量澄清石灰水,其离子方程式为
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】四个试剂瓶中分别盛有 溶液、
溶液、 溶液、
溶液、 溶液和
溶液和 溶液,就如何检验这四种溶液分别做如下探究。
溶液,就如何检验这四种溶液分别做如下探究。
探究过程:分别取四种溶液各 于四支试管中,做下列实验。
于四支试管中,做下列实验。
(1)在四支试管中分别滴入稀硝酸,依据___________ 现象能检测出的物质是___________ 其离子方程式为___________ 。
(2)在剩余三支试管中分别滴入 溶液,依据
溶液,依据___________ 现象能检测出的物质是___________ ,其离子方程式为___________ 。
(3)在剩余两支试管中分别滴入___________ 溶液,依据___________ 现象能检测出的物质是___________ ,离子方程式为___________ 。
 溶液、
溶液、 溶液、
溶液、 溶液和
溶液和 溶液,就如何检验这四种溶液分别做如下探究。
溶液,就如何检验这四种溶液分别做如下探究。探究过程:分别取四种溶液各
 于四支试管中,做下列实验。
于四支试管中,做下列实验。(1)在四支试管中分别滴入稀硝酸,依据
(2)在剩余三支试管中分别滴入
 溶液,依据
溶液,依据(3)在剩余两支试管中分别滴入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D四种易溶于水的白色固体,分别由 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A______ ;D______ 。
(2)写出下列反应的离子方程式:
①B+D→:______ ;
③C+HCl→气体:______ 。
(3)在作实验反思时,有同学提出:如果溶液中同时存在 和
和 ,
, 会对
会对 的检验产生干扰。为了确定该溶液中是否存在
的检验产生干扰。为了确定该溶液中是否存在 ,该小组同学进行了如下探究实验:
,该小组同学进行了如下探究实验:
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断盐的化学式分别为:A
(2)写出下列反应的离子方程式:
①B+D→:
③C+HCl→气体:
(3)在作实验反思时,有同学提出:如果溶液中同时存在
 和
和 ,
, 会对
会对 的检验产生干扰。为了确定该溶液中是否存在
的检验产生干扰。为了确定该溶液中是否存在 ,该小组同学进行了如下探究实验:
,该小组同学进行了如下探究实验:| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
| 第一步 | 向溶液中滴加过量的 溶液 溶液 | 除去 | 略 |
| 第二步 | 向第一步实验后的溶液中滴加 | 检验 | 略 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈__________ 色。
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是__________ 。
A. 1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______ 。
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点________ 。
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为_______ mL。
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________ ,其物质的量之比为________ 。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是
A. 1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中三次检验结果如下表所示,请回答下列问题。
(1)三次检验结果中第___________ 次检验结果不正确。
(2)检验时,为了确定溶液中是否存在 、
、 、
、 进行下列实验:
进行下列实验:
第一,向溶液中滴加___________ (填化学式)溶液,其目的是___________ ;
第二,继续加入过量的___________ (填化学式)溶液,其目的是___________ ;
第三:向溶液中滴加___________ (填化学式)溶液,其目的是___________ ;
第四:过滤,再向滤液中加入___________ (填化学式)溶液,其目的是___________ 。
(3)为了确定 的存在,写出
的存在,写出 鉴定的实验方法和现象:
鉴定的实验方法和现象:___________ 。
| 检验次数 | 溶液中检验出的物质 |
| 第一次 |  、 、 、 、 、 、 |
| 第二次 |  、 、 、 、 、 、 |
| 第三次 |  、 、 、 、 、 、 |
(2)检验时,为了确定溶液中是否存在
 、
、 、
、 进行下列实验:
进行下列实验:第一,向溶液中滴加
第二,继续加入过量的
第三:向溶液中滴加
第四:过滤,再向滤液中加入
(3)为了确定
 的存在,写出
的存在,写出 鉴定的实验方法和现象:
鉴定的实验方法和现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
(1)已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:___ 。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是__ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是___ (填序号)。
A.焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___ 。
| 药品 | NaNO2 (亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是
A.焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次



