氯及其化合物在生产、生活中有着广泛的用途
(1)次氯酸钠是最普通的家庭洗涤中的“氯”漂白剂和消毒剂。已知“84消毒液”的主要成分是次氯酸钠,在清洗卫生间时,若将“洁厕灵”与“84消毒液”混合使用会发生氯气中毒事件。请从氧化还原反应的角度分析原因:_______________________ 。
(2)漂白粉的有效成分是:______________ (填化学式),老师新买的漂白粉没有保存说明书,请你为漂白粉设计一份保存注意事项(不超过20个字):_____________ ,漂白粉久置后其成分除CaCl2外还含有______________ (填化学式),请你设计实验方案证明该固体粉末含Cl-离子:____________________________ 。
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下述离子方程式Fe(OH)3+ClO-+OH-→ +□:
+□:_____________________________ 。
(4)ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O
①请用双线桥表示反应中电子转移的方向和数目: 2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O:______________________ 。
②上述反应中,当生成1 mol ClO2分子时,转移电子的物质的量为:___________ mol。
③Cl2和ClO2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-,则ClO2和Cl2相同质量时,ClO2的消毒能力是Cl2的___________ 倍。
(5)ClO2在工业上的一种生产工艺如图所示:
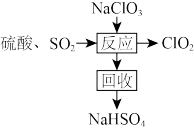
请写出“反应”步骤中生成CO2的化学方程式:________________ 。
(1)次氯酸钠是最普通的家庭洗涤中的“氯”漂白剂和消毒剂。已知“84消毒液”的主要成分是次氯酸钠,在清洗卫生间时,若将“洁厕灵”与“84消毒液”混合使用会发生氯气中毒事件。请从氧化还原反应的角度分析原因:
(2)漂白粉的有效成分是:
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下述离子方程式Fe(OH)3+ClO-+OH-→
 +□:
+□:(4)ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O
①请用双线桥表示反应中电子转移的方向和数目: 2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O:
②上述反应中,当生成1 mol ClO2分子时,转移电子的物质的量为:
③Cl2和ClO2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-,则ClO2和Cl2相同质量时,ClO2的消毒能力是Cl2的
(5)ClO2在工业上的一种生产工艺如图所示:

请写出“反应”步骤中生成CO2的化学方程式:
更新时间:2020-11-29 09:41:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___ (填字母)。

(2)利用氧化还原反应原理配平如下方程式:___
____NH3+____O2 ____NO+____H2O
____NO+____H2O
(3)用单线桥法标出如下反应的电子转移的方向和数目:___ 。
Cl2+SO2+2H2O=H2SO4+2HCl
(1)虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)利用氧化还原反应原理配平如下方程式:
____NH3+____O2
 ____NO+____H2O
____NO+____H2O(3)用单线桥法标出如下反应的电子转移的方向和数目:
Cl2+SO2+2H2O=H2SO4+2HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按指定要求完成下列问题。
(1)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被水还原的BrF3的物质的量是___ 。
(2)已知砒霜As2O3与Zn可发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目___ 。
②若生成0.2molAsH3,则转移的电子数为___ 。
(3)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有以下两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为___ 。
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两种方法中消耗的还原剂质量之比是___ 。
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为Cl-,则相同质量的ClO2是Cl2消毒效率的___ 倍(消毒效率:等质量两种物质所转移电子的物质的量之比)。
(1)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被水还原的BrF3的物质的量是
(2)已知砒霜As2O3与Zn可发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目
②若生成0.2molAsH3,则转移的电子数为
(3)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有以下两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两种方法中消耗的还原剂质量之比是
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为Cl-,则相同质量的ClO2是Cl2消毒效率的
您最近一年使用:0次
【推荐3】碘化钾和碘酸钾(KIO3)在食品工业中常用作营养增补剂(碘值强化剂),我国从1994年起在食盐中添加碘酸钾作为补碘剂。
(1)为检验某食盐中所加碘强化剂是碘化钾或碘酸钾,现进行分步实验:
已知:Ⅰ.氧化性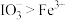 ;
;
Ⅱ.实验中可选用的试剂有:FeCl3溶液、FeSO4溶液、淀粉溶液
①补充完整检验食盐中是否含有I-的实验方案:取少量食盐,加水溶解,_______ 。
②补充完整检验食盐中是否含有 的实验方案:取少量食盐,加水溶解,
的实验方案:取少量食盐,加水溶解,_______ 。
(2)工业可用“氯酸钾氧化法”分两步制备KIO3,其中第一步反应方程式为: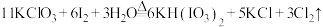
①用单线桥表示该反应电子转移的方向和数目:_______ 。
②每生成标准状况下11.2LCl2,反应转移电子的物质的量是_______ 。
③第二步反应时应向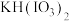 中加入的物质是
中加入的物质是_______ 。
(1)为检验某食盐中所加碘强化剂是碘化钾或碘酸钾,现进行分步实验:
已知:Ⅰ.氧化性
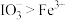 ;
;Ⅱ.实验中可选用的试剂有:FeCl3溶液、FeSO4溶液、淀粉溶液
①补充完整检验食盐中是否含有I-的实验方案:取少量食盐,加水溶解,
②补充完整检验食盐中是否含有
 的实验方案:取少量食盐,加水溶解,
的实验方案:取少量食盐,加水溶解,(2)工业可用“氯酸钾氧化法”分两步制备KIO3,其中第一步反应方程式为:
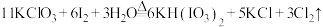
①用单线桥表示该反应电子转移的方向和数目:
②每生成标准状况下11.2LCl2,反应转移电子的物质的量是
③第二步反应时应向
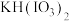 中加入的物质是
中加入的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氨基磺酸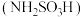 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
(1)由尿素 与发烟硫酸(用
与发烟硫酸(用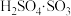 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为_______ 。
(2)氨基磺酸在高温时的分解反应为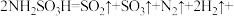
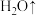 。
。
①检验该混合产物中含有 的试剂是
的试剂是_______ (填序号)。
A.品红溶液 B. 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液
②高温时,该反应中转移2mol电子时,生成气体的总物质的量是_______ mol。
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为_______ 。
②下列有关浓硫酸和浓硝酸的说法正确的是_______ (填序号)。
A.浓硫酸可用于干燥 、
、 、HI
、HI
B.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
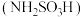 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。(1)由尿素
 与发烟硫酸(用
与发烟硫酸(用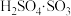 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为(2)氨基磺酸在高温时的分解反应为
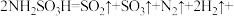
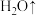 。
。①检验该混合产物中含有
 的试剂是
的试剂是A.品红溶液 B.
 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液②高温时,该反应中转移2mol电子时,生成气体的总物质的量是
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为
②下列有关浓硫酸和浓硝酸的说法正确的是
A.浓硫酸可用于干燥
 、
、 、HI
、HIB.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原反应是一类重要的化学反应,广泛存在于生产生活中。
(1)下列变化中,与氧化还原反应有关的是_______ (填字母)。
a.食物的腐败 b.钢铁的锈蚀 c.钟乳石的形成 d.燃料的燃烧
(2)汽车尾气中的CO和NO在催化剂作用下发生反应,生成CO2和N2。写出化学方程式:_______ 。
(3)FeSO4、K2FeO4是水处理中常用的物质。
①选择两种属于不同基本反应类型 的方法制取FeSO4,用离子方程式表示该方法:_______ 、_______ 。
②依据“性质决定用途”的学科观念,分析K2FeO4的性质,预测K2FeO4在处理含 的废水中的作用。简述分析过程:
的废水中的作用。简述分析过程:_______ 。
(1)下列变化中,与氧化还原反应有关的是
a.食物的腐败 b.钢铁的锈蚀 c.钟乳石的形成 d.燃料的燃烧
(2)汽车尾气中的CO和NO在催化剂作用下发生反应,生成CO2和N2。写出化学方程式:
(3)FeSO4、K2FeO4是水处理中常用的物质。
①选择两种属于
②依据“性质决定用途”的学科观念,分析K2FeO4的性质,预测K2FeO4在处理含
 的废水中的作用。简述分析过程:
的废水中的作用。简述分析过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列各题。
(1)按如图所示操作,充分反应后:
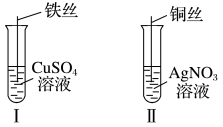
①Ⅰ中发生反应的离子方程式为_____ 。
②Ⅱ中铜丝上观察到现象是_____ 。
③结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_____ 。
(2)人体内的铁元素以 和
和 的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含
的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含 的亚铁盐,如硫酸亚铁。服用维生素
的亚铁盐,如硫酸亚铁。服用维生素 ,可使食物中的
,可使食物中的 还原成
还原成 ,有利于人体吸收。这句话说明维生素
,有利于人体吸收。这句话说明维生素 在这一反应中起的作用是
在这一反应中起的作用是_____ 。
(3)实验室可以用铜和稀硝酸反应制取 ,反应的化学方程式如下(未配平):
,反应的化学方程式如下(未配平):
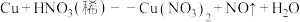
①写出配平后的上述化学方程式:_____ 。
②该反应中,被还原的硝酸与未被还原的硝酸质量比为_____ 。
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到现象是
③结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)人体内的铁元素以
 和
和 的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含
的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含 的亚铁盐,如硫酸亚铁。服用维生素
的亚铁盐,如硫酸亚铁。服用维生素 ,可使食物中的
,可使食物中的 还原成
还原成 ,有利于人体吸收。这句话说明维生素
,有利于人体吸收。这句话说明维生素 在这一反应中起的作用是
在这一反应中起的作用是(3)实验室可以用铜和稀硝酸反应制取
 ,反应的化学方程式如下(未配平):
,反应的化学方程式如下(未配平):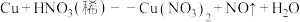
①写出配平后的上述化学方程式:
②该反应中,被还原的硝酸与未被还原的硝酸质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氯气和氯化氢在生产生活中有着重要的应用。回答下列问题:
(1)混在氯气中的HCl气体可用饱和食盐水除去。请设计一个简单实验证明产生的氯气中含有HCl__ 。
(2)氯气可以制得漂粉精和消毒水(有效成分为NaClO),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):__ 。将一瓶NaClO溶液(只含一种溶质),长时间放置在空气中,最终变为__ (填溶质的化学式)。
(3)在标准状态下,300体积的氯化氢溶解在1体积的水中,形成密度为1.159g/cm3的溶液。则该溶液的物质的量浓度为___ 。
(4)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质,写出一个包含上述七种物质的氧化还原反应方程式(不用配平):__ 。上述反应中,生成1mol氧化产物,还原剂失去__ mol电子。
(1)混在氯气中的HCl气体可用饱和食盐水除去。请设计一个简单实验证明产生的氯气中含有HCl
(2)氯气可以制得漂粉精和消毒水(有效成分为NaClO),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):
(3)在标准状态下,300体积的氯化氢溶解在1体积的水中,形成密度为1.159g/cm3的溶液。则该溶液的物质的量浓度为
(4)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质,写出一个包含上述七种物质的氧化还原反应方程式(不用配平):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用化学用语表达。
(1) K2S的电子式_______ 。
(2)氯气溶于水的离子方程式_______ 。
(3)漂白粉在空气中失效的化学方程式为_______ 。
(1) K2S的电子式
(2)氯气溶于水的离子方程式
(3)漂白粉在空气中失效的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯化钠是一种重要的化工原料,可用于制备如下图所示的一系列物质。
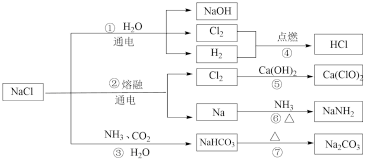
(1)反应①的离子方程式为___________ ,反应中氧化剂为___________ 。
(2)Na+的离子结构示意图为___________ ,NH3的电子式为___________ 。
(3)漂白粉在空气中久置易变质的原因是___________ (用文字表述)。
(4)氨基钠(NaNH2)是生产维生素A的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨,再加热至一定温度生成氨基钠和氢气。NaNH2中氮元素的化合价为___________ ,该反应属于四大基本反应类型中的___________ 。

(1)反应①的离子方程式为
(2)Na+的离子结构示意图为
(3)漂白粉在空气中久置易变质的原因是
(4)氨基钠(NaNH2)是生产维生素A的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨,再加热至一定温度生成氨基钠和氢气。NaNH2中氮元素的化合价为
您最近一年使用:0次
【推荐1】储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑ +2K2SO4+2Cr2(SO4)3 +8H2O。请回答下列问题:
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目_______ 。
(2)上述反应中氧化剂是__ , 每生成 lmolCO2,转移电子数目为_______ 。
(3)请配平下列离子方程式__ 。 Fe 2+ +_______ H++_______ =_______Fe3++_______N2O↑+_______H2O
=_______Fe3++_______N2O↑+_______H2O
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目
(2)上述反应中氧化剂是
(3)请配平下列离子方程式
 =_______Fe3++_______N2O↑+_______H2O
=_______Fe3++_______N2O↑+_______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)将符合下列反应类型的化学方程式的序号填入相应的横线中:
①Fe3O4+4CO 3Fe+4CO2
3Fe+4CO2
②2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
③Zn+H2SO4=ZnSO4+H2↑
④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
⑥3Fe+2O2 Fe3O4
Fe3O4
⑦CuO+H2 Cu十H2O
Cu十H2O
属于化合反应的是_______ ,属于分解反应的是_______ ,属于复分解反应的是_______ ,属于置换反应的是_______ ,属于氧化还原反应的是_______ 。
(2)在化学反应Fe+CuSO4=Cu+FeSO4中,该反应的还原剂是_______ (填化学式)。
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是_______。(双选,漏选错选无分填字母序号)
(4)当反应2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O,有1个FeO 离子生成时,转移的电子数是
离子生成时,转移的电子数是_______ 个。
(5)铜和浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目
CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目_______ 。
(1)将符合下列反应类型的化学方程式的序号填入相应的横线中:
①Fe3O4+4CO
 3Fe+4CO2
3Fe+4CO2②2KMnO4
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑③Zn+H2SO4=ZnSO4+H2↑
④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O⑥3Fe+2O2
 Fe3O4
Fe3O4⑦CuO+H2
 Cu十H2O
Cu十H2O属于化合反应的是
(2)在化学反应Fe+CuSO4=Cu+FeSO4中,该反应的还原剂是
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是_______。(双选,漏选错选无分填字母序号)
| A.Cl2+2NaOH=NaCl+NaClO+H2O |
B.4P+5O2 2P2O5 2P2O5 |
| C.Zn+CuCl2=Cu+ZnCl2 |
| D.3NO2+H2O=2HNO3+NO |
 离子生成时,转移的电子数是
离子生成时,转移的电子数是(5)铜和浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目
CuSO4+SO2↑+2H2O用双线桥标出电子转移的方向和数目
您最近一年使用:0次

 。
。 ,则生成
,则生成 的物质的量为
的物质的量为 ,转移电子的物质的量为
,转移电子的物质的量为

