煤的气化是煤炭综合利用的重要途径之一,主要反应为 。
。
(1)作为还原剂的物质是___________ ,氢元素的化合价___________ (填“升高”或“降低”)。
(2)若消耗了 ,则生成
,则生成 的物质的量为
的物质的量为___________  ,转移电子的物质的量为
,转移电子的物质的量为___________  。
。
 。
。(1)作为还原剂的物质是
(2)若消耗了
 ,则生成
,则生成 的物质的量为
的物质的量为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
更新时间:2023-05-23 22:17:33
|
相似题推荐
【推荐1】世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全杀菌消毒剂,ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,它在食品保鲜、饮用水消毒等方面有着广泛的应用。
(1)实验室制备ClO2的方法之一为: ( H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是 。
( H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是 。
(2) KClO3和浓盐酸在一定温度下反应也会生成绿黄色的二氧化氯。其变化可表示为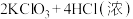
 。
。
①浓盐酸在反应中表现出来的性质是___________ ;
②已知每产生0.1mol Cl2,则发生转移的电子的物质的量为0.2mol。ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒后的还原产物是氯离子,则其消毒的效率(以单位质量得到的电子数表示)是Cl2的______ 倍。(答案保留小数点后两位)
(1)实验室制备ClO2的方法之一为:
 ( H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是 。
( H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是 。| A. KClO3在反应中得到电子 | B. ClO2是氧化产物 |
| C. H2C2O4在反应中被氧化 | D.1mol KClO3参加反应有2mol电子转移 |
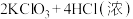
 。
。①浓盐酸在反应中表现出来的性质是
②已知每产生0.1mol Cl2,则发生转移的电子的物质的量为0.2mol。ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒后的还原产物是氯离子,则其消毒的效率(以单位质量得到的电子数表示)是Cl2的
您最近一年使用:0次
【推荐2】 K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:
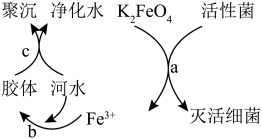
(1)高铁酸钾(K2FeO4)中铁元素的化合价为________ .
(2)过程a中K2FeO4体现________ (填“氧化”或“还原”)性,氧化产物是________ 。
(3)过程b反应的离子方程式为________ ,过程c属于________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:________ 。
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2+ +Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2+ +Cr2O +14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是
+14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是_______ (填离子符号,下同)被氧化的是_______ 。
(2)CO和CO2是碳的两种重要氧化物
①在标准状况下,5.6LCO的物质的量是_______ ,质量_______ 。
②11gCO2的体积是_______ L(标准状况)
③相同质量的CO和CO2所含的原子个数比是_______ 。
(1)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2+ +Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2+ +Cr2O +14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是
+14H+=6Fe3++2Cr3++7H2O,在该反应中,氧化剂是(2)CO和CO2是碳的两种重要氧化物
①在标准状况下,5.6LCO的物质的量是
②11gCO2的体积是
③相同质量的CO和CO2所含的原子个数比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。
(1)X的化学式是___________ 。
(2)用双线桥法标出,上述反应中电子转移的方向和数目___________ 。
(3)上述反应中的还原剂为___________ (填化学式),被还原的元素是___________ (填元素符号)。
(4)向酸性 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是___________ ,反应后溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)0.2mol 参加上述反应,转移电子
参加上述反应,转移电子___________ mol。
 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。(1)X的化学式是
(2)用双线桥法标出,上述反应中电子转移的方向和数目
(3)上述反应中的还原剂为
(4)向酸性
 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是(5)0.2mol
 参加上述反应,转移电子
参加上述反应,转移电子
您最近一年使用:0次
【推荐2】一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
(2)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 :而中毒的事件,其原因是
:而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。下列也能实现这种转化的物质是___________ (填字母序号)。
A. B.
B. C.
C.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___________ 性。
(4)在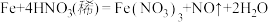 的反应中,
的反应中, 表现了
表现了___________ 性和___________ 性,每有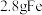 参加反应,转移电子数
参加反应,转移电子数___________ 个;生成的 (标准状况下)体积为
(标准状况下)体积为___________  。
。
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
(2)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 :而中毒的事件,其原因是
:而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有A.
 B.
B. C.
C.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在
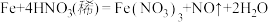 的反应中,
的反应中, 表现了
表现了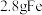 参加反应,转移电子数
参加反应,转移电子数 (标准状况下)体积为
(标准状况下)体积为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】阅读下列科普短文并回答下列问题:
燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如氢氧燃料电池在工作时,从负极连续通入 ,从正极连续通入
,从正极连续通入 ,二者在电池内部(含
,二者在电池内部(含 或
或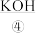 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成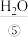 ,同时产生电能。除
,同时产生电能。除 外,
外,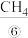 、
、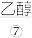 等也可以作为燃料电池的燃料,发生反应生成
等也可以作为燃料电池的燃料,发生反应生成 和
和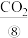 。目前已研制成功
。目前已研制成功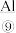 —
—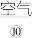 燃料电池,它可以代替汽油为汽车提供动力,反应原理是
燃料电池,它可以代替汽油为汽车提供动力,反应原理是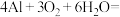
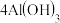 。
。
(1)在上述短文标有序号的物质中,属于单质的是_______ (填序号,下同);属于有机物的是_______ ;属于电解质的是_______ ;溶于水能导电的物质是_______ 。
(2)写出物质③的电离方程式:_______ 。
(3)燃料电池所使用的氢燃料可以来自于水的电解,该反应的化学方程式为_______ 。若电解18kg水,可分解得到__________ L (标准状况下)。
(标准状况下)。
(4)反应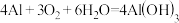 中,得电子的物质是
中,得电子的物质是___________ 。在反应中,每转移1mol电子,消耗Al___________ mol。
燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如氢氧燃料电池在工作时,从负极连续通入
 ,从正极连续通入
,从正极连续通入 ,二者在电池内部(含
,二者在电池内部(含 或
或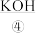 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成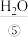 ,同时产生电能。除
,同时产生电能。除 外,
外,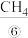 、
、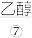 等也可以作为燃料电池的燃料,发生反应生成
等也可以作为燃料电池的燃料,发生反应生成 和
和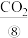 。目前已研制成功
。目前已研制成功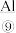 —
—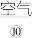 燃料电池,它可以代替汽油为汽车提供动力,反应原理是
燃料电池,它可以代替汽油为汽车提供动力,反应原理是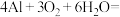
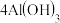 。
。(1)在上述短文标有序号的物质中,属于单质的是
(2)写出物质③的电离方程式:
(3)燃料电池所使用的氢燃料可以来自于水的电解,该反应的化学方程式为
 (标准状况下)。
(标准状况下)。(4)反应
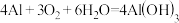 中,得电子的物质是
中,得电子的物质是
您最近一年使用:0次



