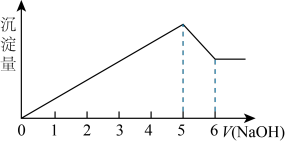回答下列问题。
(1)1 mol CO(NH2)2中含___________ mol氮原子,___________ 个氧原子,所含氧原子数跟___________ mol H2O所含氧原子数相等。
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(3)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式___________ ,若生成6.72L气体(标准状况),则消耗铝的质量为___________ g。
(1)1 mol CO(NH2)2中含
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(3)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
更新时间:2024-03-05 12:44:45
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】完成以物质的量为中心的简单计算:
(1)标准状况下,33.6LCO2的物质的量为_________ ;
(2)1.5molH2O的质量为_________ ;
(3)同温、同压下,等体积的O2和N2的质量比为_________ ;
(4)含有相同氧原子数SO3与SO2的物质的量比是_________ 。
(5)含13.8gNa+的Na3PO4溶液100mL, 的物质的量浓度为
的物质的量浓度为_________ ,取出1mL溶液,Na3PO4的物质的量浓度为_________ 。
(1)标准状况下,33.6LCO2的物质的量为
(2)1.5molH2O的质量为
(3)同温、同压下,等体积的O2和N2的质量比为
(4)含有相同氧原子数SO3与SO2的物质的量比是
(5)含13.8gNa+的Na3PO4溶液100mL,
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】向Ba(OH)2溶液中先滴加一定量CuSO4溶液,直至沉淀质量为m克,再不断滴加H2SO4溶液。整个过程中,产生沉淀的质量与加入溶液的质量关系如图所示。
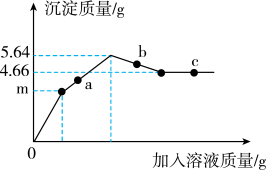
(1)a点对应溶液pH___________ (选填“>”、“=”或“<”)7。
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是___________ 。
(3)通过计算确定m的值___________ 。(写出计算过程)

(1)a点对应溶液pH
(2)取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是
(3)通过计算确定m的值
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】质量、物质的量、物质的量浓度等是用于化学计算的常见物理量,根据所学知识回答下列问题。
(1)标准状况下,17gNH3的体积为___________ ,含有氢原子个数为___________ ,它与标准状况下___________ L H2S含有相同数目的氢原子。
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(3)现有含 、
、 和
和 的混合溶液
的混合溶液 ,已知其中
,已知其中 ,
, ,
,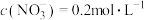 ,则此溶液中
,则此溶液中 为
为___________  。
。
(4) 溶液中含
溶液中含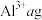 ,取
,取 溶液稀释到
溶液稀释到 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是___________  。
。
(5)标准状况下,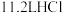 的物质的量是
的物质的量是___________  ,将这些气体溶于水中配成
,将这些气体溶于水中配成 溶液,所得盐酸的物质的量浓度是
溶液,所得盐酸的物质的量浓度是___________  。
。
(1)标准状况下,17gNH3的体积为
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(3)现有含
 、
、 和
和 的混合溶液
的混合溶液 ,已知其中
,已知其中 ,
, ,
,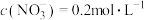 ,则此溶液中
,则此溶液中 为
为 。
。(4)
 溶液中含
溶液中含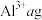 ,取
,取 溶液稀释到
溶液稀释到 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是 。
。(5)标准状况下,
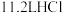 的物质的量是
的物质的量是 ,将这些气体溶于水中配成
,将这些气体溶于水中配成 溶液,所得盐酸的物质的量浓度是
溶液,所得盐酸的物质的量浓度是 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)9.03×1023个CH4中,含____ mol碳原子,___ mol氢原子,___ mol质子,____ mol电子。与___ 个NH3含有相同数目的氢原子。
(2)与17gNH3所含有分子数相同的氧气的体积(标准状况)是_____ L。
(3)某3.65g气体在标准状况下的体积是2.24L,则其摩尔质量是________ 。
(4)标准状况下9.03×1023个CH4所占的体积为________ 。
(2)与17gNH3所含有分子数相同的氧气的体积(标准状况)是
(3)某3.65g气体在标准状况下的体积是2.24L,则其摩尔质量是
(4)标准状况下9.03×1023个CH4所占的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】标准状况下,0.2molCH4中含有的CH4分子数是___________ 个,含氢原子数是___________ 个,0.2mol OH-中含有的电子数是___________ 个,0.2mol NH 其中含有的质子数是
其中含有的质子数是___________ 个。12 g石墨晶体中含有的碳碳键数目为(1mol碳原子含1.5mol碳碳键)___________
 其中含有的质子数是
其中含有的质子数是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】硫黄制硫酸时发生的反应有S+O2 SO2、2SO2+O2
SO2、2SO2+O2 2SO3、SO3+H2O=H2SO4。
2SO3、SO3+H2O=H2SO4。
(1)由硫黄制取硫酸的关系式是_______ 。
(2)假设64g硫黄完全反应,可制取硫酸的质量是_______ 。
 SO2、2SO2+O2
SO2、2SO2+O2 2SO3、SO3+H2O=H2SO4。
2SO3、SO3+H2O=H2SO4。(1)由硫黄制取硫酸的关系式是
(2)假设64g硫黄完全反应,可制取硫酸的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】根据要求进行计算:
(1)amolHClO4中含b个氧原子,则阿伏加德罗常数NA=_______ mol-1(用含a、b的代数式表示)。
(2)某含氯化合物X在标准状况下为气体,7.3gX在标准状况下的体积为4.48L,则X的摩尔质量是_______ 。
(3)1774年瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合制氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。
MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。
①生成的氯气在标准状况下的体积是_______ 。
②稀释后溶液中MnCl2的物质的量浓度是_______ 。
(1)amolHClO4中含b个氧原子,则阿伏加德罗常数NA=
(2)某含氯化合物X在标准状况下为气体,7.3gX在标准状况下的体积为4.48L,则X的摩尔质量是
(3)1774年瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合制氯气:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。
MnCl2+Cl2↑+2H2O。现将92.8g含MnO2的质量分数为75%的软锰矿与足量10mol·L-1的浓盐酸完全反应(杂质不参加反应)。把反应后的溶液稀释成400mL(已知Mn的相对原子质量为55)。①生成的氯气在标准状况下的体积是
②稀释后溶液中MnCl2的物质的量浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】2023年2月16日,空间站梦天实验舱燃烧科学实验柜成功执行首次在轨点火测试。
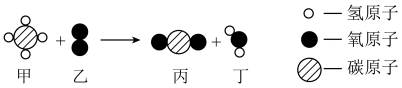
(1)此次点火实验采用甲烷作为燃料,甲烷完全燃烧的微观反应示意图如下,参加反应的甲和生成丙的质量比为___________ (写最简比)。
(2)宇航员压力服的头盔面窗两层之间充有高纯氮气,通过分离液态空气得到氮气是利用氮气和氧气的___________ 不同。
(3)空间站电池翼上的光伏太阳能电池板,为核心舱提供源源不断的动力。光伏发电用到的高纯硅可用二氧化硅( )和碳在高温条件下反应制取,同时生成一种可燃性气体,该反应的化学方程式是
)和碳在高温条件下反应制取,同时生成一种可燃性气体,该反应的化学方程式是___________ 。
(1)此次点火实验采用甲烷作为燃料,甲烷完全燃烧的微观反应示意图如下,参加反应的甲和生成丙的质量比为

(2)宇航员压力服的头盔面窗两层之间充有高纯氮气,通过分离液态空气得到氮气是利用氮气和氧气的
(3)空间站电池翼上的光伏太阳能电池板,为核心舱提供源源不断的动力。光伏发电用到的高纯硅可用二氧化硅(
 )和碳在高温条件下反应制取,同时生成一种可燃性气体,该反应的化学方程式是
)和碳在高温条件下反应制取,同时生成一种可燃性气体,该反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】选用化学方法除去下列物质中混有的少量杂质,写出有关反应的离子方程式。
(1)氧化铁中混有氧化铝_______ ,_______ 。
(2)氧化铜中混有氧化钠_______ ,_______ 。
(3)铜粉中混有氧化铜_______ ,_______ 。
(4)铁粉中混有氧化亚铁_______ ,_______ 。
(1)氧化铁中混有氧化铝
(2)氧化铜中混有氧化钠
(3)铜粉中混有氧化铜
(4)铁粉中混有氧化亚铁
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为___________ ,发生反应的离子方程式为___________ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是___________ 。
(3)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为___________ 。
②滤液Ⅱ中溶质的用途之一是___________ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: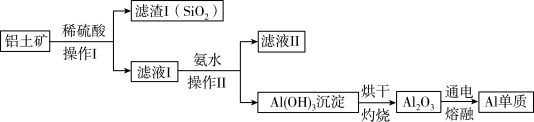
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为②滤液Ⅱ中溶质的用途之一是
您最近一年使用:0次