氯及其部分化合物相关转化如下.
(1)常温下, 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ .
(2)下列有关流程中的物质的说法正确的是:_______________.
(3) 与浓硫酸反应可得
与浓硫酸反应可得 (
(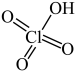 ):
):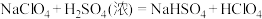 ,利用减压蒸馏分离
,利用减压蒸馏分离 .试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):
.试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):__________ . 在液态时为双聚体,请写出
在液态时为双聚体,请写出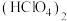 的结构式:
的结构式:___________ .
(4)通过分析,M分子中只有一种化学环境的氢原子. 与
与 经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:
经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:______________ 。设计实验检验D:_______________ 。

(1)常温下,
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:(2)下列有关流程中的物质的说法正确的是:_______________.
A.工业上采用软锰矿(主要成分是 )与浓盐酸混合加热制备 )与浓盐酸混合加热制备 |
| B.混合物A、B的物质的量之比为可为5:1 |
C.若C中的各原子最外层均达8电子稳定结构,C确定为 |
D. 具有强氧化性,用作自来水的消毒剂 具有强氧化性,用作自来水的消毒剂 |
(3)
 与浓硫酸反应可得
与浓硫酸反应可得 (
( ):
):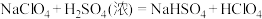 ,利用减压蒸馏分离
,利用减压蒸馏分离 .试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):
.试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析): 在液态时为双聚体,请写出
在液态时为双聚体,请写出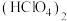 的结构式:
的结构式:(4)通过分析,M分子中只有一种化学环境的氢原子.
 与
与 经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:
经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:
23-24高三下·浙江·开学考试 查看更多[3]
浙江省新阵地教育联盟 浙江十校2023-2024学年高三下学期开学化学试题(已下线)化学(浙江卷02)-2024年高考押题预测卷(已下线)压轴题11 无机化工流程综合分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
更新时间:2024-02-28 19:29:31
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。
(1)CO2属于_______ (填“电解质”、“非电解质”)。
(2)从物质分类标准看,“铜绿”属于_______(填字母)。
(3)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出用盐酸除去铜绿而不损伤器物的反应的离子方程式_______ 。
(4)古代人们高温灼孔雀石[Cu2(OH)2·CuCO3]和木炭的混合物得到一种紫红色的金属铜,其化学反应式为CuO+C Cu+CO↑,该反应属于_______(填序号)。
Cu+CO↑,该反应属于_______(填序号)。
(5)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:2Cu2S+3O2 2Cu2O+2SO2;Cu2S+2Cu2O
2Cu2O+2SO2;Cu2S+2Cu2O 6Cu+SO2↑。第一个反应中转移的电子总数是
6Cu+SO2↑。第一个反应中转移的电子总数是_______ ,第二个反应中氧化剂有_______ 。如把红色的Cu2O固体放入稀硫酸中,溶液显蓝色,反应的离子方程式如下:Cu2O+2H+=Cu2++Cu。请用双线桥表示该反应电子转移的方向和数目_______ 。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为_______ 。
(1)CO2属于
(2)从物质分类标准看,“铜绿”属于_______(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(4)古代人们高温灼孔雀石[Cu2(OH)2·CuCO3]和木炭的混合物得到一种紫红色的金属铜,其化学反应式为CuO+C
 Cu+CO↑,该反应属于_______(填序号)。
Cu+CO↑,该反应属于_______(填序号)。| A.化合反应 | B.置换反应 | C.氧化还原反应 | D.非氧化还原反应 |
 2Cu2O+2SO2;Cu2S+2Cu2O
2Cu2O+2SO2;Cu2S+2Cu2O 6Cu+SO2↑。第一个反应中转移的电子总数是
6Cu+SO2↑。第一个反应中转移的电子总数是(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】粗盐水经过滤后仍含有 、
、 、
、 等杂质离子。为除掉这些杂质离子,常采用以下实验步骤:
等杂质离子。为除掉这些杂质离子,常采用以下实验步骤:
①加入过量 溶液,沉淀后过滤;
溶液,沉淀后过滤;
②在步骤①所得滤液中加入过量 溶液,沉淀后过滤;
溶液,沉淀后过滤;
③在步骤②所得滤液中加入过量 溶液,沉淀后过滤;
溶液,沉淀后过滤;
④在步骤③所得滤液中加入适量盐酸,即可得到纯净的 溶液。
溶液。
请回答:
(1)步骤①中加入溶液的目的是除去_______ (填“ ”或“
”或“ ”)。
”)。
(2)步骤②中加入 溶液必须
溶液必须_______ (填“少量”或“过量”),其目的是_______ 。
(3)步骤③中产生的白色是 和
和_______ (填“ ”或“
”或“ ”)的混合物,发生反应的离子方程式为
”)的混合物,发生反应的离子方程式为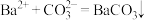 、
、_______ 。
 、
、 、
、 等杂质离子。为除掉这些杂质离子,常采用以下实验步骤:
等杂质离子。为除掉这些杂质离子,常采用以下实验步骤:①加入过量
 溶液,沉淀后过滤;
溶液,沉淀后过滤;②在步骤①所得滤液中加入过量
 溶液,沉淀后过滤;
溶液,沉淀后过滤;③在步骤②所得滤液中加入过量
 溶液,沉淀后过滤;
溶液,沉淀后过滤;④在步骤③所得滤液中加入适量盐酸,即可得到纯净的
 溶液。
溶液。请回答:
(1)步骤①中加入溶液的目的是除去
 ”或“
”或“ ”)。
”)。(2)步骤②中加入
 溶液必须
溶液必须(3)步骤③中产生的白色是
 和
和 ”或“
”或“ ”)的混合物,发生反应的离子方程式为
”)的混合物,发生反应的离子方程式为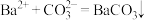 、
、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。现有以下物质:①熔融NaHSO4 ②BaCO3固体 ③铝条 ④氨气 ⑤硫化氢 ⑥蔗糖 ⑦氯水
(1)以上物质中能导电的是_______ (填标号,下同),属于电解质的是_______ ,属于非电解质的是_______
(2)写出①溶于水的电离方程式_______
(3)等质量④和⑤中氢原子的数目之比为_______ ;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为_______ 。
(4)在足量①的水溶液中加入少量②反应的离子方程式_______
(1)以上物质中能导电的是
(2)写出①溶于水的电离方程式
(3)等质量④和⑤中氢原子的数目之比为
(4)在足量①的水溶液中加入少量②反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在①H2S ②SO2 ③CO ④Cl2 ⑤HCl 五种气体中,能使品红溶液褪色的是_______ ;通入石蕊试液先变红后褪色的是_______ ,只变红不褪色的是_______ ;能使碘化钾淀粉试纸变蓝的是_______ ;能与溴水反应的是_______ 。(填序号)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在淀粉KI溶液中加入少量NaClO溶液,并加入少量硫酸,溶液立即变蓝,所发生的离子方程式是____________ ,在上述蓝色溶液中滴加足量的Na2SO3溶液,现象是___________ ,所发生的离子方程式是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用氯元素价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①⑩均含氯元素。回答下列问题:

(1)④的化学式为_______ ,⑦的酸性比碳酸_______ (填“强”或“弱”)。
(2)比较等浓度的⑥和⑦溶液的酸性强弱_______ (填“可以”或“不可以”)用 试纸分别测定。
试纸分别测定。
(3)工业制漂白粉是将①通入_______ 中(填名称)制成的,漂白粉放置时间长了就会失效,写出漂白粉失效的化学方程式_______ ,_______ 。
(4)某一淡黄色粉末与⑥相似,也具有漂白性,这种粉末能与⑤反应生成⑧,请写出该反应的化学方程式_______ 。

(1)④的化学式为
(2)比较等浓度的⑥和⑦溶液的酸性强弱
 试纸分别测定。
试纸分别测定。(3)工业制漂白粉是将①通入
(4)某一淡黄色粉末与⑥相似,也具有漂白性,这种粉末能与⑤反应生成⑧,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据要求填空:
(1)下列现代分析手段中,可用于检验水中痕量铜元素的是_________(填字母)。
(2)红宝石是刚玉的一种,主要成分为氧化铝,因含微量杂质元素铬(Cr)而呈红色。基态铬原子的价层电子排布式为__________ 。
(3)铜催化烯烃确化反应时会产生 ,键角:
,键角:
___ 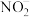 (填“<”或“=”或“>”),其原因是
(填“<”或“=”或“>”),其原因是___________ 。
(4)①乙酸;②丙酸;③二氯乙酸的酸性由强到弱的顺序为_________ (填序号)。
(5)有机物吡啶(C5H5N),结构简式为 ,其中N的杂化方式为
,其中N的杂化方式为____ ,吡啶在水中的溶解度远大于在苯中的溶解度,可能原因是:
①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②__________ 。
(1)下列现代分析手段中,可用于检验水中痕量铜元素的是_________(填字母)。
| A.原子光谱 | B.质谱 | C.X射线衍射 | D.红外光谱 |
(3)铜催化烯烃确化反应时会产生
 ,键角:
,键角:
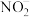 (填“<”或“=”或“>”),其原因是
(填“<”或“=”或“>”),其原因是(4)①乙酸;②丙酸;③二氯乙酸的酸性由强到弱的顺序为
(5)有机物吡啶(C5H5N),结构简式为
 ,其中N的杂化方式为
,其中N的杂化方式为①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮、磷、砷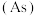 、锑
、锑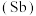 、铋
、铋 、镆
、镆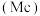 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)氮和磷氢化物性质的比较:热稳定性:
___________  (填“>”“<”)。 沸点:
(填“>”“<”)。 沸点:
___________ 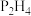 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是___________ 。
(2) 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是___________ (填序号)。
a.不能与 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应
(3) 能发生较强烈的水解,生成难溶的
能发生较强烈的水解,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式 ___________ ,因此,配制 溶液应注意
溶液应注意___________ 。
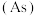 、锑
、锑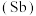 、铋
、铋 、镆
、镆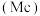 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:(1)氮和磷氢化物性质的比较:热稳定性:

 (填“>”“<”)。 沸点:
(填“>”“<”)。 沸点:
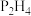 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(2)
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是a.不能与
 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应(3)
 能发生较强烈的水解,生成难溶的
能发生较强烈的水解,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式  溶液应注意
溶液应注意
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】填空。
(1)非金属氟化物在生产、生活和科研中应用广泛。
①OF2分子的空间结构为___________ ;OF2的熔、沸点___________ (填“高于”或“低于”)Cl2O,原因是___________ 。
②Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为___________ ,下列对XeF2中心原子杂化方式推断合理的是___________ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(2)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物II。
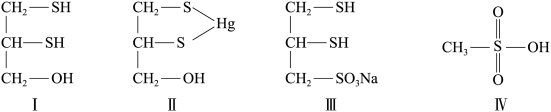
①H2S、CH4、H2O的沸点由高到低顺序为___________ 。
②化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有___________ 。
A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C—C—C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
③汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是___________ 。
(3)硅和卤素单质反应可以得到SiX4。SiX4的熔、沸点如下表:
①0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是___________ (填化学式),沸点依次升高的原因是___________ ,气态SiX4分子的空间结构是___________ 。
②SiCl4与N甲基咪唑(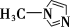 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
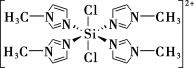
N甲基咪唑分子中碳原子的杂化轨道类型为___________ ,H、C、N的电负性由大到小的顺序为___________ ,1个M2+中含有___________ 个σ键。
(1)非金属氟化物在生产、生活和科研中应用广泛。
①OF2分子的空间结构为
②Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(2)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物II。

①H2S、CH4、H2O的沸点由高到低顺序为
②化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有
A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C—C—C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
③汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是
(3)硅和卤素单质反应可以得到SiX4。SiX4的熔、沸点如下表:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
②SiCl4与N甲基咪唑(
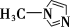 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
N甲基咪唑分子中碳原子的杂化轨道类型为
您最近一年使用:0次



