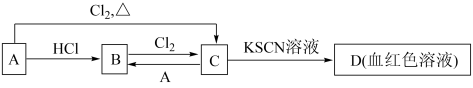
铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加___________ ,若变为红色,则说明其已变质。
(2)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力。以上事实说明
结合的能力。以上事实说明 具有
具有___________ 。下列不能实现 转化为
转化为 的物质是
的物质是___________ (填字母)。
A. B.
B. C.
C. D.
D.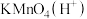
(3) 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: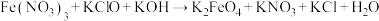 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)从制造印刷电路板的废液中回收铜,并重新获得 溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得
溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:
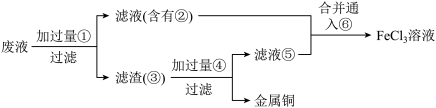
请写出上述流程中加入物质④的化学式:___________ 。请写出通入⑥反应的离子方程式___________ 。
(5)实验室由 固体配制
固体配制 溶液。
溶液。
①如下图所示的仪器中配制溶液不需使用的是___________ (填字母),还缺少的玻璃仪器是___________ (填写仪器名称)。
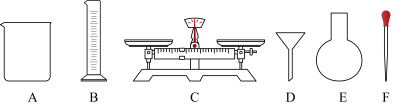
②若实验遇下列情况,导致所配溶液的物质的量浓度偏低的是___________ (填字母)。
A.定容时仰视刻度线 B. 固体失去部分结晶水
固体失去部分结晶水
C.移液前,容量瓶内有蒸馏水 D.未冷却至室温就转移定容
(1)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加(2)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力。以上事实说明
结合的能力。以上事实说明 具有
具有 转化为
转化为 的物质是
的物质是A.
 B.
B. C.
C. D.
D.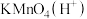
(3)
 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: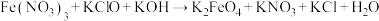 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为(4)从制造印刷电路板的废液中回收铜,并重新获得
 溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得
溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:
请写出上述流程中加入物质④的化学式:
(5)实验室由
 固体配制
固体配制 溶液。
溶液。①如下图所示的仪器中配制溶液不需使用的是

②若实验遇下列情况,导致所配溶液的物质的量浓度偏低的是
A.定容时仰视刻度线 B.
 固体失去部分结晶水
固体失去部分结晶水C.移液前,容量瓶内有蒸馏水 D.未冷却至室温就转移定容
更新时间:2024-03-09 18:15:40
|
相似题推荐
解答题-原理综合题
|
容易
(0.94)
【推荐1】研究氮及其化合物的性质具有极为重要的意义。
(1)NOx是汽车尾气中的主要污染物之一、NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_______ ,此反应的氧化产物是_______ ,1molNO2反应转移电子_______ mol。
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,写出实验室用固体加热制取NH3的化学方程式为_______ ,用5.35g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为_______ L。(NH4Cl的摩尔质量为53.5g·mol-1)
(3)实验室可以用铜与稀硝酸制取NO,写出该反应的离子方程式:_______ 。
(4)工业上采用氨氧化法制取硝酸,写出在催化剂作用下氨气与氧气反应的化学方程式:__ 。
(5)工业合成氨原料气氢气通过碳与水蒸气反应制取。已知1mol水蒸气和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ 。写出该反应的热化学方程式______ 。
(1)NOx是汽车尾气中的主要污染物之一、NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,写出实验室用固体加热制取NH3的化学方程式为
(3)实验室可以用铜与稀硝酸制取NO,写出该反应的离子方程式:
(4)工业上采用氨氧化法制取硝酸,写出在催化剂作用下氨气与氧气反应的化学方程式:
(5)工业合成氨原料气氢气通过碳与水蒸气反应制取。已知1mol水蒸气和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ 。写出该反应的热化学方程式
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】如图所示,先在小烧杯中加入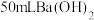 溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
(1)从物质类别看, 属于
属于____________ ;小灯泡变亮的原因是____________ .
(2)向小烧杯中滴加 溶液,观察到以下现象,按要求填写产生对应现象的原因:
溶液,观察到以下现象,按要求填写产生对应现象的原因:
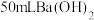 溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
(1)从物质类别看,
 属于
属于(2)向小烧杯中滴加
 溶液,观察到以下现象,按要求填写产生对应现象的原因:
溶液,观察到以下现象,按要求填写产生对应现象的原因:| 序号 | 现象 | 产生该现象的原因 |
| 1 | 酚酞颜色变浅直至褪去 | 用离子方程式表达:① |
| 2 | 产生白色沉淀 | 用离子方程式表达:② |
| 3 | 小灯泡变暗直至熄灭 | 文字表达:③ |
| 4 | 小灯泡又变亮 | 用电离方程式表达:④ |
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐1】对印刷电路板制作过程中 产生废液X进行回收处理,流程如图所示。
产生废液X进行回收处理,流程如图所示。
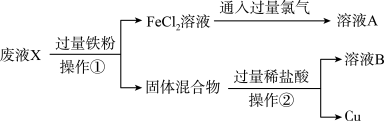
(1)操作①的名称是_______ 。
(2)废液X与过量铁粉的反应,除发生 反应外,还可能发生
反应外,还可能发生_______ (用离子方程式表示)。
(3)下列物质中,在一定条件下能与铁反应,且铁元素化合价全部 变为+3价的是_______ (填字母)。
A.稀硫酸 B. C.氯气
C.氯气
(4)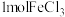 与Cu完全反应,转移电子数约为
与Cu完全反应,转移电子数约为_______ 。
 产生废液X进行回收处理,流程如图所示。
产生废液X进行回收处理,流程如图所示。
(1)操作①的名称是
(2)废液X与过量铁粉的反应,除发生
 反应外,还可能发生
反应外,还可能发生(3)下列物质中,在一定条件下能与铁反应,且铁元素化合价
A.稀硫酸 B.
 C.氯气
C.氯气(4)
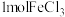 与Cu完全反应,转移电子数约为
与Cu完全反应,转移电子数约为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐2】I.黄铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)的流程如下:

回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是_______ (填序号)。
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是_______ (填化学式)。
(3)“沉淀反应”时不宜混入过多空气,其原因为_______ (用离子方程式表示)。
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加_______ 溶液。
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为_______ 。
II.为滴定检验提氧化物的纯度,现需配制 的硫酸溶液。请回答以下问题:
的硫酸溶液。请回答以下问题:
(6)仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是_______ 。
(7)请将下列各操作,按正确的顺序填在横线上。
A.用30mL水洗涤烧杯和玻璃棒2—3次,洗涤液均注入仪器①中,振荡
B.用量筒准确量取所需体积的浓硫酸,沿玻璃棒倒入盛有少量水的烧杯中,再用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入仪器①中
D.将仪器①盖紧瓶塞,反复上下颠倒,摇匀
E.改用仪器②加水,使溶液凹面恰好与刻度相切
F.继续往仪器①内小心加水,直到液面接近刻度线1—2cm处
其操作正确的顺序依次为_______ 。
(8)下列哪种情况使所配制的稀硫酸的浓度偏小_______ 。
A.溶解浓硫酸后未冷却直接配制溶液
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.用量筒量取浓硫酸时俯视刻度
E.用蒸馏水洗净量筒后直接量取浓硫酸配置溶液

回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是
(3)“沉淀反应”时不宜混入过多空气,其原因为
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为
II.为滴定检验提氧化物的纯度,现需配制
 的硫酸溶液。请回答以下问题:
的硫酸溶液。请回答以下问题:(6)仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是
(7)请将下列各操作,按正确的顺序填在横线上。
A.用30mL水洗涤烧杯和玻璃棒2—3次,洗涤液均注入仪器①中,振荡
B.用量筒准确量取所需体积的浓硫酸,沿玻璃棒倒入盛有少量水的烧杯中,再用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入仪器①中
D.将仪器①盖紧瓶塞,反复上下颠倒,摇匀
E.改用仪器②加水,使溶液凹面恰好与刻度相切
F.继续往仪器①内小心加水,直到液面接近刻度线1—2cm处
其操作正确的顺序依次为
(8)下列哪种情况使所配制的稀硫酸的浓度偏小
A.溶解浓硫酸后未冷却直接配制溶液
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.用量筒量取浓硫酸时俯视刻度
E.用蒸馏水洗净量筒后直接量取浓硫酸配置溶液
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
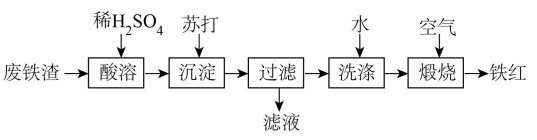
【推荐3】铁红可用于油漆、油墨、橡胶等工业中,可作为玻璃、宝石、金属的抛光剂等。某课外活动小组用废铁渣(含Fe和少量Fe2O3)制取铁红,所设计的流程如下:
(1)苏打中的化学键类型为___________ ;沉淀的化学式为___________ ;“滤液”中主要溶质的化学式为___________ 。
(2)要检测“酸溶”后,溶液中是否含有Fe3+所用的试剂是___________ (名称);若溶液中检测不到Fe3+的原因是___________ 。
(3)“酸溶”时,Fe2O3与稀硫酸反应的离子方程式为___________ 。
(4)实验室过滤所需的玻璃仪器(填名称)有___________ 。
(5)煅烧的化学方程式为___________ 。
(1)苏打中的化学键类型为
(2)要检测“酸溶”后,溶液中是否含有Fe3+所用的试剂是
(3)“酸溶”时,Fe2O3与稀硫酸反应的离子方程式为
(4)实验室过滤所需的玻璃仪器(填名称)有
(5)煅烧的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐1】利用生物浸出黄铜矿(主要成分CuFeS2,含有少量SiO2杂质)回收其中铁和铜的工艺流程如图:
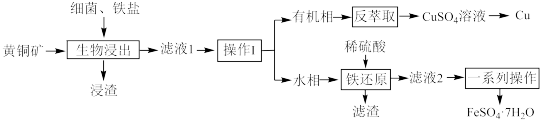
回答下列问题:
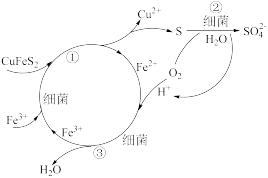
(1)Cu2+的生物浸出原理如图:浸出温度不宜过高,其原因是_____ ,反应①的离子方程式为____ 。
(2)浸渣的主要成分为____ (填化学式),操作1的名称为____ 。
(3)分离Cu2+的原理如下:Cu2++2(HR)org (CuR2)org+2H+。根据流程,反萃取加入的试剂应该为
(CuR2)org+2H+。根据流程,反萃取加入的试剂应该为_____ (填化学式)。
(4)检验滤液2中是否存在Fe3+,可选用_____ (填标号)。
(5)“一系列操作”包括_____ 、洗涤、干燥。

回答下列问题:
(1)Cu2+的生物浸出原理如图:浸出温度不宜过高,其原因是

(2)浸渣的主要成分为
(3)分离Cu2+的原理如下:Cu2++2(HR)org
 (CuR2)org+2H+。根据流程,反萃取加入的试剂应该为
(CuR2)org+2H+。根据流程,反萃取加入的试剂应该为(4)检验滤液2中是否存在Fe3+,可选用
| A.KSCN溶液 | B.K4[Fe(CN)6]溶液 | C.K3[Fe(CN)6]溶液 | D.KMnO4溶液 |
(5)“一系列操作”包括
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐2】某工厂废水中含大量 和少量的
和少量的 、
、 、
、 ,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):

(1)“试剂Ⅱ”为_______ ,与“试剂Ⅰ”反应的离子有_______
(2)“红褐色沉淀”为_______ ,“ ”的作用是
”的作用是_______
(3)“试剂Ⅲ”是沉淀“溶液B”中 ,证明“溶液B”中
,证明“溶液B”中 已经完全沉淀的试剂为
已经完全沉淀的试剂为_______ 。
(4)“溶液B”中残留 与“试剂Ⅲ”反应的化学方程式为
与“试剂Ⅲ”反应的化学方程式为_______ 。
(5)“溶液C”在空气中晾晒一段时间后,加盐酸调成弱酸性,蒸发可得工业食盐,但加盐酸时有少量气泡逸出,经检验为 ,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)_______
 和少量的
和少量的 、
、 、
、 ,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
(1)“试剂Ⅱ”为
(2)“红褐色沉淀”为
 ”的作用是
”的作用是(3)“试剂Ⅲ”是沉淀“溶液B”中
 ,证明“溶液B”中
,证明“溶液B”中 已经完全沉淀的试剂为
已经完全沉淀的试剂为(4)“溶液B”中残留
 与“试剂Ⅲ”反应的化学方程式为
与“试剂Ⅲ”反应的化学方程式为(5)“溶液C”在空气中晾晒一段时间后,加盐酸调成弱酸性,蒸发可得工业食盐,但加盐酸时有少量气泡逸出,经检验为
 ,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐1】实验室需要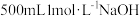 溶液,根据溶液配制情况回答下列问题:
溶液,根据溶液配制情况回答下列问题:
(1)实验中除了托盘天平(砝码)、药匙、量筒、烧杯、胶头滴管外还需要的其他仪器有_______ 。
(2)称取 固体时,所需的质量为
固体时,所需的质量为_______  。定容时,加水至液面离容量瓶刻度线
。定容时,加水至液面离容量瓶刻度线_______ 处,改用 _______ 进行定容
(3)洗涤烧杯和玻璃棒_______ 次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
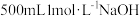 溶液,根据溶液配制情况回答下列问题:
溶液,根据溶液配制情况回答下列问题:(1)实验中除了托盘天平(砝码)、药匙、量筒、烧杯、胶头滴管外还需要的其他仪器有
(2)称取
 固体时,所需的质量为
固体时,所需的质量为 。定容时,加水至液面离容量瓶刻度线
。定容时,加水至液面离容量瓶刻度线(3)洗涤烧杯和玻璃棒
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐2】新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液(有效成分 );②
);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸(
酒精;⑧过氧乙酸( );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号)。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用导致游泳池藻类快速生长,池水变绿,写出该反应的化学方程式___________ 。
(3)实验室可用 溶液配制消毒液。
溶液配制消毒液。
①需要用托盘天平称量 固体的质量为
固体的质量为___________  ;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有
;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有___________ 。
②下列情况会导致所配制溶液浓度偏高的是___________ (填标号)。
a.称量时所用的砝码生锈
b.移液时,有少量液体浅出
c.定容时,俯视刻度线
(4)高铁酸钠 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为___________ 。用 代替
代替 处理饮用水的优点是
处理饮用水的优点是___________ (只答一条即可)。
 );②
);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸(
酒精;⑧过氧乙酸( );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用导致游泳池藻类快速生长,池水变绿,写出该反应的化学方程式
(3)实验室可用
 溶液配制消毒液。
溶液配制消毒液。①需要用托盘天平称量
 固体的质量为
固体的质量为 ;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有
;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有②下列情况会导致所配制溶液浓度偏高的是
a.称量时所用的砝码生锈
b.移液时,有少量液体浅出
c.定容时,俯视刻度线
(4)高铁酸钠
 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为 代替
代替 处理饮用水的优点是
处理饮用水的优点是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】新冠肺炎疫情期间,环境消毒是极其关键的,常常喷洒“84”消毒液,其有效成分为NaClO。已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常稀释100倍(体积之比)后使用请回答下列问题:
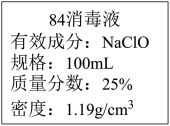
(1)某同学取100mL该“84”消毒液,稀释100倍后用于消毒,稀释后的溶液中 =
=_______  。(保留到小数点后两位)
。(保留到小数点后两位)
(2)某实验需用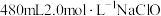 的消毒液,现用NaClO固体配制,用托盘天平称量NaClO的固体质量为
的消毒液,现用NaClO固体配制,用托盘天平称量NaClO的固体质量为_______ g,需要的玻璃仪器有_______ 。
(3)以下有关配制该溶液的说法正确的是_______ (填字母)。
A.溶解NaClO固体的操作如图①所示
B.定容时的操作如图②所示
C.定容时的操作可用图③表示
D.定容时向容量瓶内加蒸馏水至接近刻度线1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
E.定容摇匀后,若发现凹液面低于刻度线,此时不需要用胶头滴管补加蒸馏水至刻度线
(4)下列操作可能使配制溶液浓度偏低的是_______ (填字母)。
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液且马上定容
C.移液时,有少量液体溅出
D.定容时,仰视刻度线
E.容量瓶内有少量水
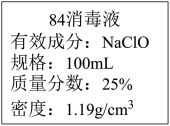
(1)某同学取100mL该“84”消毒液,稀释100倍后用于消毒,稀释后的溶液中
 =
= 。(保留到小数点后两位)
。(保留到小数点后两位)(2)某实验需用
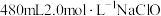 的消毒液,现用NaClO固体配制,用托盘天平称量NaClO的固体质量为
的消毒液,现用NaClO固体配制,用托盘天平称量NaClO的固体质量为(3)以下有关配制该溶液的说法正确的是
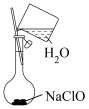 |  | 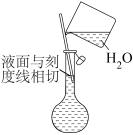 |
| ① | ② | ③ |
B.定容时的操作如图②所示
C.定容时的操作可用图③表示
D.定容时向容量瓶内加蒸馏水至接近刻度线1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
E.定容摇匀后,若发现凹液面低于刻度线,此时不需要用胶头滴管补加蒸馏水至刻度线
(4)下列操作可能使配制溶液浓度偏低的是
A.移液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液且马上定容
C.移液时,有少量液体溅出
D.定容时,仰视刻度线
E.容量瓶内有少量水
您最近一年使用:0次