H2S是一种大气污染物。工业尾气中含有H2S,会造成严重的环境污染;未脱除H2S的煤气,运输过程中还会腐蚀管道。
(1)干法氧化铁脱硫是目前除去煤气中H2S的常用方法,其原理如图所示。____________ (填序号)。
a.单质硫为黄色固体
b.脱硫反应为
c.再生过程中,硫元素被还原
d.脱硫过程中,增大反应物的接触面积可提高脱硫效率
②从安全环保的角度考虑,再生过程需控制反应温度不能过高的原因是_____________ 。
(2)电化学溶解—沉淀法是一种回收利用H2S的新方法,其工艺原理如下图所示。
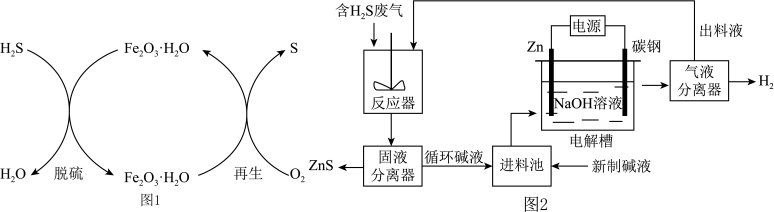
已知:Zn与强酸、强碱都能反应生成H2;Zn(II)在过量的强碱溶液中以 形式存在。
形式存在。
①锌棒连接直流电源的___________ (填“正极”或“负极”)。
②反应器中反应的离子方程式为_________ 。
③电解槽中,没接通电源时已经有H2产生,用化学用语解释原因:________ 。
(3)常用碘量法测定煤气中H2S的含量,其实验过程如下:
i.将10L煤气通入盛有100mL锌氨络合液的洗气瓶中,将其中的H2S全部转化为ZnS沉淀,过滤;
ⅱ.将带有沉淀的滤纸加入盛有15mL0.1mol/L碘标准液、200mL水和10mL盐酸的碘量瓶中,盖上瓶塞,摇动碘量瓶至瓶内滤纸摇碎,置于暗处反应10min后,用少量水冲洗瓶壁和瓶塞。(已知: )
)
ⅲ.用0.1mol/LNa2S2O3标准液滴定,待溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点。(已知: )
)
①滴定终点的现象是_______ 。
②若消耗Na2S2O3标准液的体积为20mL,则煤气中H2S的含量为_______ mg/m3。
(1)干法氧化铁脱硫是目前除去煤气中H2S的常用方法,其原理如图所示。
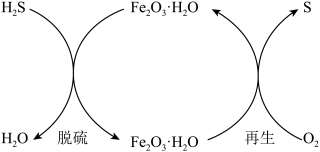
a.单质硫为黄色固体
b.脱硫反应为

c.再生过程中,硫元素被还原
d.脱硫过程中,增大反应物的接触面积可提高脱硫效率
②从安全环保的角度考虑,再生过程需控制反应温度不能过高的原因是
(2)电化学溶解—沉淀法是一种回收利用H2S的新方法,其工艺原理如下图所示。

已知:Zn与强酸、强碱都能反应生成H2;Zn(II)在过量的强碱溶液中以
 形式存在。
形式存在。①锌棒连接直流电源的
②反应器中反应的离子方程式为
③电解槽中,没接通电源时已经有H2产生,用化学用语解释原因:
(3)常用碘量法测定煤气中H2S的含量,其实验过程如下:
i.将10L煤气通入盛有100mL锌氨络合液的洗气瓶中,将其中的H2S全部转化为ZnS沉淀,过滤;
ⅱ.将带有沉淀的滤纸加入盛有15mL0.1mol/L碘标准液、200mL水和10mL盐酸的碘量瓶中,盖上瓶塞,摇动碘量瓶至瓶内滤纸摇碎,置于暗处反应10min后,用少量水冲洗瓶壁和瓶塞。(已知:
 )
)ⅲ.用0.1mol/LNa2S2O3标准液滴定,待溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点。(已知:
 )
)①滴定终点的现象是
②若消耗Na2S2O3标准液的体积为20mL,则煤气中H2S的含量为
23-24高三下·北京海淀·阶段练习 查看更多[2]
北京大学附属中学预科部2023-2024学年高三下学期3月阶段练习化学试题(已下线)大题04 化学反应原理综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
更新时间:2024-03-09 18:33:21
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】绿矾(FeSO4·7H2O)在工业上可用于制造铁盐、氧化铁红及靛青等。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
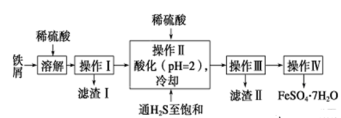
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为________ 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液 D.苯酚溶液
(2)操作Ⅱ中,通入硫化氢至饱和的目的是______________________________________ ;在溶液中用硫酸酸化至pH=2的目的是__________________________________ 。
(3)操作Ⅳ的顺序依次为_________________ 、冷却结晶、____________________ 。
(4)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②_________________________________________________________ 。
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.850 g绿矾产品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用硫酸酸化的0.010 00 mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
①滴定时盛放KMnO4溶液的仪器为________________________ (填仪器名称)。
②计算上述样品中FeSO4·7H2O的质量分数为____________________ 。

| 25℃ | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS开始沉淀 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液 D.苯酚溶液
(2)操作Ⅱ中,通入硫化氢至饱和的目的是
(3)操作Ⅳ的顺序依次为
(4)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.850 g绿矾产品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用硫酸酸化的0.010 00 mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
①滴定时盛放KMnO4溶液的仪器为
②计算上述样品中FeSO4·7H2O的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】LiMn2O4是一种无污染、成本低的锂离子电池电极材料,某研究小组利用柠檬酸配合法制备LiMn2O4。
(1)按一定配比将醋酸锂(CH3COOLi)和醋酸锰[(CH3COO)2Mn]溶液混合后,加入柠檬酸(分子式C6H8O7)溶液中配成混料。用6 mol·L-1氨水调节pH至6.5~9,在75℃~85℃水浴中加热,制得柠檬酸配合物(其中Mn为+2价)。装置如图所示(加热和夹持装置已略去)。

①滴液漏斗中a管的作用是________ 。
②实验室用14.8 mol·L-1浓氨水配制250 mL 6mol·L-1的氨水需要的仪器有胶头滴管、烧杯、玻璃棒、量筒、________ 。
③调节pH至6.5~9是为了促进柠檬酸电离。pH不能大于9的原因是______ 。
④用水浴加热的目的是__________ 。
(2)将制得的配合物在烘箱中真空干燥得到固态柠檬酸配合物前驱体,研磨后焙烧,得LiMn2O4。
①柠檬酸配合物前驱体应放在_______ (填仪器名称)中焙烧。
②焙烧需要在空气中进行的原因是__________ 。
③焙烧产生的气体是________ 。
(3)测定产品中锰的含量:准确称取0.1000 g的产品试样,加入足量浓盐酸溶液加热溶解,驱赶溶液中残留的Cl2,配成250 mL溶液。取25.00 mL溶液于锥形瓶中用0.02000 mol·L-1EDTA(Mn2+与EDTA按1:1络合)滴定,消耗EDTA溶液的体积V mL。样品中锰的质量分数为_________ 。
(1)按一定配比将醋酸锂(CH3COOLi)和醋酸锰[(CH3COO)2Mn]溶液混合后,加入柠檬酸(分子式C6H8O7)溶液中配成混料。用6 mol·L-1氨水调节pH至6.5~9,在75℃~85℃水浴中加热,制得柠檬酸配合物(其中Mn为+2价)。装置如图所示(加热和夹持装置已略去)。

①滴液漏斗中a管的作用是
②实验室用14.8 mol·L-1浓氨水配制250 mL 6mol·L-1的氨水需要的仪器有胶头滴管、烧杯、玻璃棒、量筒、
③调节pH至6.5~9是为了促进柠檬酸电离。pH不能大于9的原因是
④用水浴加热的目的是
(2)将制得的配合物在烘箱中真空干燥得到固态柠檬酸配合物前驱体,研磨后焙烧,得LiMn2O4。
①柠檬酸配合物前驱体应放在
②焙烧需要在空气中进行的原因是
③焙烧产生的气体是
(3)测定产品中锰的含量:准确称取0.1000 g的产品试样,加入足量浓盐酸溶液加热溶解,驱赶溶液中残留的Cl2,配成250 mL溶液。取25.00 mL溶液于锥形瓶中用0.02000 mol·L-1EDTA(Mn2+与EDTA按1:1络合)滴定,消耗EDTA溶液的体积V mL。样品中锰的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】三氯化六氨合钴[Co(NH3)6]Cl3是一种重要的化工原料。利用含钴废料(含少量Fe、Al等杂质)制取[Co(NH3)6]Cl3的工艺流程如图所示:

已知:①“酸浸”过滤后的滤液中含有Co2+、Fe2+、Fe3+、Al3+等。
②Ksp[Co(OH)2]=1×10-14.2 、Ksp[Co(OH)3]=1×10-43.7
Ksp[Fe(OH)3]=1×10-37.4 、Ksp[Al(OH)3]=1×10-32.9
已知:溶液中金属离子物质的量浓度低于1.0×l0-5mol/L时,可认为沉淀完全。
③[Co(NH3)6]2+具有较强还原性。
回答下列问题:
(1)制备CoCl2。
①Co2+的价电子排布式为___________ 。
②“除杂”过程中加Na2CO3调节pH后会生成两种沉淀,同时得到含c(Co2+)=0.1 mol·L-1的滤液,调节pH的范围为___________ 。
(2)制备 [Co(NH3)6]3+。
①“混合”过程中需先将NH4Cl,CoCl2溶液混合,然后再加入活性炭,NH4Cl的作用是___________ ,___________ 。
②“氧化”过程应先加入___________ (选填“氨水”或“双氧水”),原因是___________ ,___________ 。
③生成[Co(NH3)6]3+的离子方程式为___________ 。
(3)分离提纯。将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到[Co(NH3)6]Cl3晶体。该过程中加入浓盐酸的目的是___________ 。
(4)含量测定。通过碘量法可测定产品中的钴元素的含量。称取0.10g产品加入稍过量的NaOH溶液并加热,将Co完全转化为难溶的Co(OH)3,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的KI和2~3滴淀粉溶液,再用0.010mol·L-1的Na2S2O3溶液滴定(反应原理:Co3++I-→Co2++I2、I2+S2O →I-+S4O
→I-+S4O ),达到滴定终点时消耗Na2S2O3溶液24.00mL,则产品中钴元素的含量为
),达到滴定终点时消耗Na2S2O3溶液24.00mL,则产品中钴元素的含量为___________ (写出解题过程)。

已知:①“酸浸”过滤后的滤液中含有Co2+、Fe2+、Fe3+、Al3+等。
②Ksp[Co(OH)2]=1×10-14.2 、Ksp[Co(OH)3]=1×10-43.7
Ksp[Fe(OH)3]=1×10-37.4 、Ksp[Al(OH)3]=1×10-32.9
已知:溶液中金属离子物质的量浓度低于1.0×l0-5mol/L时,可认为沉淀完全。
③[Co(NH3)6]2+具有较强还原性。
回答下列问题:
(1)制备CoCl2。
①Co2+的价电子排布式为
②“除杂”过程中加Na2CO3调节pH后会生成两种沉淀,同时得到含c(Co2+)=0.1 mol·L-1的滤液,调节pH的范围为
(2)制备 [Co(NH3)6]3+。
①“混合”过程中需先将NH4Cl,CoCl2溶液混合,然后再加入活性炭,NH4Cl的作用是
②“氧化”过程应先加入
③生成[Co(NH3)6]3+的离子方程式为
(3)分离提纯。将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到[Co(NH3)6]Cl3晶体。该过程中加入浓盐酸的目的是
(4)含量测定。通过碘量法可测定产品中的钴元素的含量。称取0.10g产品加入稍过量的NaOH溶液并加热,将Co完全转化为难溶的Co(OH)3,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的KI和2~3滴淀粉溶液,再用0.010mol·L-1的Na2S2O3溶液滴定(反应原理:Co3++I-→Co2++I2、I2+S2O
 →I-+S4O
→I-+S4O ),达到滴定终点时消耗Na2S2O3溶液24.00mL,则产品中钴元素的含量为
),达到滴定终点时消耗Na2S2O3溶液24.00mL,则产品中钴元素的含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2、NO是大气污染物。吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
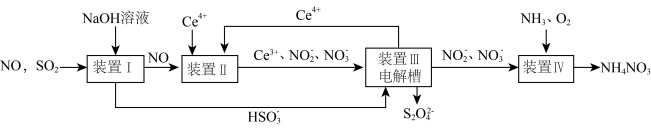
(1)装置Ⅰ中生成HSO3-的离子方程式为_____ 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
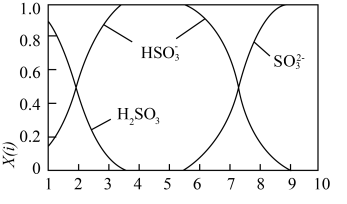
①下列说法正确的是_____ (填字母序号)。
A.pH=8时,溶液中c(HSO3-) <c(SO32-)
B.pH=7时,溶液中c(Na+)=c(HSO3-)+c(SO32-)
C.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:_____ 。
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式____ 。
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示。
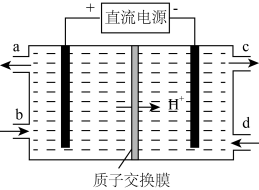
①生成Ce4+的电极反应式为_________ 。
②生成Ce4+从电解槽的_____ (填字母序号)口流出。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g/L,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2___ L。(用含a代数式表示,计算结果保留整数)

(1)装置Ⅰ中生成HSO3-的离子方程式为
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。

①下列说法正确的是
A.pH=8时,溶液中c(HSO3-) <c(SO32-)
B.pH=7时,溶液中c(Na+)=c(HSO3-)+c(SO32-)
C.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示。

①生成Ce4+的电极反应式为
②生成Ce4+从电解槽的
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g/L,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2
您最近一年使用:0次
【推荐2】将废旧锌锰电池进行回收处理以实现资源的再生利用,初步处理后的废料中含 、
、 、
、 及
及 等,用该废料制备
等,用该废料制备 和
和 的一种工艺流程如图:
的一种工艺流程如图:

已知:①Mn的金属活动性强于Fe, 在酸性条件下比较稳定,pH大于5.5时易被氧化。
在酸性条件下比较稳定,pH大于5.5时易被氧化。
②相关物质的 数据如表所示。
数据如表所示。
回答下列问题:
(1)为加快“还原焙烧”时的反应速率,可采取的措施有_______ (填一条),该过程中生成的气体产物有 、
、 和
和________ (填化学式);“酸浸”后分离出滤渣1的操作名称为_________ 。
(2)已知,“净化”时溶液中 、
、 的物质的量浓度均约为
的物质的量浓度均约为 ,当金属离子的浓度小于
,当金属离子的浓度小于 时可认为该离子完全沉淀,则“净化”时调节
时可认为该离子完全沉淀,则“净化”时调节 的合理范围是
的合理范围是
___________ 。
(3)通过“电解”滤液2制备 和
和 ,若电路中转移
,若电路中转移 电子,溶液的
电子,溶液的 将
将___________ (填“增大”或“减小”)。
(4) 为两性氢氧化物,可溶于
为两性氢氧化物,可溶于 溶液,反应为
溶液,反应为
 ,其平衡常数
,其平衡常数
___________ {已知: 的平衡常数称为稳定平衡常数,
的平衡常数称为稳定平衡常数, 。
。
(5)在 条件下,
条件下, 和
和 按4:1的物质的量比发生反应制得
按4:1的物质的量比发生反应制得 ,同时产物还有
,同时产物还有 和
和 ,则该反应中n(氧化产物):n(还原产物)=
,则该反应中n(氧化产物):n(还原产物)=___________ ;以石墨和 为电极材料可制作可充电电池,该电池的总反应为
为电极材料可制作可充电电池,该电池的总反应为 ,充电时
,充电时 电极上发生的电极反应为
电极上发生的电极反应为___________ ,若此时电路中转移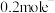 ,则石墨电极将增重
,则石墨电极将增重___________ g。
 、
、 、
、 及
及 等,用该废料制备
等,用该废料制备 和
和 的一种工艺流程如图:
的一种工艺流程如图:
已知:①Mn的金属活动性强于Fe,
 在酸性条件下比较稳定,pH大于5.5时易被氧化。
在酸性条件下比较稳定,pH大于5.5时易被氧化。②相关物质的
 数据如表所示。
数据如表所示。| 化合物 |  |  |  |
 |  | 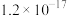 |  |
(1)为加快“还原焙烧”时的反应速率,可采取的措施有
 、
、 和
和(2)已知,“净化”时溶液中
 、
、 的物质的量浓度均约为
的物质的量浓度均约为 ,当金属离子的浓度小于
,当金属离子的浓度小于 时可认为该离子完全沉淀,则“净化”时调节
时可认为该离子完全沉淀,则“净化”时调节 的合理范围是
的合理范围是
(3)通过“电解”滤液2制备
 和
和 ,若电路中转移
,若电路中转移 电子,溶液的
电子,溶液的 将
将(4)
 为两性氢氧化物,可溶于
为两性氢氧化物,可溶于 溶液,反应为
溶液,反应为
 ,其平衡常数
,其平衡常数
 的平衡常数称为稳定平衡常数,
的平衡常数称为稳定平衡常数, 。
。(5)在
 条件下,
条件下, 和
和 按4:1的物质的量比发生反应制得
按4:1的物质的量比发生反应制得 ,同时产物还有
,同时产物还有 和
和 ,则该反应中n(氧化产物):n(还原产物)=
,则该反应中n(氧化产物):n(还原产物)= 为电极材料可制作可充电电池,该电池的总反应为
为电极材料可制作可充电电池,该电池的总反应为 ,充电时
,充电时 电极上发生的电极反应为
电极上发生的电极反应为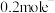 ,则石墨电极将增重
,则石墨电极将增重
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学原理在海水资源综合利用及污染治理方面有着重要的作用。
(1)电解饱和食盐水的原理如图所示。
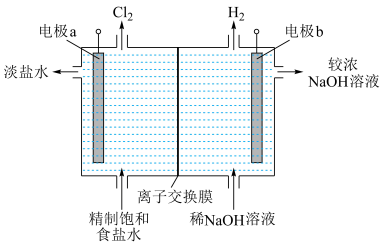
①电解饱和食盐水的离子方程式是______________________________ 。
②电极a接电源的________ (填“正”或“负”)极。
③离子交换膜主要允许________ (填离子符号)通过。
④解释装置右侧出口得到较浓NaOH溶液的原因:_________________ 。
(2)煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将 转化为
转化为 ,
, 再将煤中的含硫物质(主要成分是
再将煤中的含硫物质(主要成分是 )氧化为
)氧化为 和
和 ,即
,即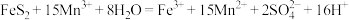 。
。
已知:两电极为完全相同的惰性电极。

① 电极上的电极反应式为
电极上的电极反应式为_____________________ 。
②电解池工作时,观察到 电极上有无色气体产生,写出电极反应式:
电极上有无色气体产生,写出电极反应式:__________________________ 。
当转移电子的物质的量为 时,则生成的无色气体在标准状况下的体积为
时,则生成的无色气体在标准状况下的体积为________ L。
③电解池工作时, 往
往________ (填“ ”或“
”或“ ”)极移动,一段时间后,混合液中
”)极移动,一段时间后,混合液中 的物质的量
的物质的量________ (填“变大”“变小”或“不变”)。
(1)电解饱和食盐水的原理如图所示。

①电解饱和食盐水的离子方程式是
②电极a接电源的
③离子交换膜主要允许
④解释装置右侧出口得到较浓NaOH溶液的原因:
(2)煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将
 转化为
转化为 ,
, 再将煤中的含硫物质(主要成分是
再将煤中的含硫物质(主要成分是 )氧化为
)氧化为 和
和 ,即
,即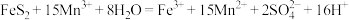 。
。已知:两电极为完全相同的惰性电极。

①
 电极上的电极反应式为
电极上的电极反应式为②电解池工作时,观察到
 电极上有无色气体产生,写出电极反应式:
电极上有无色气体产生,写出电极反应式:当转移电子的物质的量为
 时,则生成的无色气体在标准状况下的体积为
时,则生成的无色气体在标准状况下的体积为③电解池工作时,
 往
往 ”或“
”或“ ”)极移动,一段时间后,混合液中
”)极移动,一段时间后,混合液中 的物质的量
的物质的量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸锌在农业、医药、食品行业中有着广泛的应用。以红锌矿(主要成分为ZnO,还含有少量的FeO、MnO、 等)为原料制备
等)为原料制备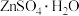 的流程如图:
的流程如图:
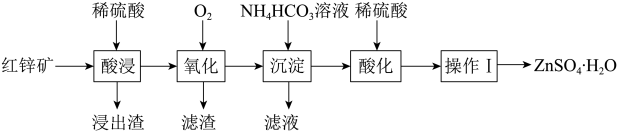
回答下列问题:
(1)“酸浸”时,欲加快反应速率,可采取的措施有_______ (写两种)。“浸出渣”的主要成分是_______ 。
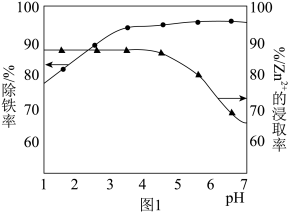
(2)“酸浸”时溶液的pH与除铁率、 的浸取率的关系如图1,“酸浸”时溶液的pH应控制在
的浸取率的关系如图1,“酸浸”时溶液的pH应控制在_______ (填整数)左右。
(3)“滤渣”的主要成分为 ,写出“氧化”时的离子方程式
,写出“氧化”时的离子方程式_______ 。
(4)“沉淀”得到的难溶物为 ,写出“沉淀”时反应的离子方程式
,写出“沉淀”时反应的离子方程式_______ 。
(5)“滤液”中浓度较大的两种阳离子是_______ 。
(6)硫酸锌晶体的溶解度与温度的变化如图2所示。“操作Ⅰ”是:_______ ,洗涤、干燥。

 等)为原料制备
等)为原料制备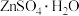 的流程如图:
的流程如图:
回答下列问题:
(1)“酸浸”时,欲加快反应速率,可采取的措施有
(2)“酸浸”时溶液的pH与除铁率、
 的浸取率的关系如图1,“酸浸”时溶液的pH应控制在
的浸取率的关系如图1,“酸浸”时溶液的pH应控制在
(3)“滤渣”的主要成分为
 ,写出“氧化”时的离子方程式
,写出“氧化”时的离子方程式(4)“沉淀”得到的难溶物为
 ,写出“沉淀”时反应的离子方程式
,写出“沉淀”时反应的离子方程式(5)“滤液”中浓度较大的两种阳离子是
(6)硫酸锌晶体的溶解度与温度的变化如图2所示。“操作Ⅰ”是:

您最近一年使用:0次
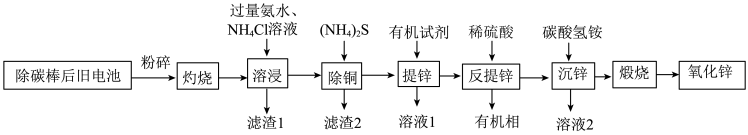
【推荐2】随着生活水平的提高,旧电池的回收利用成为当前世界各国研究的重要课题,我国科学家提出利用旧干电池(除碳棒后,主要成分为:Zn、Fe、Cu、 、
、 以及
以及 )回收氧化锌的流程如图:
)回收氧化锌的流程如图:
已知:
①二氧化锰难溶于水、弱酸、弱碱。锌、铜氧化物及其盐能溶于氨水形成配合物(如 )。
)。
②室温下, ,
, 。
。
③室温下,一些金属氢氧化物沉淀时的pH如下表:
回答下列问题:
(1)旧电池灼烧的目的是__________ ;滤渣1的主要成分是__________ (填化学式)。
(2)若在实验室中进行“提锌”操作,该操作的名称为__________ 。
(3) 含有的
含有的 键数为
键数为__________  ;氧化铜的熔点比硫化铜高的原因是
;氧化铜的熔点比硫化铜高的原因是__________ 。
(4)室温下,测得除铜后溶液中: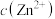 为
为 、
、 为
为 ,此时溶液中
,此时溶液中
__________ (填“能”或“不能”)形成沉淀。
(5)工业上常采用电解硫酸锌溶液的方法制备锌,阴极电极反应式为__________ 。
 、
、 以及
以及 )回收氧化锌的流程如图:
)回收氧化锌的流程如图:
已知:
①二氧化锰难溶于水、弱酸、弱碱。锌、铜氧化物及其盐能溶于氨水形成配合物(如
 )。
)。②室温下,
 ,
, 。
。③室温下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 |
|
|
|
开始沉淀的pH | 2.3 | 5.9 | 5.4 |
完全沉淀的pH | 3.2 | 8.2(>10时溶解) | 6.7 |
(1)旧电池灼烧的目的是
(2)若在实验室中进行“提锌”操作,该操作的名称为
(3)
 含有的
含有的 键数为
键数为 ;氧化铜的熔点比硫化铜高的原因是
;氧化铜的熔点比硫化铜高的原因是(4)室温下,测得除铜后溶液中:
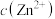 为
为 、
、 为
为 ,此时溶液中
,此时溶液中
(5)工业上常采用电解硫酸锌溶液的方法制备锌,阴极电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
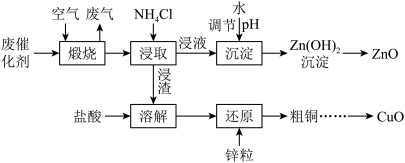
【推荐3】某甲醇合成催化剂常因硫中毒而失活,以该废催化剂(主要含Cu、Zn、Al、O、S、N、C等元素)回收铜、锌的工艺流程如图:
已知: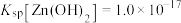
(1)“搬烧”时,烧炉内温度、煅烧时间与烧失率(烧失率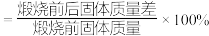 )的关系如下图所示。
)的关系如下图所示。

①温度为950℃时,60min之前烧失率增加的原因是_______ 。
②为了提高烧失率,除适宜的温度和时间外,还可以采取的措施有_______ 。
(2)控制“浸取”温度为75℃,浸取后锌元素主要以 存在,反应达到平衡时存在如下关系:
存在,反应达到平衡时存在如下关系: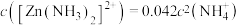 ,
,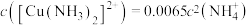 。
。
①浸取ZnO的离子方程式为_______ 。控制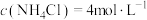 能使大部分ZnO进入浸液,大部分CuO留在浸渣,原因是
能使大部分ZnO进入浸液,大部分CuO留在浸渣,原因是_______ 。
②温度控制在75℃左右,其原因是_______ 。
(3)“沉淀”时,若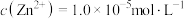 ,滤液的
,滤液的
_______ 。
(4)“还原”反应的离子方程式为_______ 。
(5)流程中可循环使用的物质是_______ (填化学式)。

已知:
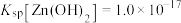
(1)“搬烧”时,烧炉内温度、煅烧时间与烧失率(烧失率
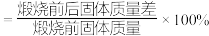 )的关系如下图所示。
)的关系如下图所示。
①温度为950℃时,60min之前烧失率增加的原因是
②为了提高烧失率,除适宜的温度和时间外,还可以采取的措施有
(2)控制“浸取”温度为75℃,浸取后锌元素主要以
 存在,反应达到平衡时存在如下关系:
存在,反应达到平衡时存在如下关系: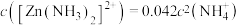 ,
,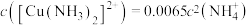 。
。①浸取ZnO的离子方程式为
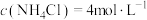 能使大部分ZnO进入浸液,大部分CuO留在浸渣,原因是
能使大部分ZnO进入浸液,大部分CuO留在浸渣,原因是②温度控制在75℃左右,其原因是
(3)“沉淀”时,若
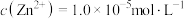 ,滤液的
,滤液的
(4)“还原”反应的离子方程式为
(5)流程中可循环使用的物质是
您最近一年使用:0次






