回答下列问题
(1)化学与日常生活、医药、环保等密不可分.
医药行业的毒胶囊事件曾被央视《每周质量报告》曝光。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
①胶体中的分散质直径范围是______ nm。
②元素铬(Cr)的几种化合物存在转化关系:Cr2O3固体 KCrO2溶液(绿色)
KCrO2溶液(绿色)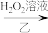 K2CrO4溶液(黄色)
K2CrO4溶液(黄色)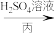 K2Cr2O7溶液(橙红色),从物质分类角度K2CrO4属于
K2Cr2O7溶液(橙红色),从物质分类角度K2CrO4属于______ (“氧化物”、“钾盐”、“碱”);甲、乙、丙中属于复分解反应的步骤是______ 。
③请配平下列离子方程式:____ 。
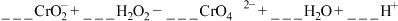
该反应中,H2O2作______ (填“氧化剂”或“还原剂”).
(2)在明代宋应星所著的《天工开物》中,有关于火法炼锌的工艺记载:“每炉甘石(主要成分为熔化成团,冷定毁知取出。……即倭铅也。”
①请完成上述火法炼锌反应的化学方程式并配平:____ 。
ZnCO3+2C ______+CO↑
______+CO↑
在该反应中,氧化产物是______ (填化学式)。
②利用生成的锌粒,加入稀硫酸会发生以下反应:Zn+H2SO4=ZnSO4+H2↑,请用“单线桥法”标出电子转移情况:____________ 。
(1)化学与日常生活、医药、环保等密不可分.
医药行业的毒胶囊事件曾被央视《每周质量报告》曝光。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
①胶体中的分散质直径范围是
②元素铬(Cr)的几种化合物存在转化关系:Cr2O3固体
 KCrO2溶液(绿色)
KCrO2溶液(绿色)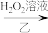 K2CrO4溶液(黄色)
K2CrO4溶液(黄色)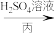 K2Cr2O7溶液(橙红色),从物质分类角度K2CrO4属于
K2Cr2O7溶液(橙红色),从物质分类角度K2CrO4属于③请配平下列离子方程式:
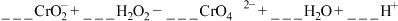
该反应中,H2O2作
(2)在明代宋应星所著的《天工开物》中,有关于火法炼锌的工艺记载:“每炉甘石(主要成分为熔化成团,冷定毁知取出。……即倭铅也。”
①请完成上述火法炼锌反应的化学方程式并配平:
ZnCO3+2C
 ______+CO↑
______+CO↑在该反应中,氧化产物是
②利用生成的锌粒,加入稀硫酸会发生以下反应:Zn+H2SO4=ZnSO4+H2↑,请用“单线桥法”标出电子转移情况:
更新时间:2024-03-11 07:10:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】“化学一我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是____ ,胶体和溶液的本质区别是____ 。
(2)钠的焰色试验的焰色为____ 色,该色的光射程远,透雾力强,据此原理制作的高压钠灯广泛应用于道路和广场的照明。焰色试验属于____ (填“物理”或“化学”)变化。
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是____ ,原因是____ 。
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有____ (填化学式)。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)钠的焰色试验的焰色为
(3)将新鲜的有色花瓣放入干燥的氯气中,可观察到的现象是
(4)漂白粉暴露在空气中易变质,若向暴露在空气中的漂白粉中加入浓盐酸,可能收集到的气体除了挥发的HCl和水蒸气,还可能有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、解决问题都有着重要的意义。请回答下列问题:
(1)2022年6月5日,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭在酒泉卫星发射中心点火发射。神舟十四号载人飞船的成功发射离不开化学燃料。火箭分级推进中使用的燃料主要有①煤油、②液氢、③肼 和 ④固态铝粉,氧化剂主要有⑤液氧、⑥
和 ④固态铝粉,氧化剂主要有⑤液氧、⑥ 和⑦高氯酸铵
和⑦高氯酸铵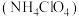 。
。
上述燃料和氧化剂涉及到的物质中,属于混合物的是____________ (填序号,下同);属于氧化物的是____________ ;属于单质的是______________ 。
(2)某同学根据性质划分,把氢溴酸( 溶于水形成的溶液)与盐酸划为一类,其理由是它们的化学性质十分相似.据此判断下列反应不会发生的是___________(填字母)。
溶于水形成的溶液)与盐酸划为一类,其理由是它们的化学性质十分相似.据此判断下列反应不会发生的是___________(填字母)。
(3)A、B、C、D、E五种物质中都含有同一种元素,它们之间的相互转化关系如图所示。
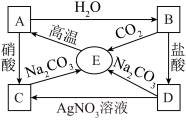
①A、B、C、D、E中所含的相同元素是___________ (填字母)。
a.铜 b.碳 c.铁 d.钙
②写出B的澄清溶液与 反应生成E和另一种物质的离子反应方程式
反应生成E和另一种物质的离子反应方程式________________ 。
(4)请对以下过程形成的分散系进行分类:
①花生油加入水中后充分搅拌;
②一定温度下,向蒸馏水中加入硝酸钾至恰好饱和;
③饱和氯化铁溶液中加入氢氧化钠溶液;
④氢氧化钠溶液中通入过量的 ;
;
⑤将饱和 溶液加入沸水中加热至呈红褐色;
溶液加入沸水中加热至呈红褐色;
⑥将颗粒直径为20~30nm的氧化铜分散在塑料中制备的复合材料.
属于浊液的是_____________ (填序号,下同);属于溶液的是_____________ ;属于胶体的是____________ 。
(1)2022年6月5日,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭在酒泉卫星发射中心点火发射。神舟十四号载人飞船的成功发射离不开化学燃料。火箭分级推进中使用的燃料主要有①煤油、②液氢、③肼
 和 ④固态铝粉,氧化剂主要有⑤液氧、⑥
和 ④固态铝粉,氧化剂主要有⑤液氧、⑥ 和⑦高氯酸铵
和⑦高氯酸铵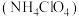 。
。上述燃料和氧化剂涉及到的物质中,属于混合物的是
(2)某同学根据性质划分,把氢溴酸(
 溶于水形成的溶液)与盐酸划为一类,其理由是它们的化学性质十分相似.据此判断下列反应不会发生的是___________(填字母)。
溶于水形成的溶液)与盐酸划为一类,其理由是它们的化学性质十分相似.据此判断下列反应不会发生的是___________(填字母)。A.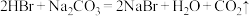 |
B.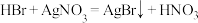 |
C. |
D. |
(3)A、B、C、D、E五种物质中都含有同一种元素,它们之间的相互转化关系如图所示。

①A、B、C、D、E中所含的相同元素是
a.铜 b.碳 c.铁 d.钙
②写出B的澄清溶液与
 反应生成E和另一种物质的离子反应方程式
反应生成E和另一种物质的离子反应方程式(4)请对以下过程形成的分散系进行分类:
①花生油加入水中后充分搅拌;
②一定温度下,向蒸馏水中加入硝酸钾至恰好饱和;
③饱和氯化铁溶液中加入氢氧化钠溶液;
④氢氧化钠溶液中通入过量的
 ;
;⑤将饱和
 溶液加入沸水中加热至呈红褐色;
溶液加入沸水中加热至呈红褐色;⑥将颗粒直径为20~30nm的氧化铜分散在塑料中制备的复合材料.
属于浊液的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是 ____ 。
A.能全部透过滤纸 B.有丁达尔效应
C.所得液体呈胶状 D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是______ 。
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体,回答下列问题:
①写出上述反应的化学方程式_______ 。
②向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象_______ 。
A.能全部透过滤纸 B.有丁达尔效应
C.所得液体呈胶状 D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体,回答下列问题:
①写出上述反应的化学方程式
②向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象
您最近一年使用:0次
【推荐1】氧化还原反应在生产、生活中有广泛的用途。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是_______ (填化学式,下同),还原剂是_______ ,氧化产物和还原产物的个数比是_______ 。
Ⅱ.工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ +
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ + + 14H+ = 6Fe3+ + 2Cr3++ 7H2O
+ 14H+ = 6Fe3+ + 2Cr3++ 7H2O
(2)在该反应中,被氧化的是_______ (填离子符号,下同),还原产物是_______ ,此反应可以推断物质还原性强弱顺序是_______ 。
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO- +2Fe3+ + 10OH- = 2 +_______+ 5H2O
+_______+ 5H2O
(3)请完成该化学方程式并配平_______ 。
(4)该反应中生成2个 转移的电子数为
转移的电子数为_______ 。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是
Ⅱ.工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ +
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ + + 14H+ = 6Fe3+ + 2Cr3++ 7H2O
+ 14H+ = 6Fe3+ + 2Cr3++ 7H2O(2)在该反应中,被氧化的是
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO- +2Fe3+ + 10OH- = 2
 +_______+ 5H2O
+_______+ 5H2O(3)请完成该化学方程式并配平
(4)该反应中生成2个
 转移的电子数为
转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】酸性高锰酸钾一般用硫酸酸化,它也可与H2O2反应,其化学方程式是:H2O2+KMnO4+H2SO4=X+MnSO4+O2+H2O(未配平)。
已知:稀MnSO4溶液几乎无色。
(1)X的化学式是_____ 。上述反应中被氧化的元素是_____ 。
(2)向酸性KMnO4溶液中滴入双氧水,观察到的现象是_____ ,反应后溶液的酸性_____ (填“增强”“减弱”或“不变”)。
已知:稀MnSO4溶液几乎无色。
(1)X的化学式是
(2)向酸性KMnO4溶液中滴入双氧水,观察到的现象是
您最近一年使用:0次
【推荐3】回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3 N2O3+H2O
N2O3+H2O
②N2O4+H2O HNO3+HNO2
HNO3+HNO2
③NH3+NO HNO2+H2O
HNO2+H2O
其中你认为一定不可能实现的是___________ (填序号)。
(3)下列三个氧化还原反应中,氧化性最强的物质是___________ 。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2NaClO3+4HCl(浓)=2NaCl+2ClO2↑+Cl2↑+2H2O
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可以用上述反应中的___________ 做氧化剂。
(4)第(3)问反应③中氧化产物是___________ ,还原产物是___________ 。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3
 N2O3+H2O
N2O3+H2O②N2O4+H2O
 HNO3+HNO2
HNO3+HNO2③NH3+NO
 HNO2+H2O
HNO2+H2O其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2NaClO3+4HCl(浓)=2NaCl+2ClO2↑+Cl2↑+2H2O
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可以用上述反应中的
(4)第(3)问反应③中氧化产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)在下列各反应均涉及HCl:
①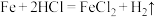 ②
②
③ ④
④
其中HCl做还原剂的是_______ (填序号),HCl做氧化剂的是_______ (填序号);试比较Cl2、Br2、KClO3的氧化性,其由强到弱的顺序为_______ ;试用“单线桥法”标明④中电子转移的方向和数目_______ 。
(2)黑火药着火时主要发生化学反应: 。该反应中被还原的元素为
。该反应中被还原的元素为_______ ,氧化产物为_______ ,若生成14gN2,则转移电子数目为_______ 。
(3)CuCl常用作催化剂,可以在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热生成CuCl沉淀,请写出该反应的离子方程式_______ 。
(1)在下列各反应均涉及HCl:
①
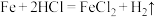 ②
②
③
 ④
④
其中HCl做还原剂的是
(2)黑火药着火时主要发生化学反应:
 。该反应中被还原的元素为
。该反应中被还原的元素为(3)CuCl常用作催化剂,可以在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热生成CuCl沉淀,请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
(1)在下列反应中,HCl作还原剂的是___________ 为还原产物的是___________ (填序号,下同),HCl作氧化剂的是___________ 。
①K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
②Cl2+H2O=HCl+HClO
③2NaCl+H2SO4(浓) Na2SO4+2HCl↑
Na2SO4+2HCl↑
④Fe+2HCl=FeCl2+H2↑
(2)用单线桥法标出反应①中电子转移的方向和数目___________ 。
(3)下列变化中,涉及氧化还原反应的是___________ (填序号)。
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐烂 ④澄清石灰水变浑浊
(4)下列4种基本类型的反应中,一定是氧化还原反应的是___________ (填序号),一定不是氧化还原反应的是___________ (填序号),可能是氧化还原反应的是___________ (填序号)。
①化合反应 ②分解反应 ③置换反应 ④复分解反应
(5)书写下列反应的离子方程式
①Ba(OH)2溶液和CuSO4溶液:___________ ;
②Fe与CuSO4溶液反应:___________ ;
③实验室制备CO2:___________ 。
(1)在下列反应中,HCl作还原剂的是
①K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
②Cl2+H2O=HCl+HClO
③2NaCl+H2SO4(浓)
 Na2SO4+2HCl↑
Na2SO4+2HCl↑④Fe+2HCl=FeCl2+H2↑
(2)用单线桥法标出反应①中电子转移的方向和数目
(3)下列变化中,涉及氧化还原反应的是
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐烂 ④澄清石灰水变浑浊
(4)下列4种基本类型的反应中,一定是氧化还原反应的是
①化合反应 ②分解反应 ③置换反应 ④复分解反应
(5)书写下列反应的离子方程式
①Ba(OH)2溶液和CuSO4溶液:
②Fe与CuSO4溶液反应:
③实验室制备CO2:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)现有下列物质:①Cl2②NaOH溶液③Cu④Na2FeO4⑤Na2CO3•10H2O⑥稀硫酸⑦CO2⑧镁铝合金。其中属于纯净物的有______ ,能导电的物质有______ ,属于电解质的有_____ 。
(2)高铁酸钠是一种新型净水剂,它的氧化性比高锰酸钾、次氯酸等还强。工业上制取高铁酸钠的方法如下:2Fe(NO3)3+16NaOH+3Cl2=2Na2FeO4+ 6NaNO3+ 6NaCl+8H2O。用单线桥表示该反应电子转移的方向和数目______ 。
(3)向含10gNaOH的溶液中通入一定量的CO2,完全反应后,在低温条件下蒸发结晶,最终得到14.8g固体。
①蒸发结晶在低温条件下进行的理由是______ (用化学方程式说明)。
②所得固体中含有的物质的化学式为______ 。
(1)现有下列物质:①Cl2②NaOH溶液③Cu④Na2FeO4⑤Na2CO3•10H2O⑥稀硫酸⑦CO2⑧镁铝合金。其中属于纯净物的有
(2)高铁酸钠是一种新型净水剂,它的氧化性比高锰酸钾、次氯酸等还强。工业上制取高铁酸钠的方法如下:2Fe(NO3)3+16NaOH+3Cl2=2Na2FeO4+ 6NaNO3+ 6NaCl+8H2O。用单线桥表示该反应电子转移的方向和数目
(3)向含10gNaOH的溶液中通入一定量的CO2,完全反应后,在低温条件下蒸发结晶,最终得到14.8g固体。
①蒸发结晶在低温条件下进行的理由是
②所得固体中含有的物质的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2=2Al(OH)3↓ +Na2CO3+H2O
(1)上述五中物质中沸点最低物质的结构式为______________ ,由上述物质中的两种元素按原子个数比1:1形成的离子化合物的电子式为__________________ (写一例)
(2)Al元素的单质有许多不同于其他金属的特性,请列举2例(也可以用化学方程式表示)
______________________ 、__________________________________ .
(3)氢有3种稳定同位素,H氕、D氘、T氚,分别为丰度a、b、c,则计算氢元素的近似相对原子质量的表达式为______________________________________________ .
甲认为H可以排在周期表ⅠA族,也可以排在ⅦA族;而乙同学认为H也可以与碳一样,排在ⅣA族,乙同学的理由是__________________________________________________ 。
(4)已知通入二氧化碳336 L(标准状况下),理论上生成Al(OH)3________________ mol,
实际上生成24 mol Al(OH)3和15 mol Na2CO3,Al(OH)3比理论上要少的原因是:________________________________________________________ .
(1)上述五中物质中沸点最低物质的结构式为
(2)Al元素的单质有许多不同于其他金属的特性,请列举2例(也可以用化学方程式表示)
(3)氢有3种稳定同位素,H氕、D氘、T氚,分别为丰度a、b、c,则计算氢元素的近似相对原子质量的表达式为
甲认为H可以排在周期表ⅠA族,也可以排在ⅦA族;而乙同学认为H也可以与碳一样,排在ⅣA族,乙同学的理由是
(4)已知通入二氧化碳336 L(标准状况下),理论上生成Al(OH)3
实际上生成24 mol Al(OH)3和15 mol Na2CO3,Al(OH)3比理论上要少的原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)配平氧化还原反应方程式:
C2O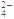 +
+____ MnO +____H+===____CO2↑+____Mn2++____H2O
+____H+===____CO2↑+____Mn2++____H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为________ mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
KMnO4溶液在滴定过程中作________ (填“氧化剂”或“还原剂”),该滴定过程________ (填“需要”或“不需要”)另加指示剂。滴至16 mL时反应完全,此时溶液颜色由________ 变为__________ 。
C2O
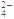 +
+ +____H+===____CO2↑+____Mn2++____H2O
+____H+===____CO2↑+____Mn2++____H2O(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
KMnO4溶液在滴定过程中作
您最近一年使用:0次
【推荐3】消毒剂在生活中应用广泛,Na2FeO4、Cl2、ClO2、H2O2、NaClO 是生活中不同领域的消毒剂。根据下列反应回答问题
A.2H2O2 2H2O+O2↑
2H2O+O2↑
B.16HCl+2KMnO4=5Cl2↑+2MnCl2+2KCl+8H2O
C.2Fe(OH)3+3KClO+4 KOH=2K2FeO4+3KCl+5H2O
D.2KClO3+4HCl=2ClO2↑+2KCl+Cl2↑+2H2O
(1)储存过氧化氢的试剂瓶上最适合贴上的一个标签是_____ (填序号)。

(2)反应 A 中,氧化产物与还原产物的质量之比为_________ ;反应 B 中,做还原剂的 HCl 与做酸性介质的 HCl 物质的量之比为_____ ,0.4mol KMnO4参加反应,做酸性介质的 HCl 的物质的量为_____ 。
(3)用双线桥表示反应 C 电子转移的方向和数目:________
2Fe(OH)3+3KClO+4 KOH=2K2FeO4+3KCl+5H2O
(4)反应 D 中 0.2mol HCl 参加反应,转移的电子数为_____ 。
(5)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:H2O、ClO-、NH 、H+、N2、Cl-。其中 c(Cl-)随反应进行逐渐增加。
、H+、N2、Cl-。其中 c(Cl-)随反应进行逐渐增加。
①氧化产物与还原产物的物质的量之比为_____ 。
② 反应后溶液的酸性_____ (填“增强”或“减弱”)。
(6)ClO2(还原产物为 Cl-)和 K2FeO4[还原产物为 Fe(OH)3]都可用作自来水的消毒剂。等质量的 ClO2和 K2FeO4的消毒能力之比为_____ (计算结果保留一位小数)。
A.2H2O2
 2H2O+O2↑
2H2O+O2↑B.16HCl+2KMnO4=5Cl2↑+2MnCl2+2KCl+8H2O
C.2Fe(OH)3+3KClO+4 KOH=2K2FeO4+3KCl+5H2O
D.2KClO3+4HCl=2ClO2↑+2KCl+Cl2↑+2H2O
(1)储存过氧化氢的试剂瓶上最适合贴上的一个标签是

(2)反应 A 中,氧化产物与还原产物的质量之比为
(3)用双线桥表示反应 C 电子转移的方向和数目:
2Fe(OH)3+3KClO+4 KOH=2K2FeO4+3KCl+5H2O
(4)反应 D 中 0.2mol HCl 参加反应,转移的电子数为
(5)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:H2O、ClO-、NH
 、H+、N2、Cl-。其中 c(Cl-)随反应进行逐渐增加。
、H+、N2、Cl-。其中 c(Cl-)随反应进行逐渐增加。①氧化产物与还原产物的物质的量之比为
② 反应后溶液的酸性
(6)ClO2(还原产物为 Cl-)和 K2FeO4[还原产物为 Fe(OH)3]都可用作自来水的消毒剂。等质量的 ClO2和 K2FeO4的消毒能力之比为
您最近一年使用:0次



