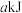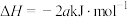下列说法错误的是
A.在25℃和101kPa时, 完全燃烧生成 完全燃烧生成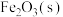 和 和 时放出853kJ的热量,则 时放出853kJ的热量,则 燃烧热的热化学方程式为: 燃烧热的热化学方程式为: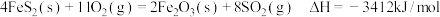 |
| B.在相同条件下,质量相等的两份氢气和足量的氧气充分反应,分别生成液态水(反应①)和水蒸气(反应②),反应①放出的热量多 |
| C.中和反应的反应热测定实验中,需要其中一个反应物稍过量让反应充分进行 |
| D.白铁(镀锌)制品比一般铁器耐腐蚀 |
更新时间:2024-03-11 14:06:26
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某种含二价铜的微粒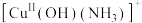 可用于汽车尾气催化脱硝。催化机理如图1所示,反应过程中不同态物质体系所具有的能量如图2所示。下列说法中错误的是
可用于汽车尾气催化脱硝。催化机理如图1所示,反应过程中不同态物质体系所具有的能量如图2所示。下列说法中错误的是
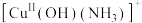 可用于汽车尾气催化脱硝。催化机理如图1所示,反应过程中不同态物质体系所具有的能量如图2所示。下列说法中错误的是
可用于汽车尾气催化脱硝。催化机理如图1所示,反应过程中不同态物质体系所具有的能量如图2所示。下列说法中错误的是
A.该脱硝过程总反应的 |
| B.由状态④到状态⑤发生了氧化还原反应 |
C.总反应的化学方程式为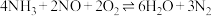 |
| D.根据图2可知,中间态②、③、④对应的物质体系稳定性逐渐升高 |
您最近一年使用:0次
【推荐2】下列说法中正确的是
| A.H2O(g)=H2O(1)是放热反应 |
| B.需要加热才能发生的反应都是吸热反应 |
| C.已知P4(s,白磷)=4P(s,红磷)为放热反应,则红磷比白磷稳定 |
| D.化学反应过程中吸热或放热越多,则温度变化对速率的影响越明显 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】根据已知条件得出的结论正确的是
选项 | 已知条件 | 结论 |
A |
| 中和反应的反应热 |
B |
|
( |
C |
| 碳和氢气的摩尔燃烧焓( |
D | 500℃、30 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知反应热:
①25℃、101 时,
时,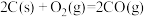
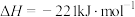
②稀溶液中,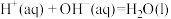
 下列说法正确的是
下列说法正确的是
①25℃、101
 时,
时,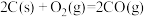
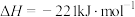
②稀溶液中,
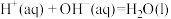
 下列说法正确的是
下列说法正确的是A.①的反应热为 |
B.C的燃烧热等于110.5 |
C.稀硫酸与 固体反应生成1 固体反应生成1 水,放出57.3 水,放出57.3 热量 热量 |
D.稀醋酸与稀 溶液(已知醋酸电离时吸热)的中和热 溶液(已知醋酸电离时吸热)的中和热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列说法或表示方法正确的是( )
| A.等质量的硫蒸气和硫固体分别在氧气中完全燃烧,后者放出的热量少 |
| B.1molH2在足量氯气中完全燃烧所放出的热量,是H2的燃烧热 |
| C.盐酸与NaOH溶液反应的中和热△H=-57.3kJ•mol-1,则硫酸和Ca(OH)2溶液反应的中和热△H=-2×57.3kJ•mol-1 |
| D.一定条件下,0.1molN2(g)与0.3molH2(g)混合充分反应时放出的热量为8kJ,则有N2(g)+3H2(g)⇌2NH3(g)△H=-80kJ•mol-1 |
您最近一年使用:0次
【推荐1】已知热化学方程式 O2(g) +C2H2(g) =2 CO2(g) + H2O (g) ΔH = -1256 kJ·mol-1,下列正确的是( )
O2(g) +C2H2(g) =2 CO2(g) + H2O (g) ΔH = -1256 kJ·mol-1,下列正确的是( )
 O2(g) +C2H2(g) =2 CO2(g) + H2O (g) ΔH = -1256 kJ·mol-1,下列正确的是( )
O2(g) +C2H2(g) =2 CO2(g) + H2O (g) ΔH = -1256 kJ·mol-1,下列正确的是( )| A.乙炔的燃烧热为1256 kJ·mol-1 |
| B.若生成2 mol液态水,则ΔH = -2512 kJ·mol-1 |
| C.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
| D.若转移10 mol电子,则消耗2.5 mol O2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列热化学方程式,正确 的是( )
| A.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
D.500 ℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)  2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】研究化学反应中的能量变化具有重要意义。下列说法正确的是
A.已知: 500° C、30MPa 下,N2(g) +3H2(g)  2NH3(g) ΔH= −92.4 kJ∙mol−1将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ 2NH3(g) ΔH= −92.4 kJ∙mol−1将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热小于46.2kJ |
| B.汽车尾气净化器中的反应为2NO(g) +2CO(g) =N2(g) +2CO2(g) ,该反应在一定条件 下能自发进行,说明该反应的 ΔH>0 |
C.已知反应2NO2(g)  N2O4(g) ΔH <0,升高温度,υ逆增大,υ正减小,平衡逆向移动 N2O4(g) ΔH <0,升高温度,υ逆增大,υ正减小,平衡逆向移动 |
| D.C2H5OH(1) 的燃烧热的热化学方程式为2C2H5OH(1) +6O2(g) =4CO2(g) +6H2O(g) ΔH= −1367.0 kJ∙mol−1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】当镀层破坏后,以下三种情况中铁腐蚀速率由快到慢的顺序是
①白铁(铁上镀锌) ②马口铁(铁上镀锡) ③铜质奖章(铁上镀铜)
①白铁(铁上镀锌) ②马口铁(铁上镀锡) ③铜质奖章(铁上镀铜)
| A.③①② | B.②①③ | C.③②① | D.①②③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列图示中的实验装置不能达到实验目的是
 |  |  |  |
Ⅰ | Ⅱ | Ⅲ | Ⅳ |
A.装置Ⅰ:2NO2 N2O4该反应为放热反应 N2O4该反应为放热反应 |
| B.装置Ⅱ:证明铁钉发生了析氢腐蚀 |
| C.装置Ⅲ:测定酸碱中和反应的中和热 |
| D.装置Ⅳ:测定反应Zn+2H+=Zn2++H2↑的平均反应速率 |
您最近一年使用:0次

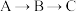 构成,反应能量曲线如图,下列叙述正确的是
构成,反应能量曲线如图,下列叙述正确的是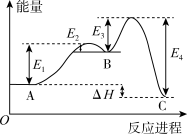

 的反应条件一定要加热
的反应条件一定要加热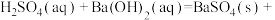
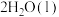
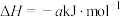
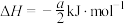


 的摩尔燃烧焓
的摩尔燃烧焓 )是
)是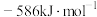
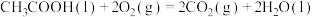
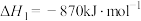

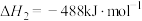
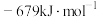
 下,将0.5
下,将0.5 和1.5
和1.5 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成 ,放出的热量为
,放出的热量为